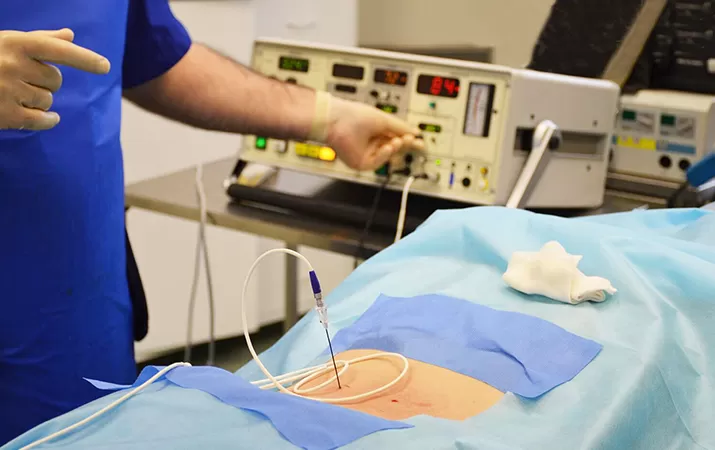
Радиочастотное воздействие нашло широкое применение в онкологии, кардиохирургии, медицине боли. Противоболевой эффект достигается благодаря радиочастотной термоабляции преимущественно сенсорных нервных волокон в лечении хронической локальной боли различного генеза: суставной (фасеточных, тазобедренных, коленных, плечевых, крестцово-подвздошных), ишемической (синдром Рейно, атеросклероз сосудов нижних конечностей), невралгии тройничного, затылочного нерва.
В последние годы активно обсуждается возможность модулирующего влияния радиочастотного воздействия в особом, импульсном режиме при ряде нейропатических болевых синдромов, что открывает новые перспективы в терапии этих сложно управляемых патологических состояний.
 Суть метода
Суть метода
Метод радиочастотной абляции (РЧА) базируется на физическом принципе термокоагуляции и основан на эффекте выделения тепловой энергии при прохождении тока ультравысокой частоты через обладающую импедансом биологическую ткань. Электрод, подключенный к генератору тока, подводится к предполагаемому месту деструкции (сенсорный нерв, симпатические ганглии и т. д.) через изолированную иглу-канюлю, и на него подается высокочастотный переменный ток.
Ток, проходя между «повреждающим» (активным) электродом, погруженным в ткани тела, и индифферентным (пассивным) электродом, вызывает колебания ионизированных частиц тканевой жидкости, в результате чего возникают очаги контролируемого повреждения размером 2–10 мм в диаметре. Наибольший нагрев происходит в области наибольшей плотности тока, которая находится вблизи кончика активного электрода. Классическая термическая РЧА вызывает повреждение нервного волокна за счет нагрева ткани до 80– 90 °C в течение короткого периода воздействия — 90 секунд.
Эффекты
В эксперименте РЧА вызывает следующие гистологические эффекты: валлеровскую дегенерацию нервных волокон, разрывы базальной мембраны, фокусы разрывов периневрия, дегрануляцию тучных клеток, локальные мышечные некрозы, замедленную аксональную регенерацию, изменения в микроциркуляторном русле с экстравазацией эритроцитов, формирующие условия для ишемических изменений после реваскуляризации (рис. 1). Радиочастотно-индуцированная зона коагуляции (размер очага поражения) определяется в первую очередь плотностью тока, длительностью экспозиции, температурой, поддерживаемой на границе раздела электрод/ткань, размером (длиной/калибром) активной поверхности электрода и импедансом окружающей ткани. Рекомендуется поддерживать тканевую температуру ниже температуры кипения (100 °C), поскольку закипание может привести к неконтролируемому газообразованию и горячим потокам вдоль стержня канюли к коже, нарушению геометрии повреждения и закипанию на кончике электрода.
Рис. 1. Электронная микрофотография изменений нервной ткани



Разновидности
В зависимости от формы радиочастотной волны и уровня достигаемой на кончике электрода температуры различают две основные разновидности РЧА: термическую и пульсовую.
При проведении термической РЧА поддерживаемая тканевая температура намного превышает 42 °C. Типично использование продленной (постоянной) РЧ-волны и поддержание тканевой температуры на уровне 70–90 °C. Клиническим эффектом является термическая абляция нерва. К этой категории относится также и метод охлаждаемой РЧА, когда электроды внутренне охлаждаемые, но индуцируемая температура достаточна для нейролизиса.

 Тканевая температура при выполнении пульсовой РЧА поддерживается ниже 42 °C. Генератор производит короткие радиочастотные импульсы, формирующие сильное электрическое поле без большого суммарного теплообразования за счет отведения тепла во время межимпульсных пауз. Клинический эффект заключается в нейрональной модификации посредством электрических и термальных полей, однако точный механизм обезболивания остается объектом исследования. Монополярная импульсная РЧА стала использоваться в ситуациях, где традиционная термальная РЧА была противопоказана (например, нейропатическая боль) или потенциально опасна (например, деструкция ганглиев чувствительных корешков).
Тканевая температура при выполнении пульсовой РЧА поддерживается ниже 42 °C. Генератор производит короткие радиочастотные импульсы, формирующие сильное электрическое поле без большого суммарного теплообразования за счет отведения тепла во время межимпульсных пауз. Клинический эффект заключается в нейрональной модификации посредством электрических и термальных полей, однако точный механизм обезболивания остается объектом исследования. Монополярная импульсная РЧА стала использоваться в ситуациях, где традиционная термальная РЧА была противопоказана (например, нейропатическая боль) или потенциально опасна (например, деструкция ганглиев чувствительных корешков).
Основные направления использования РЧА
Головная и лицевая боль. В лечении невралгий тройничного нерва используется радиочастотная термодеструкция корешка тройничного нерва, или Гассерова узла (рис. 2). В литературе также встречается название «высокочастотная селективная ризотомия» (ВЧС-ризотомия). РЧА тройничного нерва — одна из самых распространенных манипуляций, применяемых для хирургического лечения хронических болевых синдромов.
Рис. 2. РЧА тройничного нерва при невралгии — ризотомия Гассерова узла. 3D-реконструкция и MPR-реконструкция.

 Показаниями к высокочастотной ризотомии тройничного нерва являются наличие некупируемых болей различной этиологии, в т. ч. при одонтогенной природе невралгии, рассеянном склерозе, рецидиве болевого синдрома после микроваскулярной декомпрессии тройничного нерва и др.
Показаниями к высокочастотной ризотомии тройничного нерва являются наличие некупируемых болей различной этиологии, в т. ч. при одонтогенной природе невралгии, рассеянном склерозе, рецидиве болевого синдрома после микроваскулярной декомпрессии тройничного нерва и др.
 Ввиду меньшего риска осложнений РЧА показана в тех случаях, когда выполнение микроваскулярной декомпрессии тройничного нерва невозможно. Противоболевая эффективность в раннем послеоперационном периоде составляет более 90 %. Рецидивы наблюдаются от 20 % случаев в течение 5 лет до 80 % случаев при наблюдении 10 лет и более.
Ввиду меньшего риска осложнений РЧА показана в тех случаях, когда выполнение микроваскулярной декомпрессии тройничного нерва невозможно. Противоболевая эффективность в раннем послеоперационном периоде составляет более 90 %. Рецидивы наблюдаются от 20 % случаев в течение 5 лет до 80 % случаев при наблюдении 10 лет и более.
При рецидиве болевого синдрома возможно повторное выполнение РЧА, однако эффективность каждой последующей манипуляции снижается, а вероятность осложнений растет. Так, среди осложнений в литературе описывают расстройства чувствительности (дизестезии у 1 % пациентов, anesthesia dolorosa у 0,8 %), отсутствие корнеального рефлекса — 5,7 %, кератит — 0,6 %, парез жевательной мышцы — 4,1 %, повреждение черепно-мозговых нервов (добавочный и глазодвигательный) — 0,75 % и наиболее редкие осложнения (истечение цереброспинальной жидкости, каротидно-кавернозная фистула, менингит), составившие 0,35 %. Летальных исходов в литературе описано не было.
При атипичных формах прозопалгий с вовлечением вегетативных ганглиев (например, синдром Чарлина) описаны случаи эффективной радиочастотной термодеструкции крылонебного ганглия. Так, по данным метаанализа 83 исследований интервенционных манипуляций (блокад, РЧА и нейростимуляции крылонебного ганглия), при невралгиях тройничного нерва отсутствие боли после операции отмечают до 25 % пациентов, уменьшение более чем в 2 раза — до 60 %. Кроме атипичных прозопалгий данный метод применяется при кластерной головной боли, постгерпетических невралгиях и вторичных болевых синдромах, например, после удаления краниоорбитальных объемных образований.
В лечении невралгии затылочного нерва положительный результат, по данным различных источников, наблюдался в 75 % случаев, обезболивающий эффект сохранялся в среднем 6,5 месяца. Рандомизированные двойные слепые исследования доказывают преимущество импульсной радиочастотной абляции (ИРЧА) перед блокадой затылочного нерва с кортикостероидами при мигрени. Из побочных эффектов описаны нарушения чувствительности в зоне иннервации затылочного нерва, однако это не доставляет дискомфорта пациенту и не требует дополнительного лечения.
В лечении цервикогенной головной боли, по данным многочисленных исследований, использование радиочастотной денервации дугоотростчатых суставов С2–С6 не имеет преимуществ перед блокадой с кортикостероидами.
Хронический вертеброгенный болевой синдром. Частой причиной вертеброгенной боли является патология дугоотростчатых суставов — фасеточный синдром, который составляет до 40 % цервикалгий и люмбалгий без проявления радикулопатии. Наибольшим обезболивающим эффектом с наименьшим риском осложнений обладает радиочастотная денервация фасеточных суставов (высокочастотная селективная нейротомия нервов Люшка).
В США денервация межпозвонковых суставов на втором месте по частоте выполнения среди всех манипуляций в клиниках, занимающихся лечением хронической боли. Денервация фасеточных суставов выполняется на шейном и грудном уровнях, но наиболее часто — на поясничном уровне.
Успешным считается результат, когда уровень боли снижался на 50 % и более по визуально-аналоговой шкале оценки боли. Наибольший процент успешных процедур (до 90 %) наблюдается у пациентов с положительным ответом от диагностической блокады при правильном выполнении манипуляции. В случаях сомнительного результата диагностической блокады число положительных исходов снижается до 40–50 %.
В группах плацебо, когда проводилась только стимуляция нервов Люшка, положительных результатов не наблюдалось. Рецидив болевого синдрома возникал в среднем через 6–12 месяцев. Однако во многих случаях обезболивающий эффект сохранялся в течение нескольких лет. По данным русскоязычных публикаций, положительный результат достигается в 70–80 % случаев с длительностью эффекта 14–16 месяцев.
Радиочастотная денервация включена в клинические рекомендации лечения фасетогенной боли Американским обществом региональной анестезии и медицины боли, а также в клинические рекомендации по диагностике и лечению фасеточного синдрома пояснично-крестцового отдела позвоночника Ассоциации нейрохирургов России.
Патология крестцово-подвздошного сочленения является источником болевого синдрома в поясничной области в 10–30 % случаев. Для выбора пациентов на высокочастотную денервацию основным критерием является успешный исход диагностической плацебо-контролируемой блокады, которая уменьшает болевой синдром более чем на 50 % по визуально-аналоговой шкале. В настоящее время чаще всего используют методику с постоянным воздействием высокочастотного тока на дорзальные ветви корешков LV, SI–SIII (рис. 3).
Рис. 3. Денервация крестцово-подвздошного сочленения. Интраоперационный рентген-контроль и 3D-реконструкция.


ИРЧА используется в случаях с более высоким риском развития неврологических нарушений из-за повреждения моторных волокон нервов. Так, описан опыт применения ИРЧА задних ганглиев корешков спинномозговых нервов на шейном уровне у пациентов с радикулопатическим болевым синдромом.
Процедура выполнялась пациентам, которым традиционное хирургическое лечение было противопоказано ввиду наличия тяжелой соматической патологии, либо пациентам, отказавшимся от оперативного лечения. Сообщается о снижении болевого синдрома более чем в 2 раза у 67 % пациентов. У половины из них эффект сохранялся более года, а средний период снижения боли составил 37 недель.
Имеются публикации о применении данного метода и на поясничном уровне.
Боли в крупных суставах. Радиочастотная денервация — современный и перспективный метод управления хроническим болевым синдромом в крупных суставах в случаях, когда фармакотерапия и блокады недостаточно эффективны либо осложняются развитием побочных эффектов, а эндопротезирование связано с высоким риском осложнений.
Для денервации плечевого сустава применяется ИРЧА надлопаточного нерва. Так как данный нерв является смешанным, постоянные режимы РЧА используются редко из-за возможного развития парезов верхнего плечевого пояса (надостной и подостной мышц), неврита, концевой невромы. Опубликованные работы по метаанализу исследований денервации плечевого сустава доказывают, что как импульсная, так и постоянная РЧА являются безопасными эффективными методами в лечении хронического болевого синдрома в плечевом суставе.
Денервация коленного сустава также имеет доказанную эффективность. Успешное выполнение радиочастотной денервации отмечается у 60 % пациентов с сохранением эффекта в течение 12 месяцев при низкой частоте развития осложнений манипуляции. Также имеется ряд публикаций по подобным исследованиям относительно тазобедренного сустава. В данном направлении необходимы дальнейшие исследования с использованием рандомизированных плацебо-контролируемых методик.
 РЧА в лечении болевых синдромов различной этиологии. Ввиду высокой противоболевой эффективности РЧА в лечении краниальных и вертеброгенных болей данный метод находит все более широкое применение в лечении боли различной этиологии.
РЧА в лечении болевых синдромов различной этиологии. Ввиду высокой противоболевой эффективности РЧА в лечении краниальных и вертеброгенных болей данный метод находит все более широкое применение в лечении боли различной этиологии.
Имеются публикации о положительных результатах РЧА невромы Мортона (рис. 4). Стойкий обезболивающий эффект достигается у 80 % пациентов и более. Уровень боли при этом снижается в среднем с 8 до 2 баллов по визуально-аналоговой шкале оценки боли. Осложнений при выполнении данного вмешательства не описано.
При авульсии корешков плечевого сплетения с обезболивающей целью выполняется деструкция входной зоны задних корешков спинного мозга с помощью РЧА (DREZ-миелотомия).
Паллиативная помощь. Методы РЧА находят применение и для лечения онкологической боли. В этом случае необходимо провести оценку обезболивающего эффекта и риска возможных осложнений. Также надо учитывать ожидаемую продолжительность жизни пациента. Наиболее часто используют РЧА ганглия тройничного нерва, крылонебного ганглия, затылочного нерва, импульсную РЧА нервных сплетений и отдельных нервов (при раке в области конечностей, таза), хордотомию.
Опыт РНПЦ неврологии и нейрохирургии
В центре выполняется около 100–150 операций с использованием РЧА. Метод применяется при невралгиях тройничного и затылочного нерва, невромах Мортона, травмах периферической нервной системы с образованием концевых невром. Также проводится лечение фасеточного синдрома, имеется опыт денервации крестцово-подвздошного сочленения.
В практику внедрены хордотомия при онкогенной боли, а также деструкция ядра тройничного нерва в тяжелых случаях невралгии тройничного нерва.
Выводы
Радиочастотная абляция — эффективный малоинвазивный и безопасный метод лечения хронических болевых синдромов различной этиологии.
Противоболевой эффект достигается благодаря высокочастотной термоабляции преимущественно сенсорных нервных волокон и сохраняется от нескольких месяцев до года и более.
Лучшие результаты лечения наблюдаются в группах пациентов с предварительно проведенными диагностическими блокадами с местными анестетиками.
Наиболее широко РЧА применяется в лечении хронического болевого синдрома при невралгии тройничного нерва, затылочного нерва, мигрени, фасеточном синдроме, артрозе
крестцово-подвздошного сочленения и крупных суставов: плечевого, коленного, тазобедренного.
Перспективными направлениями исследований являются РЧА невромы Мортона, периферических невром при посттравматической нейропатии, импульсная РЧА при нейропатических болевых синдромах.