В последние несколько лет появляется много новой информации по заболеваниям спектра оптиконейромиелита (ЗСОНМ). Это редкая, но тяжелая воспалительная аутоиммунная патология с преимущественным поражением зрительных нервов и спинного мозга, по своей клинической симптоматике может напоминать рассеянный склероз. Однако ЗСОНМ требуют других подходов к диагностике и лечению. Более того, назначение препаратов, изменяющих течение рассеянного склероза (ПИТРС), может ухудшить течение ЗСОНМ либо вызвать обострение. Заболевание часто имеет инвалидизирующее течение, поэтому своевременная диагностика и терапия чрезвычайно важны.
 С докладом по данной теме на недавно прошедшем республиканском научно-практическом семинаре c международным участием «Рассеянный склероз и другие демиелинизирующие заболевания в практике врача-невролога» выступила Татьяна Чернуха, заместитель директора по научной работе РНПЦ неврологии и нейрохирургии, доктор мед. наук, доцент.
С докладом по данной теме на недавно прошедшем республиканском научно-практическом семинаре c международным участием «Рассеянный склероз и другие демиелинизирующие заболевания в практике врача-невролога» выступила Татьяна Чернуха, заместитель директора по научной работе РНПЦ неврологии и нейрохирургии, доктор мед. наук, доцент.
Этиология и патогенез
— Патология спектра оптиконейромиелита выделилась в отдельную нозологическую форму после открытия антител иммуноглобулина G к аквапорину-4 (AQP4-IgG), — рассказала Татьяна Чернуха. — Часто еще пользуются англоязычным термином neuromyelitis optica spectrum disorders (NMOSD), который был предложен в 2007 году для демиелинизирующих поражений ЦНС, когда при клинической картине оптикомиелита обнаруживаются аутоантитела AQP4-IgG. В настоящее время перечень ЗСОНМ расширен и включает в себя серонегативные случаи. В 2018 году предложены термин «MOG-IgG-ассоциированное расстройство» и критерии его диагностики. Это заболевание также относится к ЗСОНМ, имеет особенности клинической картины и связано с выявлением в крови пациентов антител к миелин-олигодендроцитарному гликопротеину (МОГ, или MOG, myelin oligodendrocyte glycoprotein).
Этиология ЗСОНМ до сих пор уточняется и на сегодняшний день неизвестна. Предполагается присутствие генетической предрасположенности к развитию ЗСОНМ, риск ассоциируется с аллелем гена HLA — DRB1*03.
Триггерами могут быть перенесенные инфекции: кишечные (Сlostridium рerfringens, Еscherichia coli, Нelicobacter pylori), вирусные (вирусы герпеса, Эпштейна — Барр).
Предполагается активация аутоиммунных клонов при коморбидной патологии (ревматическая патология, онкологические заболевания, как правило, у лиц молодого возраста). Представители азиатской популяции более подвержены ЗСОНМ по сравнению с европейской.
— У более 80 % пациентов обнаруживаются антитела против аквапорина — AQP4-IgG, которые играют центральную роль в патогенезе заболевания, — пояснила Татьяна Чернуха. — Эти антитела сопряжены с отростками астроцитов ЦНС и клеток Миллера сетчатки, поэтому отмечается сочетанное поражение спинного мозга и зрительных нервов, что проявляется соответствующей симптоматикой. Основные звенья патогенеза включают активацию В-клеточного звена, дисфункцию гематоэнцефалического барьера, повышенную продукцию противовоспалительного цитокина и интерлейкина 6. Также существенные изменения происходят в системе комплемента.
Средний возраст дебюта ЗСОНМ — около 30 лет. По данным исследований, в большинстве случаев заболевание диагностируется именно в этом возрасте, но может быть впервые выявлено и у пожилых людей (12 %), и у детей (5 %). Детям обычно ставят диагноз в возрасте 10–14 лет, хотя болезнь может манифестировать и в раннем детстве.
Таким образом, на протяжении всей жизни человека есть вероятность установления этого диагноза, его нужно включать в диагностический поиск при соответствующей симптоматике.
Основные клинические проявления ЗСОНМ:
- острый миелит (39,7 %);
- неврит зрительного нерва (32,5 %);
- синдром поражения area postrema (10,6 %);
- острый стволовой синдром (5,5 %);
- симптоматическая нарколепсия, или острый диэнцефальный клинический синдром (4,1 %);
- симптоматический церебральный синдром с типичными для ЗСОНМ очагами в ГМ (3,8 %).
— Диагностические критерии ЗСОНМ были разработаны и приняты в 2015 году для пациентов с выявленными антителами к AQP4-IgG, а также при их отсутствии или при неизвестном AQP4-IgG-статусе, — сообщила Татьяна Чернуха.
Диагноз ЗСОНМ при наличии антител к AQP4-IgG устанавливается, если есть хотя бы одно из шести вышеперечисленных клинических проявлений при условии исключения альтернативных диагнозов (ВИЧ, сифилис, боррелиоз и другие медленно протекающие инфекции).
Диагностические критерии ЗСОНМ при отсутствии AQP4-IgG или при неизвестном AQP4-IgG-статусе:
- не менее 2-х клинических проявлений, явившихся результатом одного или нескольких клинических обострений;
- минимум одно клиническое проявление: оптический неврит или острый поперечный миелит либо синдром поражения заднего поля;
- диссеминация в месте (2 или более различных клинических проявлений, относящихся к категории основных);
- соответствие дополнительным требованиям к МРТ;
- исключение альтернативных диагнозов.
 Дополнительные требования к МРТ у AQP4-IgG-негативных пациентов и при невозможности исследования AQP4-IgG:
Дополнительные требования к МРТ у AQP4-IgG-негативных пациентов и при невозможности исследования AQP4-IgG:
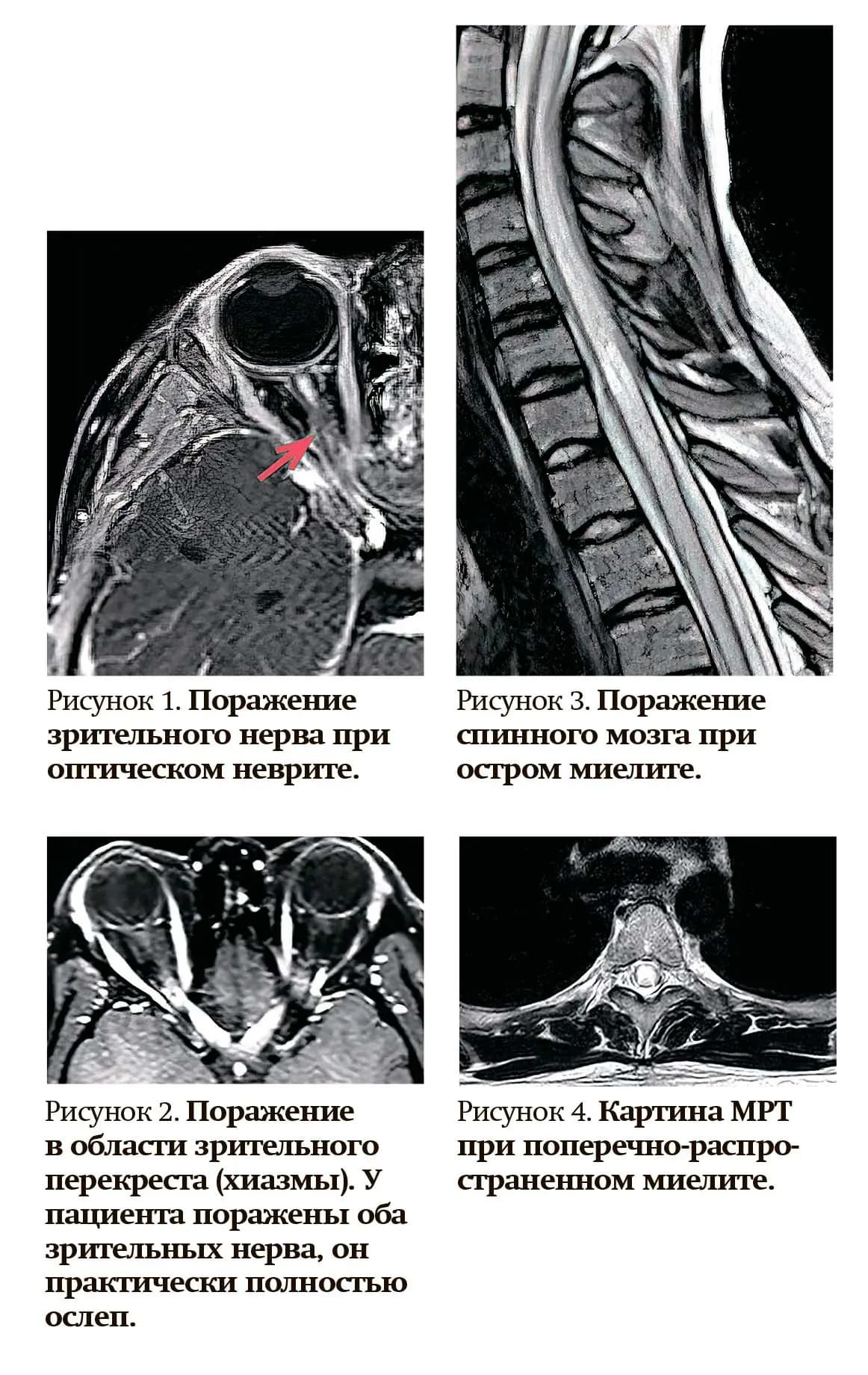
- при остром оптическом неврите в зрительном нерве должны обнаруживаться или Т2-гиперинтенсивные, или накапливающие гадолиний на Т1-взвешенных изображениях очаги поражения протяженностью более 1/2 длины зрительного нерва (см. рис.1) либо вовлекающие область зрительного перекреста (хиазмы) (см. рис. 2).
- при остром миелите: на МРТ спинного мозга наличие интрамедуллярного очага протяженностью ≥3 смежных сегментов либо локальная атрофия ≥3 смежных сегментов спинного мозга (обычно при длительном течении заболевания) (см. рис. 3). Как правило, накопление контраста негомогенное, пятнистое, точечное, но может быть и кольцом, как при рассеянном склерозе, что значительно усложняет дифференциальную диагностику.
— При остром миелите как проявлении ЗСОНМ чаще встречается поперечно-распространенный миелит с поражением более 50 % площади поперечного сечения, центрально и сзади, — уточнила Татьяна Чернуха. — На МРТ с контрастом видны яркие пятна на Т2-режиме (см. рис. 4).
Синдром поражения аrea postrema
 — Синдром поражения area postrema (дословный перевод с латинского — самого заднего поля) весьма специфичен для заболеваний спектра оптиконейромиелита, — подчеркнула эксперт.
— Синдром поражения area postrema (дословный перевод с латинского — самого заднего поля) весьма специфичен для заболеваний спектра оптиконейромиелита, — подчеркнула эксперт.
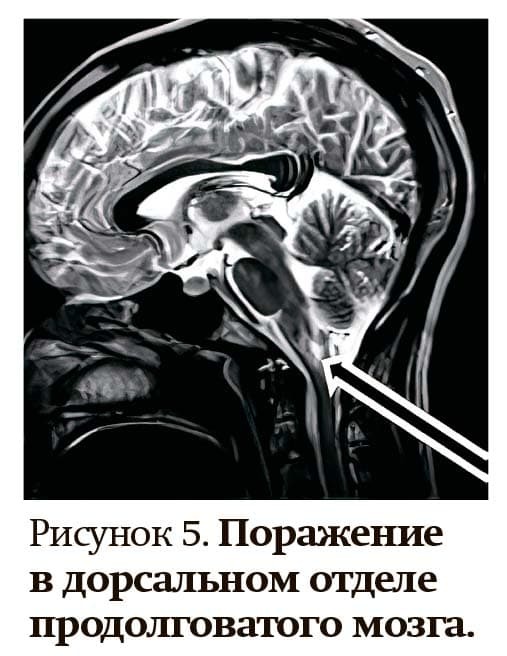
— Его частота довольно высокая — до 51 %, то есть он отмечается почти в половине случаев. Часто сопровождается некупируемой икотой, тошнотой, рвотой, что может продолжаться от нескольких дней до нескольких недель. При такой характерной симптоматике обязательно стоит задуматься о ЗСНОМ. На МРТ выявляются очаги поражения области area postrema в дорсальных отделах продолговатого мозга (см. рис. 5).
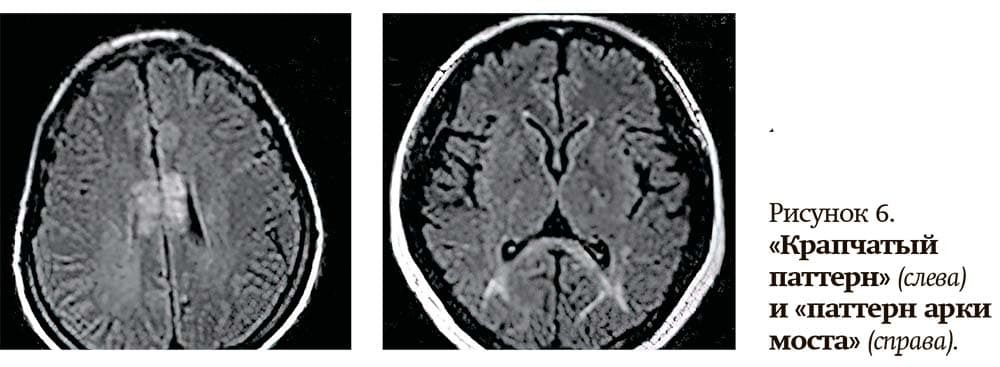
Татьяна Чернуха сообщила, что в последние годы описаны новые особенности, которые выявляются при проведении МРТ у пациентов с ЗСОНМ и на которые следует обратить внимание специалистам по лучевой диагностике. В частности, это «крапчатый паттерн» и «паттерн арки моста» (см. рис. 6).
Татьяна Чернуха:
Если при подозрении на ЗСНОМ и проведении исследования на антитела AQP4-IgG получаем отрицательный результат, то таких пациентов обязательно следует направить на скрининговое исследование по выявлению антител к миелин-олигодендроцитарному гликопротеину.
MOG-Ig-ассоциированное расстройство
Специалист обратила внимание на существование анализа на антитела к миелин-ассоциированному гликопротеину (МАГ), которые малоинформативны в данной ситуации. Поэтому в направлении на исследование лучше избегать сокращений, а писать полное название, что снизит вероятность ошибок и путаницы в лаборатории.
— Большинство пациентов с клиническими проявлениями ЗСОНМ, у которых определяются антитела к MOG, являются AQP4-IgG-серонегативными, — уточнила Татьяна Чернуха. — В нашей практике мы не встречали пациентов, у которых эти два вида антител присутствовали бы одновременно и два исследования были бы положительными. Характерная клиническая особенность для пациентов с наличием MOG-Ig и отсутствием AQP4-IgG — молодой возраст, у 10 % пациентов течение заболевания имеет однофазный характер. У нас есть пациенты, у которых отмечалось лишь одно обострение заболевания, далее они живут без рецидивов.
 Татьяна Чернуха сообщила, что все больше врачей-неврологов и экспертов, занимающихся проблемой ЗСОНМ и рассеянным склерозом, склоняются к тому, что MOG-Ig-ассоциированное расстройство является самостоятельным заболеванием со следующими особенностями:
Татьяна Чернуха сообщила, что все больше врачей-неврологов и экспертов, занимающихся проблемой ЗСОНМ и рассеянным склерозом, склоняются к тому, что MOG-Ig-ассоциированное расстройство является самостоятельным заболеванием со следующими особенностями:
- характерен ретробульбарный неврит с одновременным или последовательным вовлечением глаз, миелитом, реже стволовыми или мозжечковыми симптомами;
- молодой возраст, часто при терапии глюкокортикостероидами (ГКС) возникают гормонозависимые формы;
- на МРТ выявляются крупные или продольно-обширные поражения головного и спинного мозга или зрительного нерва. Продольные интраорбитальные поражения зрительного нерва видны с помощью T2, STIR и усиленной гадолинием T1-взвешенной МРТ, часто с периневральным усилением;
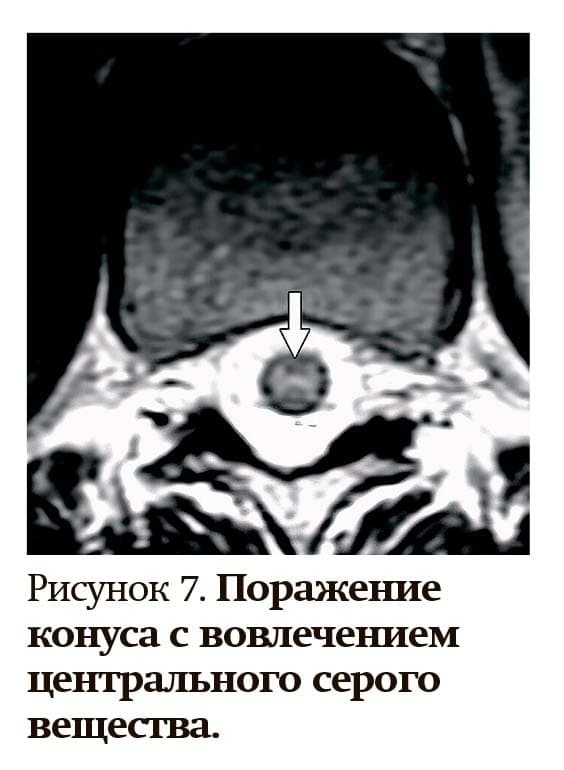
- при миелите на МРТ часто определяется поражение конуса с вовлечением центрального серого вещества, вызывая так называемый знак H (см. рис. 7).
— Поражения головного и спинного мозга при MOG-Ig-ассоциированном расстройстве бывают настолько обширными, что может ошибочно показаться, что это агрессивная либо злокачественная форма рассеянного склероза, — отметила эксперт. — Часто формируются гормонозависимые формы, когда даже при малейшем снижении дозы гормона возникает рецидив. Однако даже единичное обострение может стать причиной необратимых неврологических поражений и, к сожалению, привести к инвалидности.
Татьяна Чернуха:
У большинства пациентов с ЗСНОМ нетрудоспособность нарастает вследствие частых и тяжелых приступов. В течение 5 лет 50 % нуждаются в инвалидной коляске и 62 % становятся слепыми. Поэтому очень важно своевременно поставить правильный диагноз и начать терапию.
Современные подходы к терапии
Татьяна Чернуха проинформировала участников семинара, что в этом году опубликованы международные рекомендации NEMOS по терапии ЗСОНМ. Сформулированы общие принципы лечения, которое преследует две основные цели: терапию обострений и предотвращение дальнейших приступов. При этом рекомендации даются с учетом результатов исследований на антитела.
— Исследования показали, что у пациентов, ранее считавшихся серонегативными, поскольку у них не выявлялся AQP4-IgG, в 40 % случаев выявляется MOG-IgG, а число истинно двойных негативных ЗСОНМ значительно ниже, чем предполагалось ранее, — уточнила специалист. — Стандартом лечения острых приступов как при AQP4-IgG-положительном, так и при двойном отрицательном ЗСОНМ являются высокие дозы глюкокортикоидов и плазмаферез.
Принципы терапии обострений ЗСОНМ:
- терапию следует начинать как можно раньше;
- пульс-терапия ГКС с переводом на пероральный прием в течение 3–6 месяцев;
- пациентам, у которых не достигается достаточное восстановление после применения высоких доз ГКС, следует как можно раньше начать плазмаферез;
- в качестве аферезной терапии могут использоваться плазмаферез или иммуносорбция;
- аферезная терапия может быть вариантом лечения первой линии для пациентов:
- с недостаточным ответом на ГКС во время предыдущих атак,
- достаточным ответом на плазмаферез во время предыдущих атак,
- тяжелым миелитом;
- для пациентов с тяжелыми обострениями целесообразно одновременно назначение высоких доз ГКС и плазмафереза.
Дозирование глюкокортикоидов при терапии обострений:
- метилпреднизолон обычно вводится внутривенно в дозе 1 000 мг в день в течение 3–5 дней (по мнению Татьяны Чернухи, лучше 5 дней);
- далее препарат назначается перорально длительно, следует постепенно снижать дозу метилпреднизолона (начинать с 1 мг/кг/день, а затем постепенное снижение в течение 2–3 недель до 10–15 мг/день) в сочетании с ингибиторами протонной помпы. Лечение следует продолжать в течение 4–6 месяцев.
Предотвращение дальнейших рецидивов заболевания:
- пациентам с AQP4-IgG-положительным ЗСОНМ необходимо предлагать длительную иммунотерапию уже после первой атаки;
- пациентам, которые стабильны на терапии off-label и не имеют существенных побочных эффектов, нет необходимости переключаться на другие методы лечения;
- традиционные иммуносупрессивные препараты (азатиоприн, микофенолата мофетил), пероральные ГКС могут использоваться, но считаются менее эффективными, чем биологические препараты;
- низкие дозы ГКС не следует использовать в качестве монотерапии для предотвращения обострений, требуется назначение иммунной терапии.
Долгосрочная терапия AQP4-IgG-положительных пациентов:
- терапия моноклональными антителами является эффективным методом и повышает вероятность помочь пациентам с AQP4-IgG-положительными ЗСОНМ. Применяются ритуксимаб, тоцилизумаб (off-label), экулизумаб и др. Хотя нет убедительных доказательств, демонстрирующих превосходство одного препарата над другим, каждый из них подходит для различных клинических потребностей и ситуаций;
- выбор иммунотерапии должен основываться на таких факторах, как тяжесть приступа, восстановление после приступа, эффективность, начало действия, сопутствующие заболевания, побочные эффекты/безопасность/смертность, связанные с приемом лекарств, возраст, планирование семьи, предпочтения пациента, приверженность, клиническая полезность и доступность/стоимость;
- длительная иммунотерапия моноклональными антителами должна начинаться как монотерапия, если сопутствующие заболевания не оправдывают комбинацию с классической иммуносупрессивной терапией.
— В мире очень активно накапливается новая информация по ЗСОНМ, буквально каждые полгода появляются новые рекомендации, мы за ними следим и применяем в своей практике, — отметила Татьяна Чернуха. — В настоящее время мировые исследования сосредоточены на обсуждении схем лечения «истинного» двойного негативного NMOSD, при которых не выявлено антител к AQP4-IgG и MOG.
Основные рекомендации NEMOS (2024) по ведению двойного негативного ЗСОНМ:
- долгосрочная иммунотерапия должна быть начата после второго обострения;
- первой линией лечения являются классические иммуносупрессивные препараты или ритуксимаб, в зависимости от характеристик пациента;
- в случае неэффективности терапии ритуксимабом можно рассмотреть комбинированную терапию, тоцилизумаб или другие экспериментальные методы лечения.
— Накопленный опыт по применению ритуксимаба off-label в терапии серонегативных ЗСОНМ в нашем центре оказался достаточно успешным, у пациентов достигнута стойкая ремиссия, — сообщила Татьяна Чернуха. — На протяжении всего лечения мы должны внимательно наблюдать за анализами крови и состоянием пациента, а также учитывать наличие сопутствующих заболеваний. Очень часто у таких пациентов встречается сопутствующая аутоиммунная патология, например, ревматоидный артрит в молодом возрасте, тогда возможно лечение одним моноклональным антителом и того, и другого заболевания. Поэтому при проведении консилиумов необходимо приглашать смежных специалистов, чтобы выработать оптимальную тактику долгосрочной терапии.

