Вторичные иммунодефициты (ВИД) — стойкие нарушения иммунной системы, развивающиеся в позднем постнатальном периоде у детей и у взрослых, не являющиеся следствием какого-либо генетического дефекта и имеющие характерные признаки, которые свидетельствуют, что иммунная система не справляется с антигенной нагрузкой того или иного вида, чаще всего инфекционной. Как следствие, возникают нетипично протекающие инфекционно-воспалительные заболевания, резистентные к традиционной терапии.

О подходах к диагностике и терапии вторичных иммунодефицитов рассказала Татьяна Углова, ведущий научный сотрудник лаборатории клинических исследований РНПЦ детской онкологии, гематологии и иммунологии, кандидат мед. наук, доцент.
ВИД имеют многофакторную этиологию, связанную как с основным заболеванием, так и с его терапией, включая растущий спектр методов лечения, направленных на В-клетки (см. рис. 1).
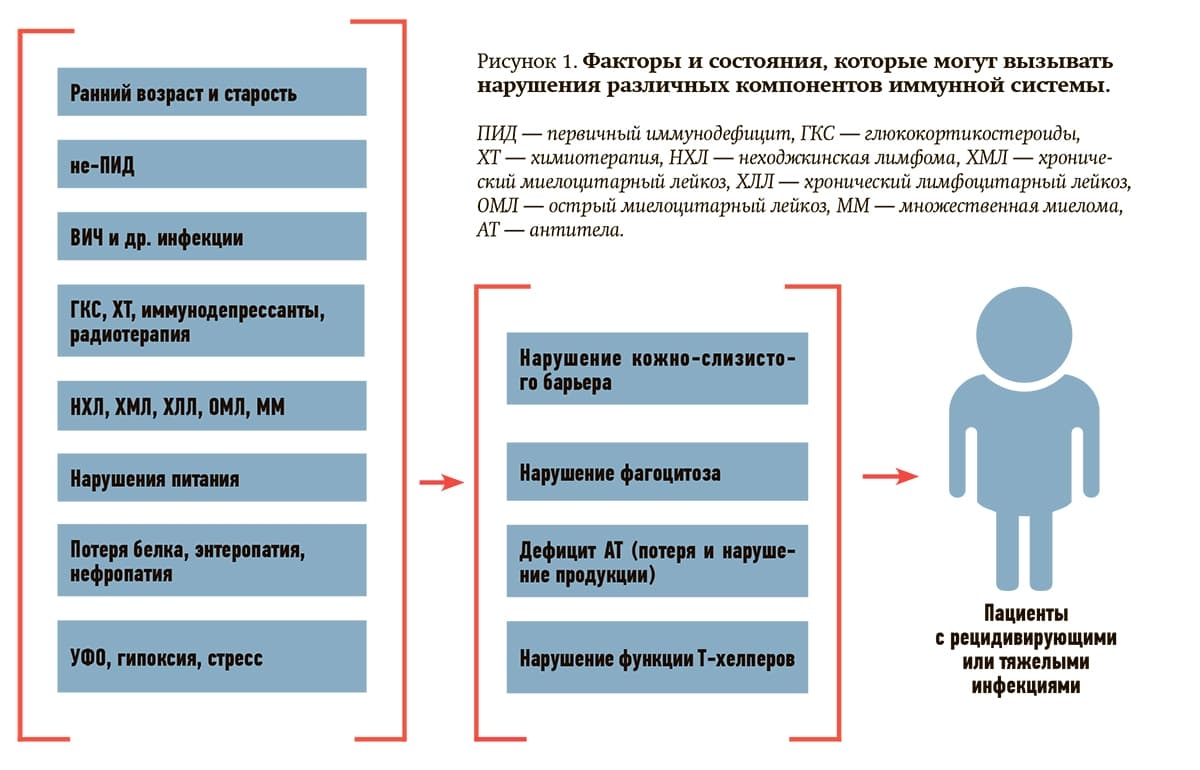
От воздействия причины до развития и диагностики ВИД может пройти до 2 лет.
ВИД — это термин-«зонтик», который объединяет очень разных пациентов как по типу клинических проявлений, так и по степени их выраженности.
Среди всех пациентов с ВИД наиболее многочисленную группу составляют пациенты с вторичным дефицитом антител (ВДА), который встречается в 30 раз чаще, чем врожденный, и в отличие от него является обратимым при устранении причины. Дефицит антител ассоциируется с инфекциями, иммунной дисфункцией, поражением органов-мишеней, увеличением заболеваемости и смертности.
Критерии постановки диагноза ВДА:
- стойкое снижение уровня IgG — более 2 стандартных отклонений от возрастной нормы в детском возрасте и менее 4 г/л у взрослых;
- нарушение специфического антительного ответа на вакцинацию 13- или 23-валентной пневмококковой вакциной;
- тяжелые или рецидивирующие инфекции, плохо отвечающие или устойчивые к стандартной противоинфекционной терапии.
Следует отметить, что уровни IgG сами по себе не указывают на способность В-клеток вырабатывать специфические антитела, поэтому для постановки диагноза ВДА наличие всех трех критериев обязательно.
В отличие от врожденных ошибок иммунитета (новая терминология первичных иммунодефицитов), у пациентов с ВДА выявляются более высокие уровни IgM и IgA, переключенных В-клеток памяти.
Частота ВДА постоянно увеличивается вследствие внедрения новых технологий лечения во всех областях медицины, применения новых таргетных лекарственных средств в качестве монотерапии или в сочетании с иммуносупрессивной терапией, увеличения продолжительности жизни пациентов. В связи с этим становится очевидной необходимость выявления факторов риска развития ВДА у конкретного пациента, разработка стратегий скрининга, мониторинга и терапии. Основные причины развития ВДА представлены в таблице.
Таблица. Наиболее частые причины развития вторичного дефицита антител.

Анализ причин наглядно свидетельствует, что ВДА — это мультидисциплинарная проблема клинической медицины.
Выявление и мониторинг состояния пациентов с высоким риском развития ВДА позволит предотвратить развитие у них тяжелых инфекций. Необходимо помнить, что к группе высокого риска относятся не только пациенты с лимфопролиферативными и другими гематологическими заболеваниями или после трансплантации органов и тканей, но и с соматической патологией, получающие преднизолон в среднегодовой дозе, превышающей 12,5 мг/сутки, а также пациенты, получившие более 8 введений ритуксимаба или те, у которых после его введения отмечалось снижение не только IgG, но и IgM, либо пациенты, получившие до введения ритуксимаба такие лекарственные средства, как пуриновые аналоги, рекомбинантный гранулоцитарный колониестимулирующий фактор, преднизолон.
Пациентам, отнесенным к группе высокого риска, необходимо регулярно (один раз в 3–6 месяцев) определять уровни иммуноглобулинов в сыворотке крови.
Основания для подтверждения/исключения ВДА:
- затяжное течение инфекционных заболеваний, плохо отвечающих/устойчивых к стандартной противомикробной терапии;
- активация условно-патогенной флоры, микст-инфекция, смена инфекционного агента в динамике заболевания;
- инфекции, обусловленные оппортунистическими агентами;
- микозы различных органов;
- рецидивирующие герпетические инфекции (более 4–6 раз в год);
- острые респираторные заболевания более 4 раз в год у взрослых или 8 раз в год у детей;
- эпизоды тяжелых системных инфекций (менингиты, сепсис);
- стойкий диарейный синдром;
- наличие причинного фактора, вызывающего ВДА.
Постановка диагноза ВДА
1. Сбор иммунологического анамнеза.
2. Анализ клинических проявлений нарушений иммунитета.
3. Иммунологическое обследование (общий анализ крови, определение уровня иммуноглобулинов в сыворотке крови, определение специфических антител к конкретным антигенам, определение субпопуляций лимфоцитов методом проточной цитофлуориметрии, другие иммунологические тесты по показаниям). Недостаточность специфического антительного ответа определяется как неспособность хотя бы 2-кратного повышения титра антител IgG в ответ на вакцинацию против пневмококка.
Следует отметить, что при выявлении снижения уровня IgG в сыворотке крови и наличии признаков иммунодефицита необходимо исключить врожденный характер выявленных нарушений, так как их дифференциальная диагностика только на основании этих признаков затруднительна.
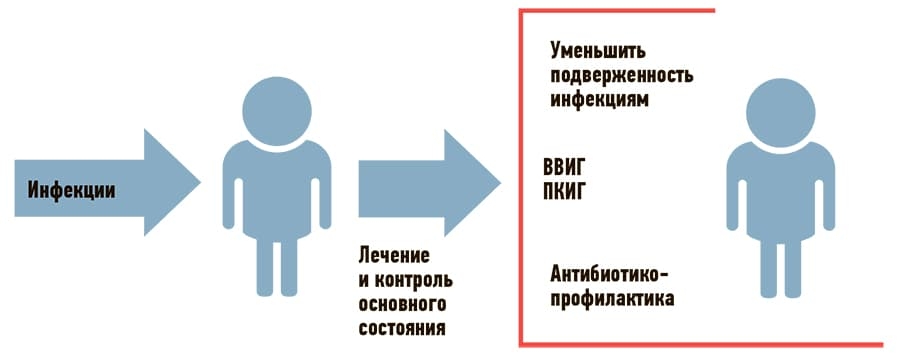
Менеджмент пациентов с ВДА должен быть сфокусирован на устранении ятрогенных причин (например, прекращение приема препарата или лечение основного заболевания) и профилактике инфекционных осложнений, включающей вакцинацию пациента и его окружения, профилактический прием антибактериальных препаратов и заместительную терапию препаратами иммуноглобулина (см. рис. 2).
Рисунок 2. Основные принципы менеджмента пациентов с ВДА. ВВИГ — внутривенные иммуноглобулины, ПКИГ — подкожные иммуноглобулины.
Антибактериальная профилактика
Первая линия при ВДА. Может быть прерывистой (только в зимнее время) или круглогодичной. Обычно используются малые дозы антибиотиков (1/2 суточной дозы). Выбор режима профилактики определяется на основе клинических данных пациента и клинических рекомендаций, утвержденных регулирующими органами. При развитии инфекционного процесса целесообразно применение антибактериальной терапии другой линии, а не просто увеличение дозы антибиотика, используемого для профилактики.
Заместительная терапия препаратами иммуноглобулина
Согласно рекомендациям Европейского агентства лекарственных средств (EMA) 2018 года (действуют с января 2019 года), заместительная терапия препаратами иммуноглобулина для внутривенного введения применяется у пациентов с ВИД при наличии трех условий:
- выявление тяжелых или рецидивирующих инфекций c доказанной неэффективностью стандартной антибактериальной терапии;
- уровень IgG в сыворотке крови менее 4 г/л (400 мг/дл) у взрослого пациента и снижение более чем на 2 стандартных отклонения от возрастной нормы в детском возрасте;
- доказанная недостаточность специфического антительного ответа.
Заместительную терапию препаратами иммуноглобулина необходимо начинать в ходе либо после однократной тяжелой или рецидивирующей хронической инфекции или ее обострения при условии адекватной противоинфекционной терапии и нарушении поствакцинального ответа.
При уровне IgG <2 г/л у подростков и взрослых начинают заместительную терапию без необходимых дополнительных функциональных тестов.
Как правило, заместительная терапия — это комплексное решение мультидисциплинарной команды с включением клинического иммунолога. Базируется на международных рекомендациях, принятых в онкогематологии.
Доза определяется на основании массы тела пациента и составляет 0,2–0,4 г/кг/месяц. При отсутствии клинического улучшения возможно повышение дозы до 0,6–0,8 г/кг/месяц. У пациентов с ожирением доза рассчитывается на основании долженствующей массы тела. Длительность терапии определяется периодом клинического улучшения: минимум 6 месяцев без клинически значимых инфекций. Если после отмены заместительной терапии препаратами иммуноглобулина возобновляются рецидивирующие или тяжелые либо хронические инфекции и гипогаммаглобулинемия, возможно повторное назначение заместительной терапии.
У пациентов, страдающих хроническими/рецидивирующими/тяжелыми инфекциями, несмотря на надлежащее противоинфекционное лечение, при уровне IgG в сыворотке крови выше 4 г/л (что может иметь место у пациентов, получающих иммуномодулирующую терапию большими дозами иммуноглобулина внутривенно), пробная иммунизация полисахаридными и полипептидными пневмококковыми вакцинами может быть инструментом принятия решения о необходимости начала заместительной терапии препаратами иммуноглобулина, так как в этих случаях уровень IgG может не отражать функциональный статус иммунной системы
Не применяется заместительная терапия препаратами иммуноглобулина у пациентов с тяжелыми, рецидивирующими или хроническими инфекциями при уровне IgG в сыворотке крови 4–6 г/л и по меньшей мере двукратном повышении специфичных антител после пробной иммунизации, а также при гипогаммаглобулинемии без нарушения антителообразования и при гипогаммаглобулинемии, обусловленной потерей белка.
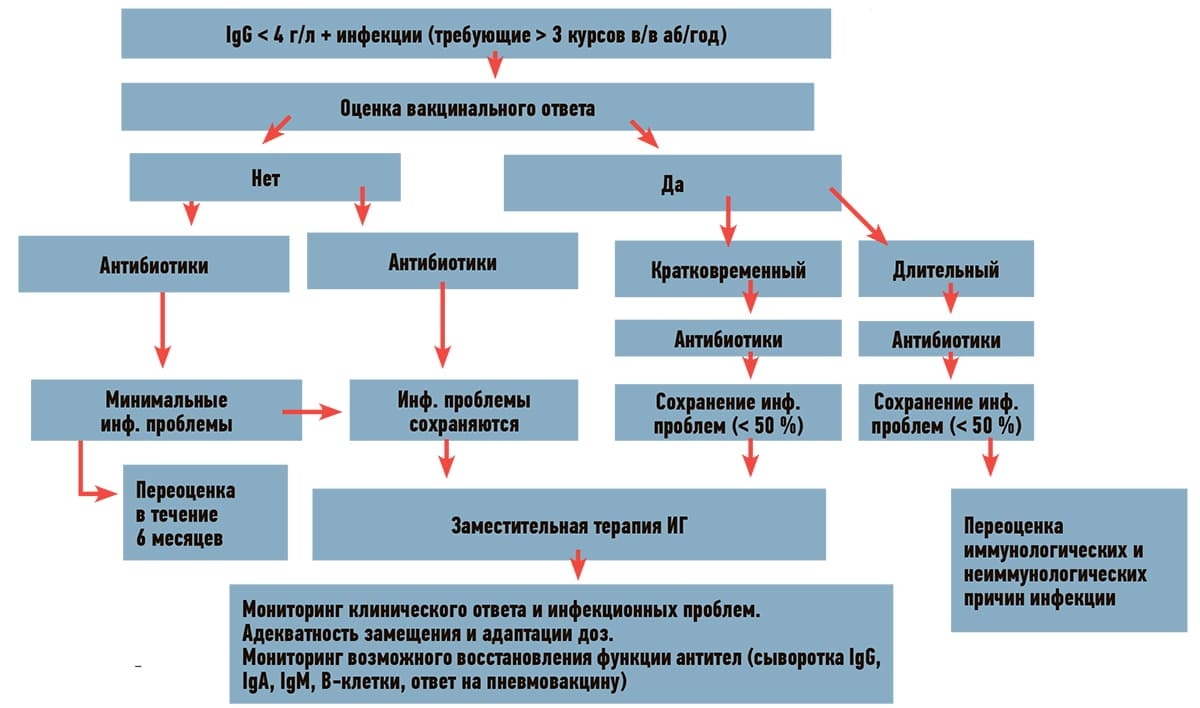
Таким образом, ВДА, как наиболее распространенная форма ВИД, — результат действия разнообразной группы факторов, влияющих на иммунную систему. Четкий мониторинг и рациональная терапия (см. рис. 3) необходимы для снижения вероятности развития тяжелых инфекций у пациентов группы риска ВДА.
Рисунок 3. Алгоритм мониторинга и терапии пациентов с ВДА.