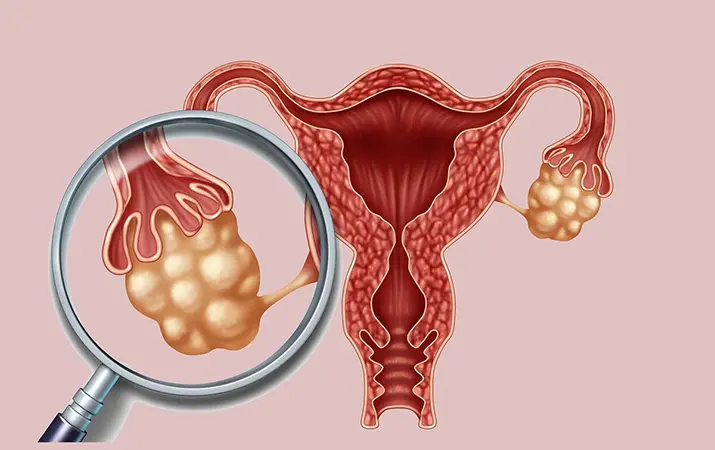
Синдром поликистозных яичников (СПКЯ) — одна из самых сложных и неоднозначных проблем в гинекологической практике, решение которой требует мультидисциплинарного взаимодействия и комплексного подхода. На кону здоровье женщины, репродуктивный потенциал, возможности его реализации. Чаще всего заболевание дебютирует в подростковом возрасте. Этот факт имеет важное значение, поскольку способность врача заподозрить заболевание на раннем этапе расширяет возможности терапии и фертильные перспективы молодых женщин.
Об особенностях диагностики СПКЯ и новейших подходах к терапии синдрома рассказала ассистент кафедры акушерства и гинекологии ИПКиПКЗ БГМУ Оксана Иванишкина-Кудина.
Проблема в масштабе
 СПКЯ — это полигенное эндокринное расстройство, которое обусловлено как генетическими, так и эпигенетическими факторами. На формирование маркеров заболевания, его развитие, длительное, замаскированное течение оказывают влияние метаболические нарушения, особенности пищевого поведения, токсические воздействия и даже принимаемые лекарственные средства.
СПКЯ — это полигенное эндокринное расстройство, которое обусловлено как генетическими, так и эпигенетическими факторами. На формирование маркеров заболевания, его развитие, длительное, замаскированное течение оказывают влияние метаболические нарушения, особенности пищевого поведения, токсические воздействия и даже принимаемые лекарственные средства.
Оксана Иванишкина-Кудина:
Четких данных о распространенности СПКЯ нет, — говорит эксперт. — Она колеблется от 6 % до 20 % в зависимости от среза популяции. В возрастной когорте до 20 лет распространенность в среднем составляет 1 случай на 5 000 населения; к 30-летнему возрасту цифры значительно увеличиваются: 1:1 000.
Реже всего СПКЯ диагностируется у жительниц азиатских стран, таких как Китай, Япония. Чаще — у женщин кавказской национальности.
Эволюция постановки диагноза
В 2006 году европейские ученые C. Sultan и F. Paris впервые указали на отсутствие согласованности в отношении диагностики СПКЯ и предложили алгоритм определения синдрома у девушек и молодых женщин, который требовал наличия 4 из 5 критериев:
- олигоменорея или аменорея через 2 года после менархе;
- клинический гиперандрогенизм (КГА): стойкое акне, выраженный гирсутизм;
- биохимический ГА (тестостерон плазмы >50 нг/дл) и повышение индекса (ЛГ/ФСГ) >2;
- абдоминальное ожирение, нарушения углеводного обмена;
- поликистозная структура яичников по данным УЗИ.
Затем на протяжении почти 20 лет ученые разных стран мира предлагали, дополняли и уточняли разные подходы к диагностике СПКЯ. Так, в 2010 году профессор E. Carmina предложил учитывать 3 Роттердамских критерия диагностики СПКЯ с уточнениями: биохимическая гиперандрогения (БГА) должна определяться по уровню тестостерона в крови, забранной в строго определенное время суток и менструального цикла (МЦ), что создает некоторые трудности, поскольку синдром сопряжен с нарушениями МЦ; КГА диагностируется только у подростков с гирсутизмом; наличие овариальной дисфункции не менее 2-х лет. Причем ни один из критериев не должен использоваться изолированно для диагностики СПКЯ.
В 2018-м было представлено международное научно обоснованное руководство по оценке и лечению СПКЯ, требовавшее для постановки диагноза наличие олигоановуляции и гиперандрогении. Дефиниции нерегулярных менструаций зависели от возраста и были подробно определены. УЗИ не рекомендовалось для диагностики у подростков с гинекологическим возрастом меньше 8 лет постменархе.
В 2020 году российские коллеги Е. П. Хащенко и соавторы определили нормы БГА для подростков. Они впервые акцентировали внимание на важности интерпретации антимюллерова гормона в постановке диагноза, а также индекса свободных андрогенов, тестостерона, соотношения ЛГ/ФСГ. При этом ученые заявили о достоверной доказательности ультрасонографических показателей, которые оценивают не только объем, но и наличие определенных ультразвуковых критериев в оценке фолликулярного аппарата.
И тем не менее до сих пор в гинекологической среде нет четкого и однозначного мнения, стоит ли рассматривать СПКЯ как самостоятельный диагноз в отношении женщин раннего репродуктивного возраста или это всего лишь опосредованный диагноз для ведения женщины с определенной симптоматикой (ановуляцией, нарушением МЦ, выраженной гиперандрогенией).
Что касается взрослых женщин, вопрос об СПКЯ у них возникает при наличии гиперандрогенизма, овуляторной дисфункции, поликистозной структуры яичников по данным УЗИ, а также сопутствующих состояний: хронической ановуляции, бесплодия, патологии эндометрия, гестационного диабета и других осложнений беременности.
Нерепродуктивные и метаболические последствия
Помимо репродуктивных нарушений СПКЯ представляет серьезную проблему в контексте нерепродуктивных и метаболических последствий. К ним относятся:
- гиперинсулинемия (ГИ),
- инсулинорезистентность (ИР),
- нарушения углеводного обмена,
- СД 2-го типа,
- неалкогольная жировая болезнь печени,
- дислипидемия,
- метаболический синдром,
- повышенный сердечно-сосудистый риск.
Оксана Иванишкина-Кудина:
Есть такое понятие, как «смертельный квартет», или синдром Х. Если у женщины с нарушениями жирового обмена есть хотя бы одно из проявлений, таких как гиперинсулинемия, андроидный тип ожирения, нарушение толерантности к глюкозе, артериальная гипертензия, то она входит в группу риска по развитию сердечно-сосудистых заболеваний и увеличению рисков смертности от них.
Критерии Американского общества сердечно-сосудистой патологии выявляют следующие критерии опасности синдрома инсулинорезистентности (1 фактор риска + хотя бы 1 из симптомов).
Факторы риска:
- ИМТ 25 кг/м2,
- ОТ женщины >88 см,
- гиподинамия,
- возраст >40 лет,
- отягощенный семейный анамнез по СД, АГ, ССЗ,
- гестационный диабет,
- наличие АГ или ССЗ,
- повышение тиреотропных гормонов,
- снижение ЛПВП,
- ксантомы,
- поликистоз яичников,
- неалкогольный стеатогепатоз,
- рак.
Симптомы:
- триглицериды 150 мг/дл (>1,7ммоль/л),
- ЛПВП: женщины <50 мг/дл ( <1,29 ммоль/л),
- АД >135/85 мм рт. ст.,
- колебания глюкозы крови натощак:
- 110–125 мг/дл (>6,1 ммоль/л),
- или через 2 часа ОГТТ (толерантность к глюкозе) >140 мг/дл (>7,8 ммоль/л).
Инсулинорезистентность имеет разные маски. Это не только заболевания, связанные с нарушениями жирового обмена. Она может формироваться и отдельно при избыточном питании, наличии опухолей, а также как следствие хронического воспаления.
Оксана Иванишкина-Кудина:
Метаболические нарушения и инсулинорезистентность с СПКЯ представляют собой замкнутый круг. Результаты исследований показывают, что пациентки с СПКЯ и любым ИМТ могут иметь инсулинорезистентность, которая опосредованно влияет на дисфункцию при СПКЯ, нарушая гипоталамо-гипофизарно-яичниковую взаимосвязь.
Теории патогенеза
У СПКЯ много патогенетических теорий: центральная, согласно которой триггером заболевания может служить избыточная секреция андрогенов надпочечниками; инсулиновая; генная; эпигенетическая. Несмотря на многочисленные исследования, до настоящего времени так и не удалось сформулировать единую концепцию патогенеза и этиологии СПКЯ.
В патогенезе заболевания условно можно выделить нарушения в четырех различных отделах нейроэндокринной системы: на уровне гипоталамо-гипофизарной системы, яичников, надпочечников и периферических инсулиночувствительных тканей.
Теория дисфункции митохондрий — тоже одна из любопытных патогенетических теорий. Дисфункции митохондрий на клеточном уровне могут повлиять на системный метаболический баланс. Недавнее широкое признание функциональных митохондриальных нарушений в качестве коррелирующего фактора многочисленных заболеваний привело к предположению, что аномальные митохондриальные метаболические маркеры связаны с СПКЯ. Исследования, проведенные в последние несколько лет, подтвердили, что повышенный окислительный стресс связан с прогрессированием СПКЯ и его осложнениями, а также доказали взаимосвязь между другими митохондриальными дисфункциями и СПКЯ.
Терапия выбора
Оксана Иванишкина-Кудина:
Подходы к лечению СПКЯ зависят от целей, которые мы преследуем, будь то устранение проявлений андрогензависимой дерматопатии, коррекция метаболических нарушений, нормализация массы тела, восстановление овуляторного менструального цикла и фертильности, предупреждение поздних осложнений. Для СПКЯ нет универсальной таблетки, которая бы решала все эти проблемы за раз.
То, с чего нужно начинать, — это изменение образа жизни и мотивирование пациентки.
Все подходы к изменению образа жизни должны быть проанализированы и проконсультированы специалистом. Дальше подключаются терапия ановуляции, терапия гиперандрогении, терапия метаболических нарушений и терапия с антиандрогенным эффектом для регуляции МЦ.
Первой линией терапии нарушений МЦ, гирсутизма и акне является монотерапия комбинированными оральными контрацептивами (КОК), но с четко определенным прогестероновым компонентом.
Вторая линия — метформин, который может назначаться как стартовая эмпирическая терапия либо при наличии противопоказаний или непереносимости КОК.
Для пациенток с СПКЯ, планирующих беременность в ближайшем будущем, оправдана прогестероновая терапия.
При рефрактерных нарушениях овуляции и выраженных метаболических нарушениях могут применяться методы лечения, где на передний план выходит прием инозитола.
Вообще новых идей в терапии СПКЯ много. Одни имеют доказательную эффективность, другие противоречивы, неоднозначны и вызывают некоторый скептицизм. Тем не менее многообразие подходов к терапии не может не удивлять.
Таргетная терапия
Мио-инозитол — линейка не новых препаратов, но до этого неоправданно мало применяемых в гинекологии. Мио-инозитол — неотъемлемый компонент метаболома человека: по крайней мере для 120 инозитол-фосфат-зависимых белков имеется достоверная информация об их специфическом участии в поддержании функционирования репродуктивной системы, развитии эмбриона, нейропротекции мозга плода, обеспечении активности сигнальных каскадов инсулина.
Нарушения обмена мио-инозитола приводят к инсулинорезистентности, резистентности клеток к гонадотропин-рилизинг-гормону, ФСГ и ЛГ, нарушениям овуляции, торможению вызревания ооцитов.
Мио-инозитол напрямую участвует в каскадной реакции гонадотропных рилизинг-гормонов, ФСГ, ЛГ, а затем в процессе выработки прогестерона и овуляции.
Мио-инозитол-зависимые белки непосредственно участвуют в реализации репродуктивной функции, в первую очередь влияя на передачу и донесение гормонов через белки-переносчики к рецепторам ЛГ и ФСГ. Помимо этого инозитол снижает инсулинорезистентность посредством улучшения передачи сигнала от рецепторов инсулина внутрь клеточных ядер, где происходят соответствующие изменения транскрипции.
Очевидно, что основными точками приложения является как раз таки влияние на ЛГ и инсулин. Потому что при развитии поликистоза яичников, при наличии метаболического синдрома и инсулинорезистентности отмечается увеличение ЛГ, инсулина, гиперандрогения, ухудшение качества ооцитов. А мио-инозитол с помощью описанных механизмов уменьшает уровень ЛГ и инсулина.
Воздействие мио-инозитола на инсулинорезистентность исключительно важно для терапии и улучшения качества ооцитов при СПКЯ. исследования показали, что мио-инозитол:
- достоверно снижает уровни тестостерона;
- снижает риск синдрома гиперстимуляции и существенно улучшает протокол лечения пациенток с СПКЯ при подготовке к процедуре ЭКО;
- в комбинированной терапии СПКЯ снижает риск нарушения обмена веществ у пациенток с избыточной массой тела;
- улучшает репродуктивную функцию у пациенток с СПКЯ (в частности, за счет снижения гиперинсулинемических состояний, негативно влияющих на секрецию ЛГ);
- улучшает и восстанавливает МЦ, благотворно влияет на снижение массы тела и жировой обмен.
Эпигенетическая терапия мио-инозитолом
Мио-инозитол является выраженным синергистом фолатов. Они необходимы для метилирования ДНК — процесса, без которого невозможно клеточное деление, и, в частности, для образования функционально полноценных эритроцитов из мегалобластов.
Систематический анализ мио-инозитол-зависимых белков показал, что мио-инозитол также воздействует на процессы метилирования ДНК посредством инозитол-зависимых белков. Поэтому в практике репродуктологии мио-инозитол используется совместно с фолатами.
Двойное слепое РКИ эффектов комбинации мио-инозитола и фолиевой кислоты в группе 92 женщин с СПКЯ показало достоверное улучшение функций яичников.
Применение D-хиро-инозитола и мио-инозитола в рамках прегравидарной подготовки улучшает исходы вспомогательных репродуктивных технологий у женщин с СПКЯ и без СПКЯ. Есть исследования, доказывающие положительное влияние D-хиро-инозитола на качество цитоплазмы ооцитов.
Оксана Иванишкина-Кудина:
Сегодня есть возможность использовать в терапии СПКЯ препараты, которые содержат подобранную в оптимальном соотношении дозу мио-инозитола и D-хиро-инозитола, фолиевую кислоту, витамины, L-глутатион, а также кофермент Q10. Комплексное применение таких препаратов снижает гинекологические риски. Фолиевая кислота давно используется в прегравидарной подготовке, снижая риски пороков развития нервной трубки, анемии, нарушения функции плаценты.
Комплекс мио-инозитола и D-хиро-инозитола улучшает липидный обмен, способствует наступлению регулярного менструального цикла, нормализует работу яичников и улучшает качество яйцеклеток. Поэтому на сегодняшний день препараты с мио-инозитолом рекомендуются и как эпигенетический подход к терапии, и как ведение в прегравидарной подготовке, помогая снижать вероятность развития гестационного диабета и инсулинорезистентности у женщин с уже имеющимся диабетом, риск рождения детей с большим весом.