Распространенность ренальной дисфункции сегодня сопоставима с такими социально значимыми заболеваниями, как артериальная гипертензия и сахарный диабет, а также с ожирением и метаболическим синдромом. Признаки повреждения почек и/или снижение скорости клубочковой фильтрации обнаруживают как минимум у каждого десятого представителя общей популяции. При этом на ранних стадиях заболевание малосимптомно. А позднее выявление ограничивает возможности в лечении — линией спасения таких пациентов становится заместительная почечная терапия.

 В минувшем году в Беларуси количество впервые выявленных пациентов с терминальной хронической почечной недостаточностью составило 83 (годом ранее — 58), согласно данным доклада руководителя Республиканского центра нефрологии, почечно-заместительной терапии и трансплантации почки Олега Калачика на республиканском совещании по итогам работы нефрологической службы Беларуси за 2021 год.
В минувшем году в Беларуси количество впервые выявленных пациентов с терминальной хронической почечной недостаточностью составило 83 (годом ранее — 58), согласно данным доклада руководителя Республиканского центра нефрологии, почечно-заместительной терапии и трансплантации почки Олега Калачика на республиканском совещании по итогам работы нефрологической службы Беларуси за 2021 год.
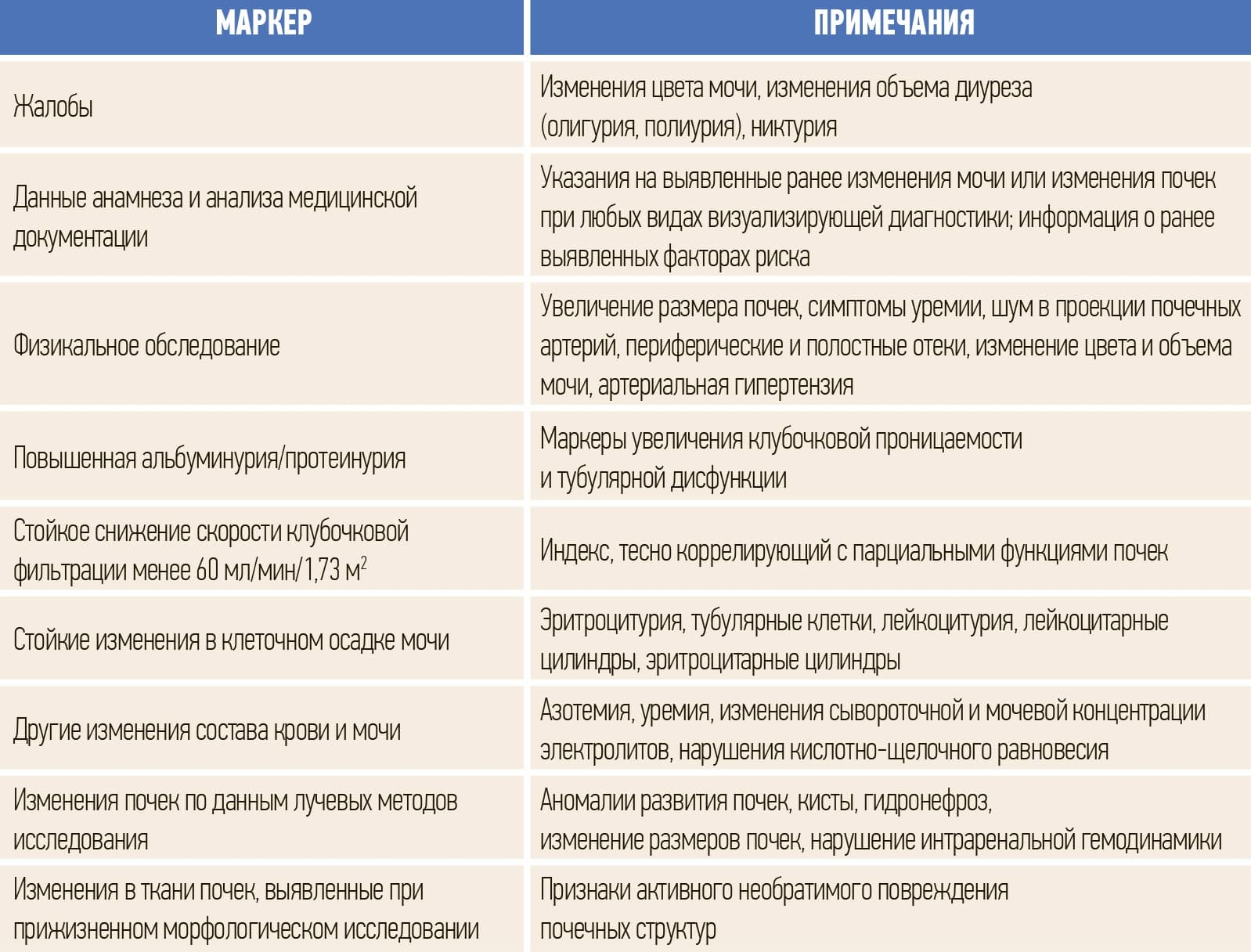
Хроническая болезнь почек (ХБП) — это персистирующее в течение трех месяцев или более поражение почек вследствие действия различных этиологических факторов (см. табл. 1).
Таблица 1. Основные признаки или маркеры, позволяющие предполагать наличие ХБП.
ХБП признана ООН патологией особого внимания как один из индикаторов достижения глобальных целей по сокращению преждевременной смертности от неинфекционных заболеваний к 2030 году.
В отделении нефрологии ГрУК на лечении в 2021 году находились 539 пациентов (в 2020 году — 315) с ХБП 3–5-й стадии. Среди причин, приведших к развитию ХБП, выделяются:
- хронический тубулоинтерстициальный нефрит — 188;
- хронический нефритический синдром — 118;
- сахарный диабет — 114;
- поликистоз почек — 39;
- артериальная гипертензия — 38;
- мочекаменная болезнь — 24.
Таким образом, широко распространенные причины вторичного повреждения почек — сахарный диабет, артериальная гипертензия, метаболические нарушения. В связи с этим понятным и логичным является алгоритм ведения нефрологических пациентов: ранний скрининг ХБП, коррекция факторов риска, изменение в лечении коморбидных состояний с учетом нарушенной скорости клубочковой фильтрации (СКФ), назначение нефропротективной терапии и динамическое наблюдение за пациентом.
К настоящему времени ХБП признана существенным фактором риска сердечно-сосудистой заболеваемости и смертности.
Взаимоотношения дисфункции почек и изменений сердечно-сосудистой системы носят многогранный характер и выстраиваются по типу обратной связи. С одной стороны, почка может выступать как орган-мишень для действия большинства известных факторов, связанных с сердечно-сосудистыми изменениями. С другой стороны, она может активно вмешиваться в формирование системных метаболических и сосудистых патологических процессов, являясь генератором и традиционных, и нетрадиционных факторов риска, тем самым замыкая сложный патогенетический круг, определяющий судьбу пациентов.
Подобный взгляд на взаимообусловленность патологических процессов в сердечно-сосудистой системе и почках, двунаправленность действия факторов риска, клиническая предсказуемость конечных результатов такого сочетания, с одной стороны, позволяет представлять данные взаимоотношения как непрерывную цепь событий, составляющих кардиоренальный континуум, а с другой — открывает дополнительные перспективы первичной и вторичной профилактики не только сердечно-сосудистых заболеваний, но и ХБП.
По данным Европейской ассоциации диализа и трансплантации, почечных реестров США и Японии, Российского регистра хронической почечной недостаточности, сердечно-сосудистые осложнения являются ведущей причиной смертности среди пациентов с терминальной стадией заболеваний почек на заместительной почечной терапии (в структуре общей смертности данной категории больных — от 30 % до 52 %).
В то же время в общей популяции населения в возрасте 45–74 лет снижение скорости клубочковой фильтрации ниже 60 мл/мин/1,73 м2 выступает в качестве независимого фактора риска инфаркта миокарда.
В канадском регистре GRACE (Global Registry of Acute Coronary Events) показано, что у больных с инфарктом миокарда с подъемом сегмента ST, не Q-инфарктом и нестабильной стенокардией при скорости клубочковой фильтрации 30–60 мл/мин/1,73 м2 риск смерти увеличивается в 2,09 раза, а при СКФ менее 30 мл/мин/1,73 м2 — почти в 4 раза.
Смертность от ХБП в 2016 году и прогноз на 2040 год.
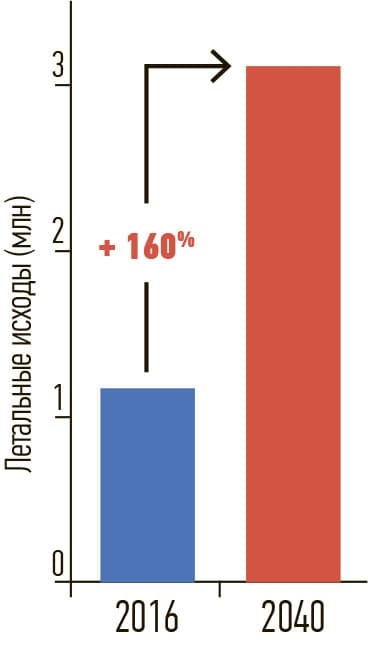 Ежегодно от ХБП умирает более 1,2 млн человек.
Ежегодно от ХБП умирает более 1,2 млн человек.
Летальность при инфаркте миокарда в популяции с терминальной стадией ХБП составляет около 59 % в течение первого года, достигая 70 % к концу второго. По данным другого анализа, включающего более 500 тысяч человек, нижний порог снижения скорости клубочковой фильтрации, при котором отмечается рост относительного риска сердечно-сосудистой смертности, равнялся 75 мл/мин/1,73 м2.
Кроме того, у людей старше 55 лет с исходным уровнем скорости клубочковой фильтрации менее 60 мл/мин/1,73 м2 риск развития ИБС и ее осложнений, в т. ч. фатальных, превышал риск формирования терминальной почечной недостаточности.
Высокий риск кардио-васкулярных осложнений возникает не только в терминальной стадии почечной недостаточности, но и на ранних стадиях снижения функции почек. Это обусловлено комплексным влиянием на миокард и сосуды гемодинамических, метаболических и эндокринных нарушений, сопровождающих почечную дисфункцию.
В связи с этим логичной выглядит рекомендация Ассоциации нефрологов (клинические рекомендации «Хроническая болезнь почек», 2021) о том, чтобы в клинической практике у пациента с вероятными признаками поражения почек врачи любых специальностей проводили диагностику ХБП и классифицировали ее в медицинской документации с указанием:
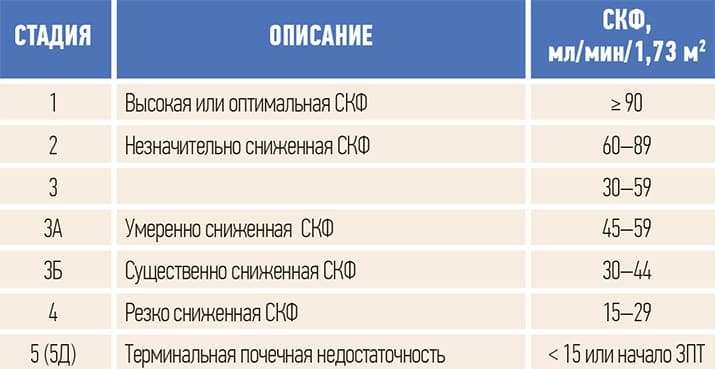
1) стадии в зависимости от значений скорости клубочковой фильтрации, вида заместительной почечной терапии (ЗПТ), факта трансплантации (см. табл. 2);
2) градации выраженности альбуминурии/протеинурии для систематизации статистических данных, оценки прогноза и планирования лечебно-профилактических мероприятий.
Таблица 2. Классификация и стратификация стадий ХБП по уровню СКФ.
Оценка функции почек осуществляется по формулам:
1) CKD-EPI (Chronic Kidney Di-sease Epidemiology Collabora-tion) — наиболее рекомендованная формула;
2) MDRD (Modification of Diet in Renal Disease);
3) формула Кокрофта — Голта используется для оценки клиренса креатинина, используется для расчета СКФ перед назначением новых оральных антикоагулянтов.
Запоминать формулы не нужно, в настоящее время есть калькуляторы — в онлайн-доступе или в виде приложений для смартфона. Следует подчеркнуть, что на сегодняшний день идеально точной формулы нет.
Более того, существует ряд клинических ситуаций, когда использование вышеуказанных формул не рекомендовано в связи с высоким риском получения ошибочных значений СКФ:
- острое почечное повреждение;
- пациенты на диализе;
- определенное диетическое питание (вегетарианская диета, высокобелковая диета, креатиновые добавки);
- экстремальные размеры тела (выраженные истощение и ожирение (ИМТ <15 кг/м2 и >40 кг/м2);
- заболевания скелетной мускулатуры (миодистрофии), параплегия или ампутированные конечности;
- высокая мышечная масса (может занижать СКФ);
- возраст до 18 лет;
- тяжелое поражение печени;
- беременность;
- прием препаратов, способных повышать продукцию креатинина (фенофибрат, альфакальцидол, кальцитриол, парикальцитол, преднизолон); подавлять тубулярную секрецию креатинина (сульфаметоксазол + триметоприм), вступающих в реакцию Яффе (диуретики в высоких дозах, некоторые цефалоспорины) либо снижающих концентрацию креатинина за счет неустановленных механизмов, прямо не связанных с влиянием на деятельность почек (ацетилцистеин).
Следует помнить, что незначительные изменения СКФ могут быть физиологичными.
В настоящее время для определения СКФ используется новый эндогенный маркер цистатин С, по своим диагностическим характеристикам значительно превосходящий креатинин.
Цистатин С — это белок, который:
1) с постоянной скоростью синтезируется всеми клетками, содержащими ядра;
2) свободно фильтруется через клубочковую мембрану, полностью метаболизируется в почках;
3) не секретируется проксимальными почечными канальцами.
Согласно ряду исследований, уровень цистатина С, в отличие от уровня креатинина, не зависит от роста, массы тела, мышечной массы и пола человека.
Показания к назначению измерения цистатина С
1. Рутинный скрининг ренальной дисфункции и связанных с ней ССЗ у всех лиц 55 лет и старше.
2. Оценка ренальной дисфункции любой этиологии и стратификации ее тяжести при:
- гипертензии;
- сахарном диабете и/или метаболическом синдроме;
- патологии почек;
- диабетической нефропатии;
- трансплантации почек и печени;
- операциях с применением аппарата искусственного кровообращения,
- у детей.
3. Быстрая диагностика и стратификация пациентов в отделении интенсивной терапии.
4. При беременности — для оценки риска преэклампсии. (Применение цистатина С для расчета СКФ у беременных сегодня является спорным: одни авторы утверждают, что цистатин С можно использовать для ранней диагностики ренальных нарушений при беременности, другие — что измерение СКФ у здоровых беременных женщин по цистатину С и креатинину дает разные результаты и разница зависит от срока беременности.
Поэтому при определении СКФ у беременных следует учитывать, что разные маркеры имеют разные референтные уровни, которые, в случае цистатина С, например, сильно зависят от срока беременности).
5. При сердечной недостаточности (особенно в сочетании с NT-proBNP и тропонином), в т. ч. ОКС и инфаркте миокарда.
При наличии у пациента тиреоидной патологии, злокачественных новообразований или же на фоне приема высоких доз глюкокортикоидов концентрация цистатина С может меняться.
Что делать, если формульные методы неинформативны, а цистатин С недоступен?
В классическом варианте определение СКФ по клиренсу эндогенного креатинина возможно по пробе Реберга — Тареева: собирается суточная моча, определяется содержание креатинина в крови и моче, минутный диурез и рассчитывается СКФ по формуле:

Поскольку минутный объем фильтрации в почках зависит от роста и веса человека, для нормирования показателя у людей, значительно отклоняющихся в размерах от средних значений, клиренс креатинина пересчитывают на условную величину стандартной средней поверхности тела (1,7 м2).
Для этого нужно знать рост и вес человека. Нормальные значения СКФ (объем крови, очищаемой почками от креатинина за одну минуту) по пробе Реберга — Тареева составляют 80–120 мл/мин/1,73 м2. Начиная с возраста 30–40 лет СКФ постепенно уменьшается (примерно на 1 % в год) и к 80–90 годам составляет лишь половину той величины, которая определяется в 30 лет.
Критерием диагноза ХБП является скорость клубочковой фильтрации менее 60 мл/мин/1,73 м2 продолжительностью 3 месяца и более независимо от наличия других признаков повреждения почек.
При этом ХБП не ставится:
- если уровень СКФ в пределах 60–89 мл/мин/1,73 м2 при отсутствии признаков почечного повреждения, что обозначается как «начальное снижение СКФ» и требует динамического наблюдения и скрининга факторов риска;
- возраст обследуемого 65 лет и старше — это вариант возрастной нормы. Лицам моложе этого возраста рекомендуют контроль состояния почек не реже 1 раза в год и активную профилактику ХБП.
Формулирование диагноза ХБП не должно носить формальный характер. Скорость клубочковой фильтрации нужно динамично отслеживать, что влияет на медикаментозную терапию и ее своевременную корректировку.
Пациентам с ФП рекомендован регулярный контроль функции почек, даже если у них нет диагноза ХБП (см. табл. 3).
Таблица 3. Практические рекомендации Европейской ассоциации аритмологов (EHRA) по применению новых ОАК у пациентов с ФП.
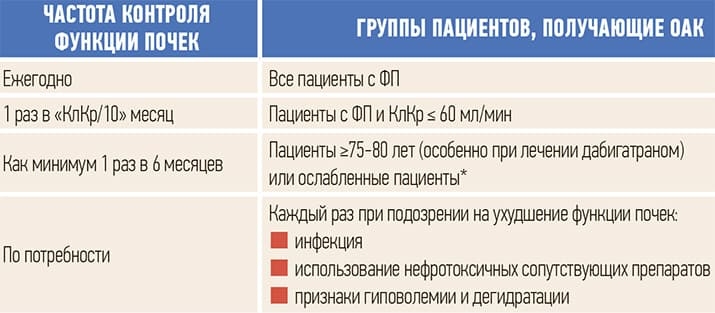
* Определяется при наличии 3 или более критериев: беспричинная потеря веса; жалобы на утомляемость; снижение мышечной силы рук; замедленная ходьба или низкая физическая активность.
ФП — фибрилляция предсердий; ХБП — хроническая болезнь почек; ОАК — оральные антикоагулянты; КлКр — клиренс креатинина.
Правило «делим на 10» описывает условную частоту пересмотра значений СКФ. Например, полученные значения СКФ составили 60 мл/мин/1,73 м2, делим данное значение на 10 и получаем 6, что означает: раз в 6 месяцев пациенту следует пересчитывать уровень СКФ.
Также следует помнить о ситуациях, которые автоматически сопряжены с расчетом значений СКФ, — это инфекции, использование нефротоксичных препаратов, гиповолемия и дегидратация, в т. ч. при назначении диуретиков.