Ежегодно в мире на 1 000 беременностей выявляется один случай онкозаболевания: рак шейки матки или рак молочной железы (более 60 % случаев), лимфомы, рак щитовидной железы, меланома. Лечащий врач беременной пациентки c онкологическим заболеванием сталкивается как с этическим конфликтом, так и с непростой профессиональной задачей — отсроченная диагностика, недостаточно агрессивное лечение, вероятное токсическое влияние некоторых диагностических процедур и медикаментозной терапии на развитие плода.
 Евгения ТихоновичОбо всех нюансах «Медвестнику»рассказала старший преподаватель кафедры акушерства и гинекологии БГМУ, кандидат мед. наук Евгения Тихонович.
Евгения ТихоновичОбо всех нюансах «Медвестнику»рассказала старший преподаватель кафедры акушерства и гинекологии БГМУ, кандидат мед. наук Евгения Тихонович.
Концепция спасения жизни
Беременность может влиять на течение злокачественного заболевания за счет иммунологической, микроциркуляторной и гормональной перестройки организма, однако в настоящее время не существует убедительных научных данных о негативном влиянии беременности на прогноз онкологического заболевания: особенности течения заболевания и прогноз обычно сопоставимы с показателями у небеременных того же возраста и стадии.
В середине прошлого века американский хирург B. F. Byrd опубликовал тезис о том, что не беременность должна быть прервана, а рак. Также российские коллеги выдвинули концепцию спасения жизни: если спасать одну жизнь, то не спасешь никого; если обе, то спасешь минимум одну.
Показания к прерыванию беременности при онкопатологии
Онкологические заболевания, требующие проведения химиотерапии и лучевой терапии, являются медицинскими показаниями для прерывания беременности. Однако современные методы лечения делают возможными ведение желанной беременности у женщин со злокачественными новообразованиями. Тем не менее решение о прерывании может быть принято у пациенток в ранние сроки беременности при распространенных стадиях рака, агрессивном течении злокачественного процесса или необходимости проведения терапии, противопоказанной при беременности.
Допустимая диагностика
Рекомендовано:
- УЗИ грудной клетки, брюшной полости, области таза;
- рентгенография легких и маммография (только с использованием экранирования матки для защиты плода);
- МРТ (без контраста) — не показало негативного воздействия на новорожденных, в том числе на слуховые органы;
- КТ грудной клетки при условии экранирования матки (для безопасности плода доза должна быть ниже пороговой). Если йодсодержащий контраст применялся у беременной парентерально в сроке более 12 недель, то рекомендовано провести исследование функции щитовидной железы новорожденного;
- пункция и последующая биопсия лимфоузлов, сore-биопсия.
Не рекомендовано:
- позитронно-эмиссионная томография (ПЭТ) с изотопом фтор-18, фтордезоксиглюкозой;
- сцинтиграфия костей и лимфоузлов.
Методы лечения
Согласно рекомендациям Европейского онкологического общества, все используемые методы лечения разделены на 3 группы: разрешенные, рекомендованные и противопоказанные.
В первом триместре (0–12 недель) разрешено:
- хирургическое лечение.
Во втором триместре (13–27 недель) возможны:
- хирургическое лечение,
- лучевая терапия (кроме области таза),
- химиотерапия.
В третьем триместре (>27 недель) разрешены:
- хирургическое лечение,
- химиотерапия.
Европейское онкологическое общество также не рекомендует таргетную терапию на всем протяжении беременности в связи с недостатком данных (исключения: ритуксимаб, иматиниб).
Химиотерапия
Назначение полихимиотерапии после 12 недель беременности относительно безопасно, так как процессы органогенеза уже завершены.
Наиболее восприимчивыми к воздействию химиопрепаратов являются органы зрения, слуха, гематопоэтическая и центральная нервная системы плода.
После 35 недель беременности химиотерапию обычно не рекомендуется проводить, чтобы в период между последним циклом химиотерапии и родами костный мозг матери и плода восстанавливался.
Дозы препаратов тщательно рассчитываются, и для многих концентрации минимальны.
Переход препаратов может быть низким (паклитаксел — 0–1 %), умеренным (антрациклины — 5–7 %) и высоким (карбоплатин — 60 %).
В настоящее время нет действующих протоколов, координирующих химиотерапию во время беременности, и поэтому назначаются те же дозы, что и небеременным.
Защитная роль плаценты
Во втором триместре плацента защищает будущего малыша от химиопрепаратов и выступает своеобразным биологическим барьером, что дает возможность не откладывать лечение.
Химиопрепараты могут преодолеть плацентарный барьер способом пассивной или облегченной диффузии, активного транспорта. При этом скорость проникновения зависит от молекулярной массы, липофильности и связи с белками-переносчиками.
Вещества, имеющие низкую молекулярную массу, а также высокую липофильность, которые не ионизируются при физиологических уровнях рН и незначительно связаны с белками плазмы, легче проникают через плаценту.
Кроме того, на материнской поверхности плаценты экспрессируются белки, способные препятствовать проникновению некоторых химиопрепаратов к плоду, такие как Р-гликопротеин и белок резистентности рака молочной железы (BCRP, ABCG2).
Лучевая терапия
При наличии беременности лучевая терапия допустима для воздействия на наддиафрагмальные образования (к ним относятся злокачественные опухоли молочной железы, рак головного мозга, лимфома Ходжкина, опухоли головы и шеи).
Пороки развития плода могут возникнуть при дозе 100–200 мГр и выше (согласно данным Международной комиссии по радиологической защите).
Однако вероятность того, что в детском или юношеском возрасте у ребенка, перенесшего внутриутробную лучевую экспозицию в дозе 0,1 Гр, разовьется злокачественное заболевание, составляет 3 %. Таким образом, доза <0,1 Гр не является показанием для прерывания беременности.
Пренатальный скрининг
На сегодняшний день наши пациентки имеют возможность пройти неинвазивный пренатальный тест. Однако следует помнить, что опухолевые заболевания, включая доброкачественные, а также лечение гемопоэтическими стволовыми клетками являются противопоказаниями к выполнению неинвазивного перинатального скрининга, поскольку с большой вероятностью будет оцениваться хромосомный набор не плода, а опухоли.
Когда по результатам этого скрининга наблюдаются множественные хромосомные аномалии, у женщины можно заподозрить опухоль.
Акушерская и неонатальная помощь
Для выявления задержки роста плода рекомендуется проводить пренатальное УЗИ каждые две недели во время курса антенатальной химиотерапии для того, чтобы мониторировать рост плода и количество околоплодных вод.
Химиотерапия, особенно платиновые и неплатиновые алкилирующие агенты, ассоциирована с преждевременными родами — рекомендуется проводить цервикометрию дважды в неделю у каждой беременной, получающей антенатальную химиотерапию.
Развитие преждевременных родов можно объяснить активацией материнской гипоталамо-гипофизарно-надпочечниковой оси или вызванным химиотерапией апоптозом в плодных оболочках, провоцирующим преждевременный разрыв плодных оболочек.
На фоне химиотерапии у беременных повышен риск развития инфекционных осложнений, анемии и кровотечения.
Плановое родоразрешение на фоне химиотерапии недопустимо. Химиопрепараты, применяемые в непосредственно предродовый период, могут привести к супрессии костного мозга, гемопоэтических клеток и повысить риск развития септических послеродовых осложнений, тяжелой анемии, кровотечения и ранней неонатальной смертности.
По возможности роды следует планировать после 37 недель беременности, чтобы избежать неонатальных осложнений, связанных с недоношенностью.
Рекомендуется придерживаться трехнедельного интервала между окончанием курса химиотерапии и родами — это окно безопасности дает плаценте время для метаболизма химиопрепаратов.
Родоразрешение путем кесарева сечения необходимо при наличии метастазов в трубчатые кости (из-за существенного риска переломов), в ЦНС (так как женщине противопоказаны потуги), при онкопатологии шейки матки и вульвы.
Если необходимо затем продолжить химиотерапию, то начать курс можно не ранее чем через 7 дней после рождения ребенка. Как послеродовый период, так и злокачественная опухоль — независимые факторы риска тромбоэмболических осложнений. С целью профилактики назначается лечение низкомолекулярными гепаринами на весь период нахождения в стационарных условиях.
Чаще всего метастазы поражают плаценту при меланоме, лейкозе, лимфоме, раке легких и раке молочной железы. При этом риск проникновения метастазов в ткани плода составляет 22 %.
Плаценту также могут поражать первичные злокачественные новообразования плода (например, нейробластома).
При обнаружении метастазов в плаценте стоит придерживаться выжидательной тактики. Досрочное родоразрешение оправдано, если метастазы быстро увеличиваются в размерах, имеется подтверждение фетальных поражений плода и неиммунной водянки.
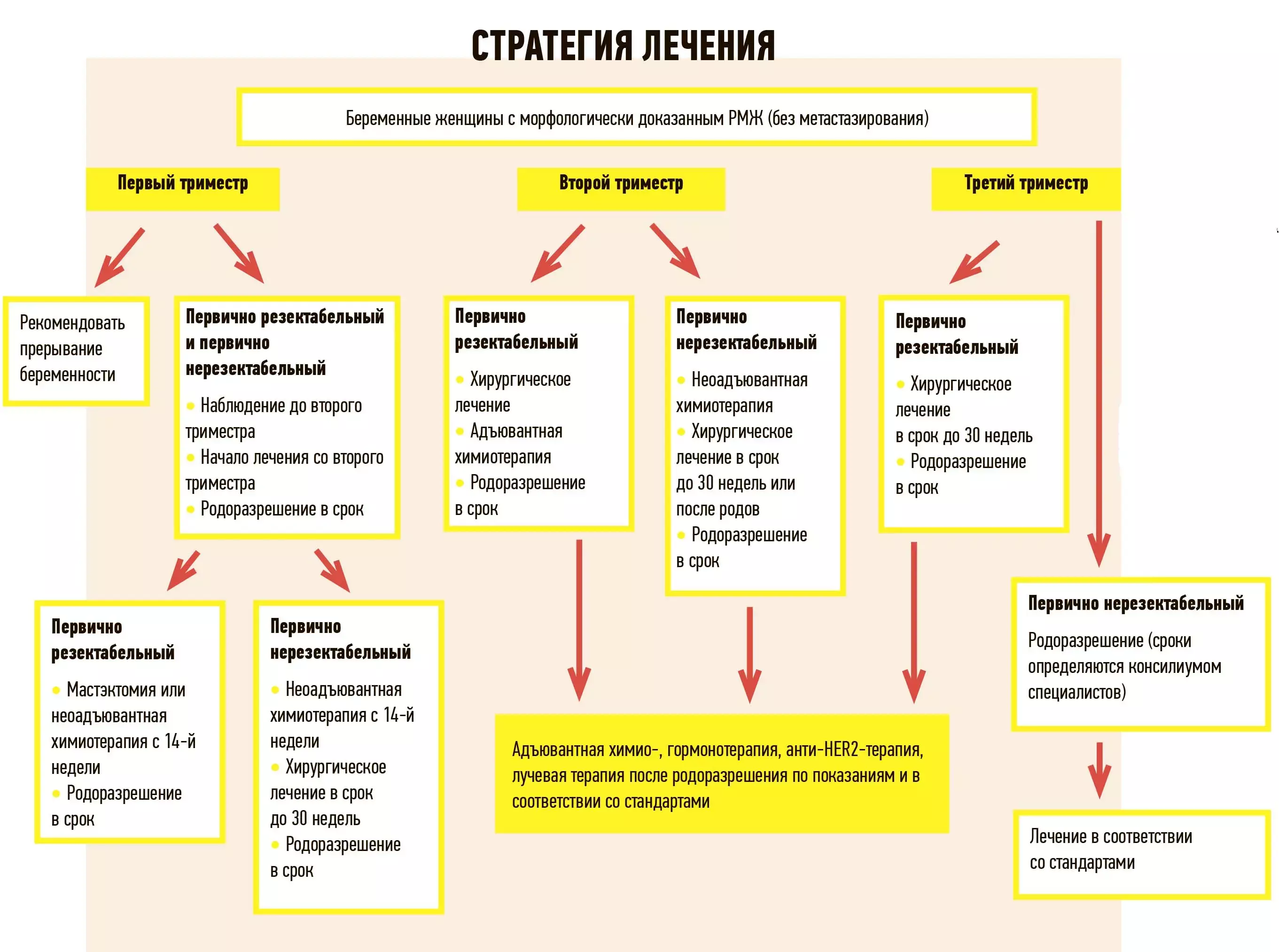
Рак молочной железы
Чтобы оценить степень распространенности злокачественного процесса, используются следующие методы диагностики:
- УЗИ молочных желез и регионарных зон;
- УЗИ органов малого таза и брюшной полости;
- трепан-биопсия опухоли (уровни экспрессии ER, PR, HER2/neu и Ki-67 определяет гистологическое исследование);
- рентгенография органов грудной клетки с абдоминальной защитой;
- МРТ грудного и поясничного отделов позвоночника без использования контраста (клинический протокол минздрава «Алгоритмы диагностики и лечения злокачественных новообразований», 2018 год).
Хирургическое вмешательство допускает как выполнение мастэктомии, так и органосохраняющей операции.
По возможности любого хирургического вмешательства лучше избегать в первом триместре. Во втором и третьем триместрах хирургическое лечение не имеет существенных отличий у беременных по сравнению с небеременными.
На сроке 25 недель и больше в операционной обязательно должны присутствовать акушер-гинеколог и специалист перинатального звена на случай преждевременных родов.
Системную химиотерапию не следует проводить раньше второго триместра.
Важно тщательно подбирать лекарственные препараты. Так, доксорубицин меньше воздействует на плод и считается относительно безопасным. На втором месте по степени токсичности циклофосфамид.
Метотрексат и 5-фторурацил больше других губительны для плода. Побочные эффекты таксанов еще до конца не изучены.
Перед началом каждого курса химиотерапии необходим тщательный мониторинг состояния плода.
Химиотерапию следует прекратить после 35-й недели беременности или за 3 недели до планируемых родов, чтобы избежать возможных гематологических осложнений в родовом процессе.
На протяжении всей беременности противопоказаны гормонотерапия и лучевая терапия. Если есть четкие показания к этим видам лечения, то начинать можно лишь после родов.
На сегодняшний день проблему составляет отсутствие мультицентровых рандомизированных исследований (при наличии единичных когортных и проспективных исследований с коротким периодом наблюдения) диагностики и лечения беременных пациенток со злокачественными заболеваниями.
В основе тактики ведения беременности женщин с онкологическими заболеваниями должно быть совместное обсуждение медицинских специалистов, самой беременной и ее семьи.
Мультидисциплинарная врачебная команда включает онколога, акушера-гинеколога, перинатолога, онкогематолога, генетика, психолога и репродуктолога.
Решение относительно беременности принимается с учетом срока, стадии заболевания, доступных методов терапии и желания пациентки.