Окончание. Начало в «МВ» № 49 от 3 декабря.
Несахарный диабет
Как правило, у пациентов с центральной формой несахарного диабета (НД) осморегулируемая жажда не нарушена и питьевой режим точно компенсирует потери жидкости, однако вероятным осложнением терапии десмопрессином является развитие гипонатриемии.
Ретроспективный анализ данных, выполненный L. A. Behan и соавторами, показал, что 27 % пациентов с центральным НД демонстрируют умеренную гипонатриемию (131–134 ммоль/л) при мониторинге электролитов и у 15 % развивается более тяжелая гипонатриемия (≤130 ммоль/л) в течение длительного периода наблюдения. В то же время гиповолемическая гипонатриемия является общим состоянием при пневмонии различной этиологии и может быть зарегистрирована у 40 % пациентов, при атипичной флоре (легионеллы) — до 50 % случаев, при вирусной этиологии SARS-COV-1 — у 60 %, COVID-19 — в 50 % случаев. Choi K. W. и соавторы отметили достоверную связь гипонатриемии и худшего прогноза течения вирусной пневмонии.
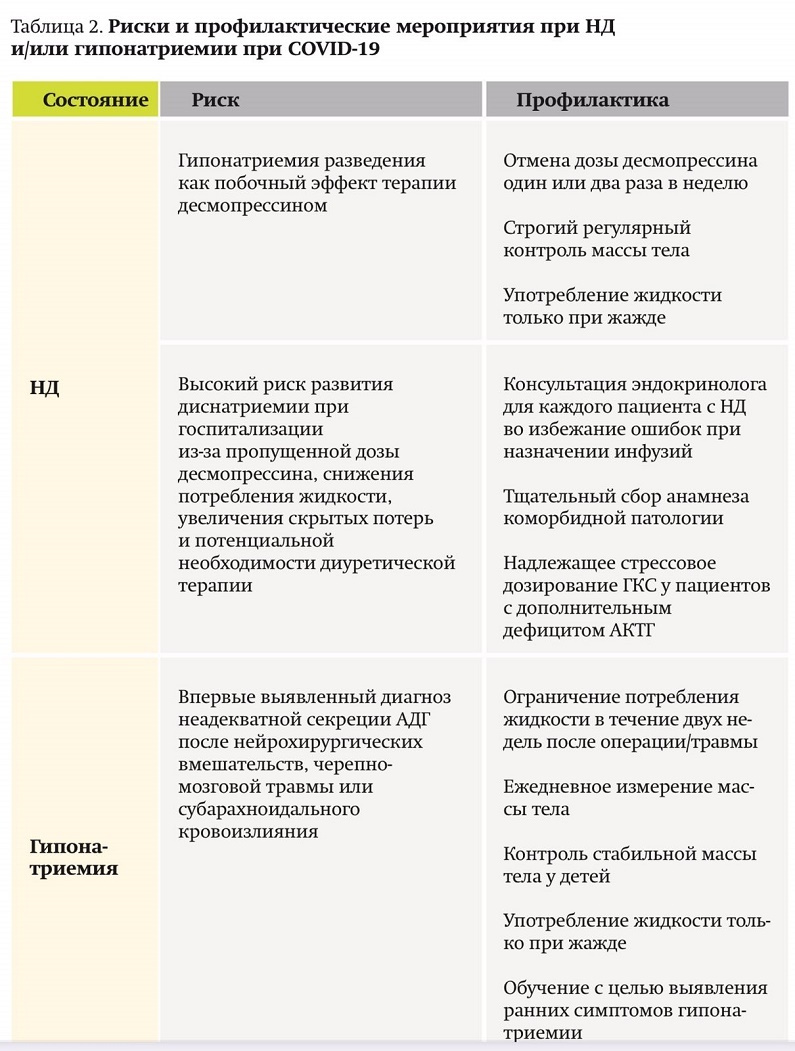
Экспертами Европейского общества эндокринологов разработаны рекомендации по поведению пациентов с НД, гипонатриемией и инфекцией COVID-19. Суммарные риски и профилактические мероприятия см. в табл. 2.
В то же время гипернатриемия является распространенной проблемой COVID-19 в отделениях интенсивной терапии, наиболее вероятно, вследствие скрытых потерь жидкости на фоне стойкой гипертермии и увеличения частоты дыхания. Данная тенденция может усиливаться у пациентов с НД, которые подвержены риску гипернатриемической дегидратации.
Проведение регидратации требует согласованных действий эндокринолога и врача интенсивной терапии. Коррекция гипонатриемии у пациентов с тяжелой COVID-19 осуществляется в соответствии с регламентированными принципами, но с осторожностью в отношении объема внутривенно вводимой жидкости.
Синдром гиперкортицизма
Гиперкортицизм (ГК) — тяжелое нейроэндокринное заболевание, сопровождающееся появлением множества специфических симптомов, развивающееся вследствие воздействия на организм избыточного количества гормонов коры надпочечников (в первую очередь ГКС, в меньшей степени минералокортикоидов и половых стероидов) и представляющее собой сложную клиническую ситуацию независимо от эпидемиологической обстановки.
У здоровых людей на ранней стадии инфицирования физиологические концентрации ГКС приводят к гиперреактивности иммунного ответа, потенцируя экспрессию рецепторов цитокинов и тем самым повышая чувствительность иммунной системы к внешним агентам.
Длительное влияние высоких концентраций ГКС вызывает глубокую иммуносупрессию с угнетением врожденных и адаптивных иммунных реакций. Соответственно, хронический гиперкортицизм может препятствовать первоначальному ответу на внешние агенты и последующей активации адаптивных механизмов. Уменьшение количества В-лимфоцитов и Т-лимфоцитов, а также снижение активации Т-хелперов ассоциированы с риском развития оппортунистической и внутриклеточной инфекции. В результате наблюдается повышенный риск инфицирования, распространенность которой составляет 21–51 % у пациентов с ГК.
У пациентов с активным течением ГК наблюдается супрессия иммунного ответа и повышение риска вирусных и других инфекций. В то же время быстрая нормализация секреции кортизола ассоциирована со снижением риска инфицирования.
Международной группой экспертов по проблемам ГК отмечено, что в условиях ограничения доступности лабораторно-инструментальных методов исследования особенное значение имеет детальная оценка клинической картины (см. рис. 6).
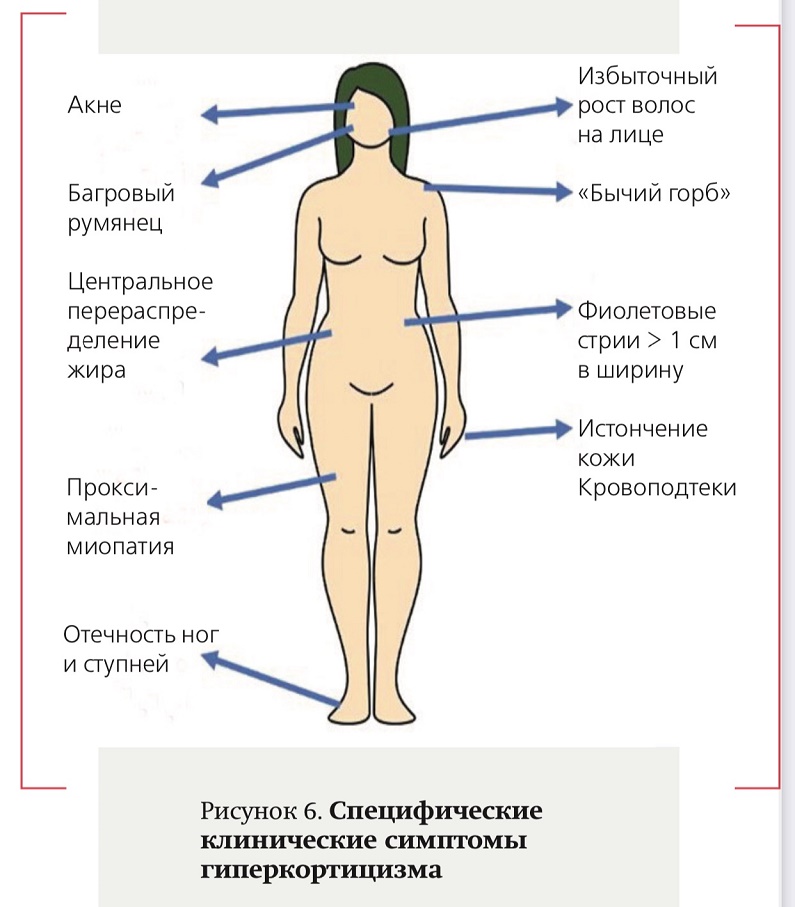
Наиболее яркие симптомы ГК связаны с белковой атрофией и перераспределением жировой ткани. Кроме того, специфичны впервые диагностированная гипертензия, гипергликемия, остеопороз и переломы позвонков, быстрый набор массы тела, которые рассматриваются в качестве наиболее распространенных осложнений ГК и особенно информативные у людей молодого возраста.
Алгоритм лечебно-диагностической помощи пациентам с ГК см. на рис. 7. 
Принципиально выделение группы пациентов с выраженными клиническими проявлениями ГК, которым необходимо проведение обследования в экстренном порядке.
Основой диагностики является исследование суточного кортизола мочи и ночной тест подавления секреции кортизола с 1 мг дексаметазона. В случае подтверждения гиперсекреции ГКС проводится топическая диагностика с целью исключения адренокортикального рака, АКТГ-секретирующего эктопированного образования, макроаденомы гипофиза, которые требуют экстренного хирургического вмешательства. В случае иного источника гиперсекреции ГКС рабочей группой экспертов по проблеме ГК в условиях пандемии COVID-19 рекомендовано консервативное лечение с использованием схемы «блокируй — замещай» в течение 3–6 месяцев (см. рис. 8).

Эффективность блокирования стероидогенеза оценивается по уровню сывороточного кортизола в 9:00 до приема метирапона/кетоконазола и ГКС. Также возможно суточное мониторирование кортизола на фоне перевода на дексаметазон/преднизолон в течение двух дней (до и после назначения). Целью данной схемы терапии является достижение максимально низких значений кортизола.
Наличие как гипокортицизма, так и гиперкортицизма ассоциировано с повышением риска инфекций, что обусловливает необходимость определения данных категорий пациентов в группу повышенного внимания для медицинских специалистов.
Выводы
Большое количество исследований продемонстрировало, что эндокринопатии являются важными факторами риска, влияющими на клиническую тяжесть широкого спектра инфекций. Расстройства иммунной системы, быстрая прогрессия метаболических нарушений играют критическую роль в усугублении тяжести инфекции. Дополнительный дисбаланс функционирования гипоталамо-гипофизарной системы, формирующийся как на фоне избыточной, так и недостаточной функции надпочечников, оказывает существенное негативное влияние на течение инфекции, электролитный дисбаланс требует ургентного ситуационного вмешательства с прогнозом коррекции системной терапии.