Первичные иммунодефициты (ПИД) — группа врожденных генетически детерминированных заболеваний, приводящих к нарушениям в работе иммунной системы. Неспецифичность и вариабельность симптомов, а также низкая осведомленность специалистов часто приводят к поздней диагностике. Среди ПИД есть группа тяжелых комбинированных иммунодефицитов (ТКИД), для которых ранняя диагностика чрезвычайна важна. У новорожденных ТКИД часто протекает бессимптомно, но без раннего выявления и адекватного лечения такие дети погибают в возрасте до года. Таким образом, диагностика ПИД еще до развития клинических проявлений является ключевым моментом успешного лечения данной патологии.
Клиническая манифестация
 При рождении младенцы с ТКИД могут не отличаться от здоровых новорожденных. В течение первого полугодия жизни дети могут расти и развиваться нормально, особенно если не была проведена БЦЖ-вакцинация. В большинстве случаев такую форму иммунодефицита можно заподозрить только при наличии положительного семейного анамнеза.
При рождении младенцы с ТКИД могут не отличаться от здоровых новорожденных. В течение первого полугодия жизни дети могут расти и развиваться нормально, особенно если не была проведена БЦЖ-вакцинация. В большинстве случаев такую форму иммунодефицита можно заподозрить только при наличии положительного семейного анамнеза.
Дебют клинической манифестации охватывает период от нескольких дней до 10 месяцев и в 65 % случаев приходится на первые 3 месяца жизни. Клинически ТКИД проявляется гипоплазией лимфоидной ткани, упорной диареей, мальабсорбцией, поражением респираторного тракта, грибковым поражением слизистых, кожи, ногтей (чаще всего Candida albicans), персистирующими инфекциями, несмотря на проводимую терапию (цитомегаловирус, аденовирус, вирус Эпштейна — Барр, энтеровирусы, герпесвирусы, респираторно-синцитиальный вирус).
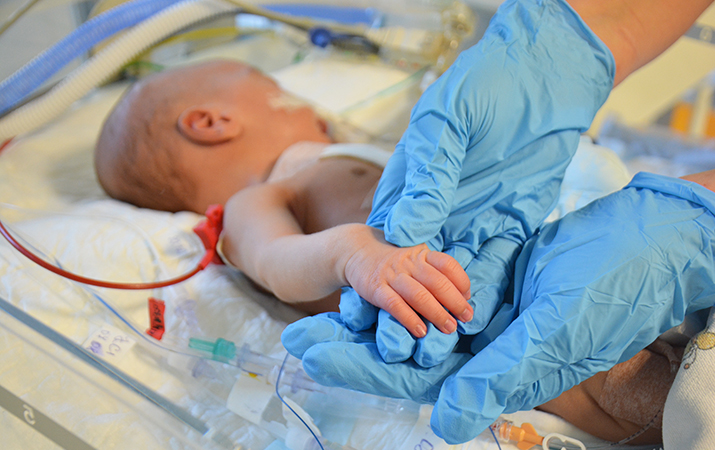
В случае трансплацентарной передачи материнских лимфоцитов могут развиваться симптомы реакции «трансплантат против хозяина», которые проявляются в виде кожной эритематозной или папулезной сыпи — синдрома Омена (см. рисунок). На фоне тяжелых инфекций развивается отставание в физическом развитии.
Клиническая практика показывает, что как можно более ранняя постановка диагноза и назначение соответствующей терапии улучшает качество жизни, предотвращает развитие многих осложнений, снижает летальность, что особенно важно для пациентов с ТКИД.
Наиболее благоприятный исход для этих пациентов достигается трансплантацией гемопоэтических стволовых клеток (ТГСК) или генной терапией, начатой до манифестации инфекционных заболеваний. По результатам научных исследований, проведенных за последние 20 лет, было выявлено, что наилучшим методом лечения пациентов с ТКИД является ТГСК, проведенная в раннем возрасте, до начала инфекции. Установлено, что у младенцев, которым ТГСК выполнена в первые 3 месяца жизни, выживаемость превышает 95 % по сравнению с 74 % среди тех детей, которым ТГСК проведена после 6 месяцев жизни.
Рисунок. Пациент с ТКИД (синдром Омена). Кожная манифестация в виде эритродермии, атопического дерматита.


Диагностика ПИД в РНПЦ ДОГИ
Внедрение диагностических методик ПИД началось в 2005 году в лаборатории иммунологии под руководством кандидата биол. наук Михаила Белевцева.
Данной проблемой занимаются специалисты в области иммунологии и молекулярно-генетической диагностики кандидат биол. наук Светлана Шарапова, старший научный сотрудник Ирина Гурьянова, научный сотрудник Инга Cакович, а также врач-гематолог Светлана Алешкевич, врач-иммунолог Юлия Жаранкова.
Благодаря приобретению современного оборудования, диагностических систем, внедрению актуальных технологий и методик в лаборатории верифицируется диагноз ТКИД у детей с мутациями в генах IL2R, IL7R, RAG1, ADA.
Сложности раннего выявления ТКИД
Применение технологий секвенирования нового поколения имеет высокую эффективность, однако и высокую стоимость для использования в качестве скрининга на ПИД.
Традиционно первоначальное обследование пациентов с подозрением на ПИД состоит из оценки как количественного, так и функционального состояния иммунной системы. Для диагностики проводят исследования субпопуляций лимфоцитов и их пролиферации, количественную оценку уровней иммуноглобулинов, сигнальные пути Т-клеточного рецептора. Этот подход позволяет врачам классифицировать фенотип ПИД у пациента с целью определения приоритетов наиболее вероятных причинных генетических дефектов и принятия терапевтического решения. Однако для него нужно много времени и затрат, следовательно, существует большая потребность в улучшении доступа пациентов к передовым диагностическим технологиям.
Одним из современных и перспективных методов оценки пролиферации лимфоцитов, который может быть использован в качестве теста первой лабораторной линии на ТКИД до определения субпопуляционного состава лимфоцитов, является определение кольцевых структур ДНК (ТРЭК и КРЭК), которые формируются при реаранжировке Т- и В-клеточных рецепторов лимфоцитов и содержат определенные константные последовательности нуклеотидов, по которым их можно обнаружить.
История изучения ТРЭК и КРЭК
ТРЭК были впервые визуализированы с помощью электронной микроскопии в виде кольцевой внехромосомной ДНК в тимоцитах мышей в 1982 году, позже было продемонстрировано, что они являются продуктом перестройки Т-клеточного рецептора. Выяснилось, что ТРЭК были специфичны для наивных Т-клеток, и Douek et al. описали возрастное снижение у здоровых людей и уменьшение уровней при ВИЧ-инфекции. Отмечалось, что ТРЭК стабильны, не подвержены деградации и не реплицируются с последующим делением клеток, и это делает их идеальным маркером для продукции наивных Т-клеток.
В 2005 году Ки Чан и Дженнифер Пак впервые описали применение анализа ТРЭК для крупномасштабного популяционного скрининга на ТКИД и другие формы Т-клеточной лимфопении. Впоследствии метод определения ТРЭК был оптимизирован, и первое пилотное исследование по скринингу ТКИД в штате Висконсин было начато в 2008 году под руководством Джека Рутса и Джеймса Вербски. В том же году была успешно проведена трансплантация первому ребенку с ТКИД, идентифицированным при скрининге новорожденных. В 2009-м скрининг проведен в Массачусетсе, Луизиане и Нью-Йорке, в 2010 году в Калифорнии, Техасе и Пенсильвании. По состоянию на 2018-й скрининг на раннее выявление ТКИД проводился уже во всех штатах США.
В 2007 году van Zelm et al. разработали анализ КРЭК с использованием метода на основе количественной ПЦР в реальном времени. Они продемонстрировали, что уровни КРЭК отражают историю репликации В-лимфоцитов и имеют потенциальную полезность и при выявлении пациентов с нарушениями, связанными с дефицитом антител. В 2011 году была обозначена важность анализа КРЭК для выявления новорожденных с дефицитом В-лимфоцитов и показано, что КРЭК отсутствовали в крови и образцах карты Гатри у пациентов с X-сцепленной агаммаглобулинемией.
По данным международной пациентской организации по первичным иммунодефицитам (IPOPI, www.ipopi.org), в настоящий момент выявление первичных иммунодефицитных состояний у новорожденных методом анализа уровня ТРЭК и КРЭК нашло широкое применение при проведении пилотных исследований по скринингу новорожденных в США, а также во многих странах Европы. Скрининг новорожденных на лимфопению и ПИД проводится в Израиле, Норвегии, Швейцарии, Швеции, Финляндии, Германии, Исландии, Испании (Каталония), Италии (Тоскана), Китае, Тайване. Так, к примеру, в Израиле в 2015–2017 годах было обследовано 290 864 новорожденных и выявлено 13 детей с ТКИД, тогда как в Тайване за 7 лет (2010–2017) обнаружено 7 случаев ТКИД среди 920 398 новорожденных, подвергшихся скринингу, что отражает различный уровень заболеваемости ТКИД в разных регионах.
В странах, где проводились пилотные исследования и скрининг на выявление ПИД, отмечают высокую эффективность и низкую стоимость исследования с определением ТРЭК и КРЭК. Стоимость данного исследования составляет примерно 5–7 долларов США для одного пациента. Метод относительно недорогой, при использовании определения ТРЭК/КРЭК в качестве теста первой лабораторной линии позволяет определить, есть ли у пациента дефект Т- и/или В-клеточного звеньев иммунитета, с целью дальнейшего проведения иммунологических исследований.
В РНПЦ ДОГИ начиная с 2016 года кандидатом биол. наук Марией Стеганцевой совместно с научным сотрудником Екатериной Поляковой велись разработки собственной технологии количественного определения копий ТРЭК и КРЭК методом количественной ПЦР в реальном времени. Был разработан метод, который доказал свою клиническую эффективность в диагностике ПИД и был представлен в инструкции по применению, утвержденной Минздравом Беларуси.
Применение количественного определения ТРЭК и КРЭК
РНПЦ ДОГИ совместно с РНПЦ «Мать и дитя» проведено исследование показателей ТРЭК и КРЭК у детей в возрасте от 1 года до 18 лет, а также у новорожденных, как доношенных, так и недоношенных. По результатам установлен диапазон нормальных значений количественного содержания копий ТРЭК и КРЭК для новорожденных и детей старшей возрастной группы. Согласно данным показателям, в РНПЦ ДОГИ проводится первичное исследование ТРЭК и КРЭК у детей с подозрением на ПИД.
Новорожденные, в особенности недоношенные со сроком гестации менее 37 недель, подвержены высокому риску инфекционной патологии, которая является основной причиной смертности ввиду незрелости врожденного и адаптивного звеньев иммунитета. Тяжелые инфекции, специфичные для неонатального периода, и иммуноассоциированные заболевания, такие как некротический энтероколит и сепсис, являются частыми причинами смерти среди недоношенных новорожденных. Это служит убедительным свидетельством того, что иммунная система таких детей еще более незрелая по сравнению с доношенными новорожденными, как в количественном, так и в качественном отношении.
Иммунологическое исследование периферической крови у новорожденных, особенно у недоношенных, не всегда возможно по причине малого объема крови и инвазивности процедуры. Образцы, адсорбированные на фильтровальной бумаге («сухая капля крови»), представляют собой удобную альтернативу образцам свежей крови. Оценка состояния иммунной системы по «сухой капле» может быть проведена с использованием анализа на ТРЭК/КРЭК.
Учитывая, что для определения ТРЭК и КРЭК используется мультиплексная ПЦР в реальном времени (одновременное исследование показателей), оптимальный срок выполнения данного исследования определяется маркером ТРЭК, для которого свойственно более позднее появление в системе кровообращения новорожденного. Необходимо принимать во внимание срок гестации недоношенного ребенка. Наиболее важным является нижний порог значений.
ВАЖНО! При проведении исследования у недоношенных новорожденных со сроком гестации менее 35 недель и получении низких показателей количества копий ТРЭК при нормальном количестве контрольного гена необходимо повторить исследование после достижения срока гестации не менее 37 недель для получения наиболее информативных данных о состоянии иммунной системы ребенка. Получение низких показателей относительно референсов — повод для расширенного иммунологического и молекулярно-генетического обследования.
Повышение эффективности постановки диагноза
Главным условием успешного дифференциального диагноза ПИД является наличие осведомленности и высокой степени настороженности у специалистов в отношении данных заболеваний. Возможность прогнозировать развитие клинического фенотипа иммунодефицитного состояния на основе генотипических признаков (в частности, определения количества маркеров ТРЭК и КРЭК) позволило бы оптимизировать существующие многоступенчатые диагностические протоколы и повысить эффективность начального этапа диагностики ПИД.
Несмотря на отсутствие доказательства этнической предрасположенности к комбинированным дефектам Т- и В-лимфоцитов, есть сообщения о более частой встречаемости некоторых форм иммунодефицитов в определенных этнических группах. Например, повышенная частота мутаций в гене DCLRE1 отмечена среди народностей коренных американцев в штате Навахо, мутации в гене JAK3 чаще встречаются в Италии, генетические поломки в RAG1 имеют повышенную частоту встречаемости среди славянских народов. В Беларуси большая доля ТКИД с генетическими поломками в гене RAG1 и IL7R выявлена среди детей Брестской и Гомельской областей.
Согласно литературным данным, средний возраст постановки диагноза ПИД при отсутствии скрининга колеблется в разных странах от одного дня до 583 дней, составляя в среднем 138,5 дня (4,2 месяца). В семьях с отягощенным анамнезом по ПИД такие дети, как правило, выявляются раньше и начинают получать адекватное лечение в более раннем возрасте, до развития тяжелой инфекции, однако частота случаев семейной патологии составляет не более 20 % от общего количества больных.
Таким образом введение скринингового исследования с использованием ТРЭК и КРЭК на выявление ПИД важно проводить как новорожденным, так и детям в качестве первой линии диагностики.
Клинические случаи
Пациент М., родился на сроке 25,5 недели гестации от 1-й беременности, 1-х родов (вес 980 г, рост 30 см). Был обследован и находился под наблюдением в РНПЦ «Мать и дитя». У пациента отмечались лейкоцитоз (лейкоциты 71,61×109 г/л) и выраженная лимфопения. При клиниколабораторном исследовании диагноз: сепсис новорожденного, обусловленный анаэробными организмами.
На базе РНПЦ ДОГИ оворожденному было выполнено определение количества ТРЭК и КРЭК.
Из данных таблицы видно, что у пациента отмечается дисбаланс клеточного и гуморального звеньев иммунитета, что характерно для недоношенных новорожденных. Однако ввиду клинической картины сепсиса, низких наивных лимфоцитов и показателей ТРЭК возникла настороженность относительно диагноза тяжелого комбинированного иммунодефицита. Пациент был консультирован врачом-иммунологом Юлией Жаранковой, принято решение продолжать иммунологическое наблюдение в динамике по достижении гестационного возраста не менее 37 недель.
На 47-й неделе клиническая картина сепсиса разрешилась: лейкоциты 6,0×109 г/л, лимфоциты 58 %), количество наивных лимфоцитов в норме, показатели ТРЭК также нормализовались. По причине физиологически нормальных по возрасту иммунологических показателей генетическое исследование не проводилось. Ребенок остается под наблюдением.
Пациентка Л., поступила в возрасте один месяц с лейкопенией и лимфопенией (лейкоциты 4,23×109 г/л, лимфоциты 2,96×109 г/л), критическим снижением относительного количества тимических мигрантов (1,8 %), генерализованной формой ЦМВ, ТРЭК — 0 копий, КРЭК — 0 копий. Ребенку поставлен диагноз ТКИД (Т–В–). Проведено молекулярно-генетическое исследование и выявлена мутация в гене RAG1, приводящая к ТКИД.
Постановка корректного диагноза имеет значение еще и потому, что знание о семейном случае ТКИД позволит вести следующую беременность женщины с обязательным назначением медико-генетического консультирования и наблюдением у иммунолога.