Хроническая боль в животе — боль, которая присутствует на протяжении более 3 месяцев. Она может беспокоить постоянно или периодически (рецидивирующая). Может исходить из любой системы, включая мочеполовую, желудочно-кишечную и гинекологическую. (Продолжение. Начало материала здесь.)
Классификация гастритов
Диагностическая оценка дисплазии. Обычная эндоскопия с использованием белого света не может точно дифференцировать и диагностировать пренеопластические состояния желудка — антральную нодулярность, отсутствие складок, видимые сосуды/истончение слизистой, белые наложения на слизистой.
Антральная нодулярность может быть эндоскопическим признаком (>90 % случаев) для инфекции H. рylori. Однако, за исключением детей, присутствует у минимального числа пациентов с хеликобактерными гастритами среди взрослых (Loffeld R., 1999; Bah A. et al., 1995; Calabrese C. et al., 1999).
Новые эндоскопы высокого разрешения не более надежны. Увеличивающая хромоэндоскопия и эндоскопия в узком спектре (NBI) с/без увеличения и с окрашиванием метиленовым синим, индигокармином, уксусной кислотой, гематоксилином улучшают диагностику пренеопластических состояний/патологий желудка. Однако увеличивающая хромоэндоскопия не может быть рекомендована для рутинного выполнения, а NBI не применяется в ежедневной клинической практике.
Атрофический гастрит и кишечная метаплазия часто неравномерно распространяются по желудку. Для диагностики дисплазии должны быть взяты по крайней мере 4 неприцельных биоптата из 2 топографических мест (из малой и большой кривизны тела и антрума желудка), дополнительно — прицельно из зоны патологии. Системы гистопатологического стадирования OLGA и OLGIM могут быть полезны для определения риска прогрессии в рак желудка. Гистологические данные позволяют диагностировать неопластический эпителий без доказательств инвазии в ткани. Правильная диагностика с определением стадии имеет решающее значение. Существует большая вариабельность гистологических протоколов.
Гистологические данные согласно классификации ВОЗ:
- отрицательные данные для интраэпителиальной неоплазии/дисплазии;
- неопределенная интраэпителиальная неоплазия/дисплазия;
- низкой степени интраэпителиальная неоплазия/дисплазия;
- высокой степени интраэпителиальная неоплазия/дисплазия;
- внутрислизистая инвазивная неоплазия/внутрислизистая карцинома.
(Отрицательная интраэпителиальная неоплазия/дисплазия — хронический атрофический гастрит, кишечная метаплазия. Неопределенная интраэпителиальная неоплазия/дисплазия —
сомнения относительно неопластической или ненеопластической патологии (реактивная или регенеративная); требует дополнительной биопсии.)
Пациенты с распространенным атрофическим гастритом и/или кишечной метаплазией должны проходить эндоскопические исследования каждые 3 года. Нет доказательств о наблюдении пациентов с легкой до умеренной атрофии/кишечной метаплазии, ограниченной антральным отделом.
Пациенты с дисплазией низкой степени при отсутствии эндоскопической патологии нуждаются в обследовании каждый год. При наличии эндоскопически определенной патологии должна рассматриваться эндоскопическая резекция для получения более точного гистологического диагноза.
Пациентам с дисплазией высокой степени при отсутствии эндоскопической патологии нужно повторить эндоскопическое исследование с расширенной биопсией («картография желудка»); показано наблюдение с интервалами 0,5–1 год (Dinis-Ribeiro M. et al., 2012).
Хеликобактерный и нехеликобактерный гастрит. Так как H. pylori — наиболее частая причина гастрита и, вероятно, легко лечится, нехеликобактерный гастрит (см. рис. 3) должен диагностироваться с особым вниманием. Обычно заражение H. pylori пропускается из-за малого числа возбудителей. Такая ситуация возможна, например, когда пациенты недавно принимали антибиотики или ингибиторы протонной помпы либо инфекция вызвана кишечной метаплазией в желудке. Следовательно, помимо взятия биоптатов на уреазный тест, гистологию, врач должен провести серологическое тестирование H. pylori, которое может подтвердить отсутствие патогена.
Рисунок 3. Нехеликобактерные гастриты.
 Аутоиммунный метапластический атрофический гастрит является наследственным аутоиммунным заболеванием, которое поражает париетальные клетки, в результате чего возникает гипохлоргидрия и уменьшается выработка внутреннего фактора Кастла. Последствия включают атрофический гастрит, мальабсорбцию B12 и зачастую злокачественную анемию. Риск аденокарциномы желудка возрастает в 3 раза.
Аутоиммунный метапластический атрофический гастрит является наследственным аутоиммунным заболеванием, которое поражает париетальные клетки, в результате чего возникает гипохлоргидрия и уменьшается выработка внутреннего фактора Кастла. Последствия включают атрофический гастрит, мальабсорбцию B12 и зачастую злокачественную анемию. Риск аденокарциномы желудка возрастает в 3 раза.
Пациенты с аутоиммунным метапластическим атрофическим гастритом имеют антитела к париетальным клеткам и их компонентам, которые включают в себя внутренний фактор и протонный насос Н+/К+АТФазы. Этот гастрит наследуется по аутосомно-доминантному типу. У некоторых пациентов также может развиваться тиреоидит Хашимото и 50 % имеют антитела к тиреопероксидазе щитовидной железы. С другой стороны, антитела к париетальным клеткам обнаружены у 30 % пациентов с тиреоидитом.
Отсутствие внутреннего фактора способствует дефициту витамина B12, что может привести к мегалобластной анемии (злокачественная анемия) или неврологическим симптомам (подострой комбинированной дегенерации). Гипохлоргидрия связана с гиперплазией G-клеток и повышенным уровнем сывороточного гастрина (часто >1 000 мЕД/мл). Повышенные уровни гастрина приводят к гиперплазии энтерохромаффиноподобных клеток, которые иногда претерпевают трансформацию в карциноидные опухоли. У некоторых пациентов аутоиммунный метапластический атрофический гастрит может быть связан с хронической H. pylori инфекцией, хотя отношение не ясно. Резекция желудка и хроническое подавление кислоты с ИПП вызывают подобный дефицит секреции внутреннего фактора.
Диагностика осуществляется параэндоскопическим методом определения рН желудочного сока, затем тестом с конго красным и эндоскопической биопсией. Должны быть получены показатели сывороточного витамина B12. Антитела к париетальным клеткам могут быть обнаружены, но не замеряются рутинно. Вопрос об эндоскопическом наблюдении при скрининге рака является нерешенным, видимо, как и при хеликобактерном атрофическом гастрите. Лечение состоит в заместительной терапии и парентеральной замене витамина B12.
Реактивный гастрит вызывается химическими раздражителями, такими как алкоголь, НПВС и желчь. Обычно вовлекается антрум.
Лимфоцитарный гастрит характеризуется плотным инфильтратом в теле желудка и антруме. Он ассоциируется с целиакией, а также с лимфатическим колитом. Некоторым пациентам помогают ИПП. Диета без глютена приводит к улучшению.
Гипертрофический гастрит (болезнь Менетрие). Изредка складки желудка сильно увеличены в размерах из-за гиперплазии и гипертрофии специализированной кислотопродуцирующей слизистой. Избыточная секреция слизи приводит к синдрому гипоальбуминемии с диареей, отекам или гиперкоагуляционному статусу. Одна из причин — H. рylori. У детей — цитомегаловирус (ЦМВ). Другие причины — идиопатические.
Портальная гипертензионная гастропатия и ангиодисплазия. Ангиодисплазия, вызванная портальной гипертензией, дает картину «змеиной кожи» и «арбузного» желудка. Они могут вызывать потери крови в ЖКТ. При необходимости проводится лечение аргоноплазменной коагуляцией.
НПВС-индуцированный эрозивный гастрит. Аспирин и НПВС — коррозийные препараты, ингибируют синтез простагландина, который необходим для образования слизи и щелочного барьера в желудке. Возникшие эрозии часто бессимптомные, но иногда приводят к язве желудка или дуоденальной язве. Опасный эффект НПВС и H. pylori не синергичный, потому что инфекция повышает уровень простагландина, частично нивелируя повреждающий эффект НПВС. Эрадикация H. pylori до или в начале НПВС-терапии оправдана.
Вирусный гастрит обычно вызывается ЦМВ, отмечается у пациентов со СПИД или тех, кто подвергался трансплантации органа. Для лечения ЦМВ применяется ганцикловир, однако после его отмены бывают частые рецидивы. Случайно может быть выявлена инфекция Herpes simplex.
Бактериальные гастриты вызываются другими инфекциями (Streptococcus, Staphylococcus, Klebsiella и E. coli). Находясь в просвете желудка, такие микроорганизмы вызывают проблемы только при наличии тяжелой ишемии или при супрессии иммунитета. Флегмонозный гастрит возникает, когда такие возбудители способствуют гнойному некрозу стенки желудка. Эмфизематозный гастрит развивается, когда патологические организмы газообразующие.
Грибковый гастрит сам по себе редкий, хотя колонизация язв желудка грибками рода Candida встречается часто. Тяжелый некротический гастрит может быть вызван оппортунистическими грибками у иммуносупрессивных пациентов.
Паразитарный гастрит редок и может быть вызван, например, Strongyloides stercoralis и Cryptosporidium.
Гранулематозный гастрит вызывается инфекциями или токсинами (к примеру, туберкулез, сифилис, гистоплазмоз) и неинфекционными причинами (к примеру, саркоидоз, болезнь Крона и гранулематоз Вегенера). Туберкулезная инфекция может возникнуть при наличии СПИД и диссеминированного туберкулеза. Сифилитический гастрит возникает во второй или третьей стадиях сифилиса.
Эозинофильный гастрит характеризуется интенсивной эозинофильной инфильтрацией антрума, в меньшей степени тела или свода желудка. Может возникнуть при гиперчувствительности к медикаментам или некоторой пище либо в результате паразитарной инфекции. У пациентов отмечаются абдоминальная боль, тошнота или рвота. Тестируется стул на наличие инфекционного патогена. Но в большинстве случаев причины не удается обнаружить. Лечение с кортикостероидами дает эффект.
Сосудистая эктазия антрального отдела желудка, также известная как арбузный желудок, преимущественно отмечается у женщин и ассоциируется с ахлоргидрией и атрофией желудка. Представлены пациенты с острыми и хроническими желудочно-кишечными кровотечениями, приводящим к анемии. Эндоскопически видны красные полосы, сходящиеся к привратнику. Гистология патогномонична и характеризуется сосудистой эктазией, пролиферацией веретенообразных клеток и фиброгиалинозом. Большинство пациентов отвечают на лечение с Nd:YAG лазером или аргоноплазменной коагуляцией. Операция в виде антрумэктомии — последняя надежда.
Портальная гипертензионная гастропатия заметна у пациентов с заболеваниями печени. Мозаичный рисунок слизистой преимущественно наблюдается в теле и своде желудка. Лечение включает неселективные бета-адреноблокаторы (пропранолол или надолол), трансъюгулярное портосистемное шунтирование или портальную декомпрессивную операцию. Локальное лечение лазером или аргоноплазменная коагуляция могут ухудшить ситуацию.
Нет корреляции между микроскопическим воспалением (гистологический гастрит) и наличием желудочных симптомов (абдоминальная боль, тошнота, рвота). Фактически большинство пациентов с гистологическими доказательствами острого гастрита бессимптомны.
Диагностика обычно происходит во время эндоскопии, выполняемой по симптомам диспепсии. Пациент с острым гастритом может испытывать дискомфорт, который трудно описать словами. Диагноз можно заподозрить на основе анамнеза и подтвердить эндоскопически и гистологически в биоптатах, взятых во время процедуры. Макроскопическая диагностика атрофического гастрита рутинной эндоскопией невозможна, выполняется только с помощью красящих методик (см. рис. 4).
Рисунок 4. Эндоскопия с использованием красящих методик.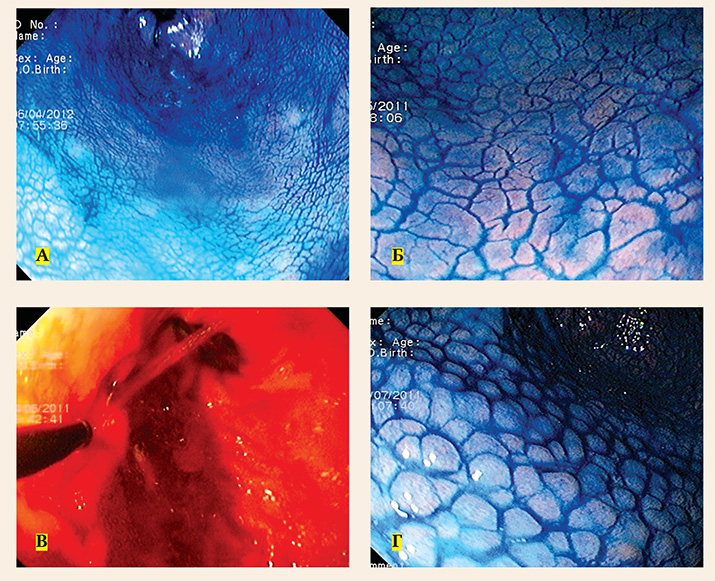 А — нормальный мелкосетчатый микрорельеф антрального отдела желудка. Исследование с метиленовым синим + эспумизан.
А — нормальный мелкосетчатый микрорельеф антрального отдела желудка. Исследование с метиленовым синим + эспумизан.
Б — атрофический антральный гастрит. Феномен «потресканной земли».
В — атрофический фундальный гастрит. Исследование с конго красным (рН-индикатор не изменил окраску в теле желудка).
Г — нодулярный (гиперпластический) антральный (хеликобактерный) гастрит.
