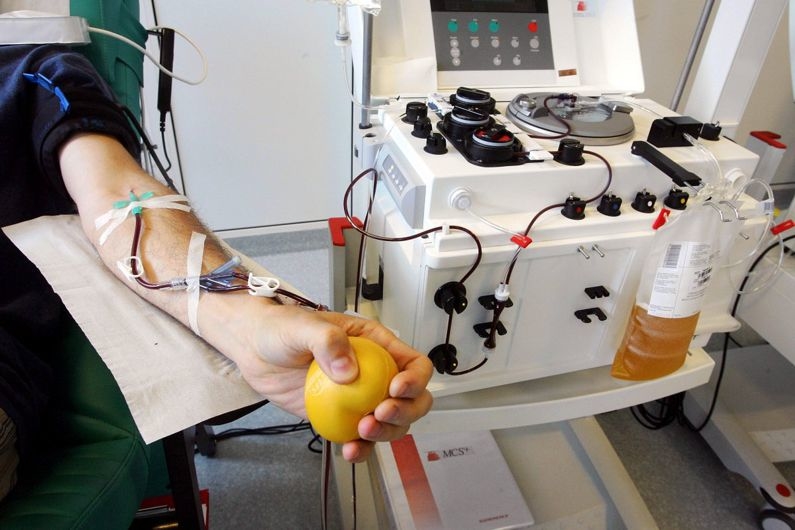
В Беларуси получен успешный опыт применения автоматического плазмафереза в лечении двух пациентов с подтвержденной инфекцией COVID-19. Об этом в интервью «МВ» сообщил начальник центра переливания крови 432-го Главного военного клинического медицинского центра Вооруженных Сил Республики Беларусь, подполковник медицинской службы, кандидат мед. наук Дмитрий Третьяк.
 Дмитрий Станиславович, с самого начала пандемии врачи всего мира ищут способы победить COVID-19, используя разные схемы и методы лечения. Но вот о плазмаферезе, кажется, пока не встречались публикации. Как у вас появилась эта идея? В чем суть лечебного плазмафереза и цель его применения при COVID-19?
Дмитрий Станиславович, с самого начала пандемии врачи всего мира ищут способы победить COVID-19, используя разные схемы и методы лечения. Но вот о плазмаферезе, кажется, пока не встречались публикации. Как у вас появилась эта идея? В чем суть лечебного плазмафереза и цель его применения при COVID-19?
Автоматический лечебный плазмаферез — это одна из методик гравитационной хирургии. В нашем центре переливания крови ГВКМЦ мы используем эту технологию при лечении пациентов c аутоиммунной патологией, псориазом, рассеянным склерозом и некоторыми другими заболеваниями. При лечебном плазмаферезе кровь берется из организма и под воздействием гравитационных сил в специальной центрифуге ее клетки (эритроциты, лейкоциты, тромбоциты) отделяются от плазмы — жидкой части, в которой растворены в том числе патологические субстраты. При аутоиммунных заболеваниях это могут быть патологические антитела, различные иммунные комплексы, эндо- и экзогенные токсины и т. д. Их нужно удалить. Клетки крови возвращаются в организм, а плазма замещается свежезамороженной донорской плазмой или физраствором.
Идея применить плазмаферез при COVID-19 возникла после того, как стало известно, что в патогенезе развития этой инфекции определенную роль играет цитокиновый шторм. На внедрение вируса организм некоторых пациентов дает сильный аутоиммунный ответ, что приводит к развитию опасных осложнений — острого респираторного дистресс-синдрома (ОРДС), генерализованного воспаления и полиорганной недостаточности. Предикторами цитокинового шторма является повышение интерлейкина-6, стимулирующего иммунный ответ, С-реактивного белка и других факторов. Мы предположили, что удаление медиаторов воспаления может заблокировать возникновение цитокинового каскада и предотвратить прогрессирование патологических процессов.
Как развивалась инфекция у этих пациентов?
Они были госпитализированы в отделение ГВКМЦ, перепрофилированное для лечения пациентов с COVID-19. Клиническая картина у них была схожей. По данным КТ, выявлена двусторонняя полисегментарная пневмония. Температура достигала высоких цифр (выше 39 °С) и не сбивалась ни с помощью жаропонижающих, ни с применением других методов. В течение нескольких дней состояние постепенно ухудшалось, дыхательная недостаточность прогрессировала. Пациенты были переведены в отделение реанимации и интенсивной терапии, где находились в прон-позиции, получали кислородотерапию и медикаментозное лечение. Однако их состояние не улучшалось. Через несколько дней средняя сатурация была ниже 90 %, у первого пациента — 88 %, у него уже начиналась спутанность сознания. Оба пациента рассматривались как кандидаты на подключение к ИВЛ.
В ходе консилиума, проводимого начальником отделения ОРИТ Константином Абдиным, обсуждались различные варианты, как избежать развития ОРДС и перевода на ИВЛ. Тогда и появилась идея провести сеанс плазмафереза. Наше мнение поддержал начальник отделения гравитационной хирургии крови Александр Добриянец.
Был ли риск, что ожидания могут не оправдаться? Как проходила процедура и сколько времени заняла? В какой момент стало понятно, что вы на правильном пути?
Разумеется, коронавирусная инфекция — непредсказуемая, невозможно точно предугадать гемодинамику пациента. Для того чтобы снизить риски, первому пациенту мы провели низкообъемный плазмаферез, то есть использовали в процессе сеанса только 30 % циркулирующей крови, это чуть больше, чем при донорском плазмаферезе. Сеанс выполнялся с применением сепаратора для автоматического плазмафереза Autopheresis-C по стандартным алгоритмам: трансфузиологическая бригада настраивает аппарат, подключает контур, врач-трансфузиолог и медицинские сестры наблюдают за параметрами гемодинамики, вычисляют и корректируют оптимальную скорость трансфузии, необходимое число коагулянта в зависимости от параметров коагулограммы. Процедура при низкообъемном плазмаферезе длится примерно час-полтора, при высокообъемном 2–2,5 часа.
Практически сразу после процедуры мы заметили улучшение состояния пациента: температура снизилась, а к вечеру того же дня нормализовалась. Сатурация повысилась, сам пациент отметил, что стало легче дышать, он даже смог самостоятельно поесть (для этого ненадолго был выведен из прон-позиции). На следующий день был проведен второй сеанс плазмафереза, а через два дня — третий сеанс. Состояние пациента значительно улучшилось, он был переведен из ОРИТ в перепрофилированное отделение.
Со вторым пациентом действовали по такой же схеме?
У второго пациента отмечалась нестабильная гемодинамика, поэтому мы немного снизили скорость трансфузии. Как правило, при лечебном автоматическом плазмаферезе замещение поводится препаратами крови или кровезаменителями. Однако, учитывая волемический эффект свежезамороженной плазмы, мы понимали, что можем перегрузить левые отделы сердца. Поэтому замещение провели не плазмой, а физраствором. А чтобы восполнить белок, в конце сеанса добавили 10%-ный раствор альбумина. Этому пациенту потребовались только два сеанса плазмафереза для значительного улучшения состояния.
Оба пациента уже выписаны домой.
Можно ли, на ваш взгляд, рассматривать автоматический лечебный плазмаферез как альтернативу ИВЛ? Эта дилемма широко обсуждается медицинской общественностью: с одной стороны, ИВЛ применяется как последний шанс для тяжелых пациентов, а с другой — несет большие риски летальности или тяжелой инвалидности…
В данных двух клинических случаях плазмаферез стал альтернативой ИВЛ. Но это только два случая. К счастью, таких тяжелых пациентов в нашем центре больше не было, поэтому глобальные выводы делать рано. Наш опыт показал, что плазмаферез эффективен на определенной стадии болезни — при переходе пневмонии к ОРДС. Этот момент непросто уловить, как правило, он сопровождается очень высокой температурой, которая не сбивается ни физическими, ни химическими методами, а также резким затруднением дыхания, снижением сатурации. Если же развился ОРДС, то возникают серьезные нарушения гемодинамики. Но именно в шаге от ИВЛ, когда пациент уже не может дышать самостоятельно, плазмаферез следует рассмотреть как шанс избежать перевода на ИВЛ.
Справка
Дмитрий Третьяк в 2005 году окончил БГМУ, получил специальность анестезиолога-реаниматолога. С 2009-го работает в ГВКМЦ Вооруженных Сил Республики Беларусь, с 2017-го возглавляет центр переливания крови. В 2014 году защитил кандидатскую диссертацию «Медико-биологические свойства и клиническая эффективность антилипополисахаридного гемосорбента при лечении сепсиса».