Традиционно понятие «хирургическое лечение онкологических заболеваний» ассоциируется с обширными оперативными вмешательствами, длительным восстановительным периодом и значительной травматизацией тканей. Однако развитие медицинских технологий предлагает альтернативный подход — малоинвазивную хирургию с минимизацией операционного доступа, снижением интра- и послеоперационных рисков и сокращением сроков реабилитации. Внедрение такого подхода в педиатрическую онкохирургическую практику открывает новые возможности в лечении злокачественных новообразований. В статье представлен опыт РНПЦ детской онкологии, гематологии и иммунологии.
От диагностических процедур к радикальным вмешательствам
 Сергей НазарукПервые малоинвазивные операции в детской онкологии в Республике Беларусь начали выполняться около двух десятилетий назад.
Сергей НазарукПервые малоинвазивные операции в детской онкологии в Республике Беларусь начали выполняться около двух десятилетий назад.
За период с 1999 по 2013 год в РНПЦ ДОГИ было проведено 134 подобных вмешательства, в основном с диагностической целью, таких как лапароскопия и операции на органах малого таза.
 Александра МитиловичЗначительное расширение арсенала малоинвазивных методов произошло в последнее десятилетие: с 2014 года по октябрь 2025 года выполнено 730 операций. Количественный рост отражает и качественную трансформацию — переход от преимущественно диагностических манипуляций к радикальному лечению.
Александра МитиловичЗначительное расширение арсенала малоинвазивных методов произошло в последнее десятилетие: с 2014 года по октябрь 2025 года выполнено 730 операций. Количественный рост отражает и качественную трансформацию — переход от преимущественно диагностических манипуляций к радикальному лечению.
Если на начальном этапе внедрения малоинвазивные технологии применялись главным образом для визуализации и биопсии, то в настоящее время спектр выполняемых вмешательств значительно расширился и соответствует мировым тенденциям: это такие сложные операции, как удаление опухолей надпочечников, почек, поджелудочной железы и печени, спленэктомии, резекции селезенки, а также вмешательства на органах плевральной полости. В рамках сотрудничества РНПЦ ДОГИ с МНПЦ хирургии, трансплантологии и гематологии в 2022 году впервые в стране были успешно выполнены лапароскопические гемигепатэктомии по поводу гепатобластомы у детей 2 и 3 лет.
Клинические преимущества малоинвазивного подхода
- Сниженная травматичность. Минимизация операционного доступа приводит к уменьшению интраоперационной кровопотери и выраженности болевого синдрома в послеоперационном периоде, снижению частоты осложнений.
- Сокращение сроков госпитализации. Более быстрое восстановление пациентов позволяет сократить длительность пребывания в стационаре, что имеет важное значение для психоэмоционального состояния ребенка и его семьи.
- Возможность ранней реабилитации и своевременного начала терапии. Отсутствие необходимости в длительном заживлении обширной операционной раны позволяет раньше начать химио- или лучевую терапию, не нарушая общих сроков лечения.
- Технические аспекты. Использование оптического увеличения обеспечивает детальную визуализацию анатомических структур и границ новообразования, способствуя точности манипуляций.
- Косметический эффект. Отсутствие обширных послеоперационных рубцов имеет существенное психологическое значение, способствуя более полной социальной реадаптации пациента.
Актуальные ограничения и проблемы внедрения
Несмотря на положительную динамику, применение малоинвазивной хирургии в детской онкологии сопряжено с рядом методологических и практических сложностей, требующих взвешенного подхода.
Ключевой проблемой остается отсутствие масштабных рандомизированных исследований, доказывающих равную онкологическую радикальность малоинвазивной хирургии по сравнению с открытыми вмешательствами в отдаленном периоде. Редкость и гетерогенность солидных опухолей у детей затрудняют накопление репрезентативных данных.
К основным ограничениям метода относятся:
- Риск нерадикальности резекции. Ограниченное пространство для манипуляций, особенно у пациентов младшего возраста, может повышать риск оставления микроскопических остатков опухоли (R1-резекция).
- Трудности интраоперационного стадирования. Оценка состояния регионарных лимфатических узлов при малоинвазивной хирургии может быть менее точной.
- Высокие требования к квалификации хирургической бригады. Оператор должен в совершенстве владеть не только техникой малоинвазивной хирургии, но и иметь значительный опыт открытой онкохирургии для выполнения конверсии при необходимости.
- Отсутствие тактильной обратной связи.
- Зависимость от специализированного дорогостоящего оборудования.
Выбор хирургического доступа всегда определяется приоритетом онкологического результата. Каждый клинический случай в РНПЦ ДОГИ подвергается мультидисциплинарному обсуждению. Если достижение радикальности требует открытой операции, этот метод будет применен.
Перспективы развития малоинвазивной хирургии в детской онкологии:
- Накопление и систематизация собственного клинического опыта с расширением показаний при условии строгого отбора пациентов.
- Проведение сравнительного анализа отдаленных результатов малоинвазивной хирургии и традиционных открытых операций.
- Развитие многоцентрового международного сотрудничества для проведения крупных исследований и формирования научно обоснованных клинических рекомендаций.
- Внедрение и освоение роботической хирургии (робот-ассистированных хирургических систем). Эта технология потенциально способна преодолеть некоторые ограничения традиционной лапароскопии, такие как недостаточная свобода движений инструментов и отсутствие тактильной чувствительности, за счет обеспечения трехмерной визуализации, повышенной точности манипуляций.
Случаи из практики
Пациентка, 12 лет, поступила в РНПЦ ДОГИ с жалобами на желтушность кожных покровов и склер. Из анамнеза известно, что с рождения наблюдается с диагнозом «наследственный микросфероцитоз (болезнь Минковского — Шоффара)», состоит на учете у гематолога. Получала консервативную терапию (фолиевая кислота), в возрасте 6 месяцев однократно — трансфузия отмытых эритроцитов. Проведена вакцинация против пневмококковой инфекции.
При поступлении общее состояние удовлетворительное. В объективном статусе отмечалась иктеричность кожи, пальпировалась селезенка +3–4 см из-под реберной дуги. По данным лабораторных исследований: анемия (Hb 102 г/л), гипербилирубинемия за счет непрямой фракции (общий билирубин 141,9 мкмоль/л, прямой — 7,74 мкмоль/л). УЗИ органов брюшной полости подтвердило спленомегалию (+5 см) и гепатомегалию (+1 см). В просвете желчного пузыря визуализировались множественные конкременты, просвет не прослеживался, что потребовало дифференциальной диагностики между отключенным и сокращенным желчным пузырем.
Пациентке выполнено симультанное оперативное вмешательство: лапароскопическая спленэктомия и лапароскопическая холецистэктомия под эндотрахеальным наркозом. Интраоперационных осложнений не было.
Послеоперационный период протекал гладко. При контрольном УЗИ (послеоперационном) отмечено уменьшение размеров печени, отсутствие свободной жидкости в брюшной полости. Жалоб пациентка не предъявляла. Выписана в удовлетворительном состоянии.
Представленный клинический случай демонстрирует эффективность и безопасность одномоментного выполнения лапароскопической спленэктомии и холецистэктомии у педиатрического пациента с наследственным сфероцитозом, осложненным желчнокаменной болезнью.
Малоинвазивный подход позволил радикально решить две клинические проблемы (устранить орган патологического гемолиза и источник потенциальных билиарных осложнений) в рамках одной анестезии и одного госпитального этапа. Это способствовало значительному снижению физиологической и психологической травмы для ребенка, обеспечило быстрое восстановление и хороший косметический эффект.
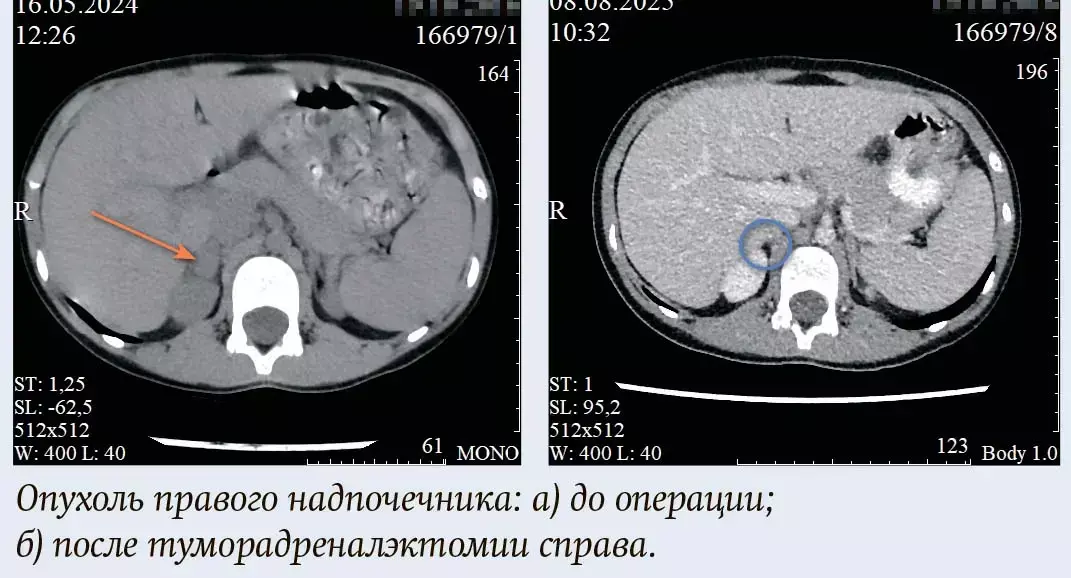
Пациентка, 8 лет, направлена в стационар РНПЦ ДОГИ для планового хирургического лечения. Из анамнеза: в 2022 году при плановом УЗИ органов брюшной полости случайно выявлено образование правого надпочечника диаметром около 1,5 см. В динамическом наблюдении в апреле 2024 года в анализах крови отмечено транзиторное повышение уровня кортизола и пролактина, что потребовало дообследования. Пациентка была консультирована эндокринологом и онкологом. Последующие гормональные исследования (май 2025) патологии не выявили. По данным инструментальной диагностики (КТ, МРТ) подтверждено наличие четко контурированного объемного образования правого надпочечника 16×15×11 мм. По результатам МРТ данные за аденому с низким содержанием жира. Принято решение о необходимости хирургической резекции образования.
Пациентке выполнена операция: диагностическая лапароскопия, туморадреналэктомия справа. Интраоперационных осложнений не было. Послеоперационный период протекал гладко. Состояние пациентки стабилизировалось в течение первых суток. Контрольное УЗИ органов брюшной полости на 6-е сутки после операции: свободной жидкости не выявлено. Заключительный гистологический диагноз: созревающая ганглионеврома. Пациентка была выписана в удовлетворительном состоянии на 6-е послеоперационные сутки.
Клиническое наблюдение иллюстрирует успешное применение лапароскопической техники для радикального удаления объемного образования надпочечника у ребенка.
Случай демонстрирует несколько важных аспектов современной детской хирургии:
- диагностическая ценность лапароскопии: метод позволил произвести прямую визуальную оценку образования, его отношения к ткани надпочечника и окружающим структурам;
- техническая осуществимость и безопасность: лапароскопический доступ обеспечил отличную визуализацию в труднодоступной анатомической области, позволив безопасно выделить и лигировать короткие и хрупкие сосуды надпочечника;
- преимущества миниинвазивного подхода: несмотря на сложность вмешательства, послеоперационный период протекал без осложнений, с минимальным болевым синдромом и коротким сроком госпитализации.
Пациент, 14 лет, экстренно госпитализирован в РНПЦ ДОГИ в тяжелом состоянии после гипертонического криза (АД 240/160 мм рт. ст.), осложненного фокальным судорожным приступом и потерей сознания.
При поступлении сохранялась злокачественная артериальная гипертензия (188/124 мм рт. ст.). КТ и МРТ брюшной полости с контрастированием выявили двусторонние объемные образования надпочечников: справа — солидно-кистозный узел 36×43×55 мм, слева — не менее двух образований до 17 мм. Лабораторно подтвержден гиперкатехоламиновый синдром.
Диагноз: феохромоцитома обоих надпочечников; киста головки поджелудочной железы; вторичная симптоматическая артериальная гипертензия.
В условиях отделения реанимации проведена 14-дневная терапия альфа-адреноблокаторами для стабилизации гемодинамики и профилактики интраоперационного катехоламинового криза. На консилиуме принято решение о необходимости двусторонней адреналэктомии с последующей пожизненной заместительной гормональной терапией.
Выполнена лапароскопическая двусторонняя туморадреналэктомия.
Операция проведена в два этапа:
1) удаление правого надпочечника (в положении на левом боку);
2) удаление левого надпочечника (в положении на правом боку).
Ранний послеоперационный период характеризовался лабильностью гемодинамики с эпизодами артериальной гипертензии, потребовавшей титрования урапидила в условиях отделения интенсивной терапии. Состояние стабилизировалось к 3-м суткам. Послеоперационный период протекал без инфекционных и тромбоэмболических осложнений. Пациент выписан на 15-е сутки в удовлетворительном состоянии.
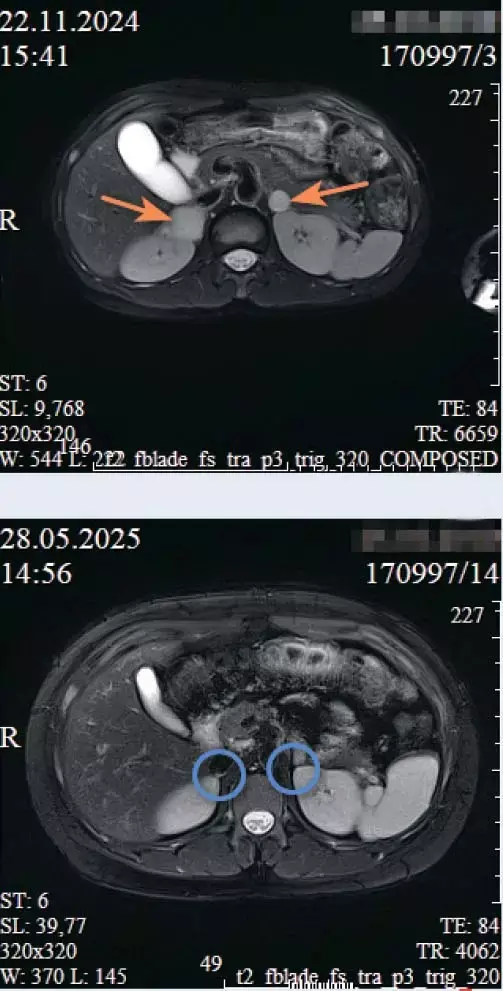 Двусторонняя феохромоцитома: а) до операции; б) после лапароскопической двусторонней туморадреналэктомии.Контрольные УЗИ и МРТ подтвердили отсутствие объемных образований в ложе надпочечников, что свидетельствовало о радикальности операции. Выявленные неспецифические диффузные изменения паренхимы печени и поджелудочной железы трактовались как следствие перенесенной катехоламиновой интоксикации. Киста головки поджелудочной железы оставалась без динамики, что исключило ее опухолевую природу.
Двусторонняя феохромоцитома: а) до операции; б) после лапароскопической двусторонней туморадреналэктомии.Контрольные УЗИ и МРТ подтвердили отсутствие объемных образований в ложе надпочечников, что свидетельствовало о радикальности операции. Выявленные неспецифические диффузные изменения паренхимы печени и поджелудочной железы трактовались как следствие перенесенной катехоламиновой интоксикации. Киста головки поджелудочной железы оставалась без динамики, что исключило ее опухолевую природу.
Представленный случай демонстрирует, что лапароскопическая двусторонняя адреналэктомия является высокоэффективным и безопасным методом лечения сложных форм феохромоцитомы у подростков.
Несмотря на крупные размеры опухоли, интимное прилежание к магистральным сосудам и высокий анестезиологический риск, малоинвазивный подход позволил:
1) выполнить радикальное одномоментное вмешательство через минидоступы;
2) обеспечить прецизионную диссекцию в критической зоне у нижней полой вены благодаря оптическому увеличению и современным энергетическим установкам;
3) минимизировать послеоперационную травму, способствуя быстрой реабилитации.
Успех операции был обеспечен мультидисциплинарным подходом, включающим адекватную предоперационную подготовку, тщательное интраоперационное гемодинамическое управление и точную хирургическую технику.
Опыт РНПЦ детской онкологии, гематологии и иммунологии демонстрирует, что малоинвазивная хирургия является высокоэффективным и перспективным инструментом в арсенале детского онколога. При условии выполнения опытной мультидисциплинарной командой с соблюдением фундаментальных онкологических принципов, малоинвазивная хирургия позволяет достигать радикального лечения с минимизацией физической и психологической травмы для пациента.
Основная цель — не только удаление опухоли, но и обеспечение ребенку возможности вернуться к полноценной жизни — становится более достижимой.

