Частота развития ишемического инсульта (ИИ) у пациентов молодого возраста (18–45 лет), по различным данным, составляет 5–14 % всех случаев заболевания. Актуальность и сложность проблемы помимо всего прочего обусловлены изменением структуры причин патологии по сравнению с другими возрастными категориями. В частности, неатеросклеротическая васкулопатия (НАВ) имеет особенно важное значение у детей и молодых людей и составляет 14–25 % случаев инсультов в возрасте до 50 лет. НАВ представляет большую разновидность заболеваний с различными патогенетическими механизмами, включая иммунологические, инфекционные, патологию соединительной ткани и гематологические состояния.
Механизм развития диссекции
 Светлана КузьменкоАртериальная диссекция (расслоение), как травматическая, так и спонтанная, является самой распространенной НАВ и причиной инфаркта головного мозга в молодом возрасте. Диссекция зачастую взаимосвязана с другими артериопатиями, включая фибромускулярную дисплазию и коллагенные васкулярные расстройства. Установлена также роль других НАВ, в том числе синдрома обратимого церебрального спазма сосудов (вазиконстрикция), односторонней интракраниальной артериопатии детей, болезни моямоя, пострадиационных васкулопатий и церебральных васкулитов.
Светлана КузьменкоАртериальная диссекция (расслоение), как травматическая, так и спонтанная, является самой распространенной НАВ и причиной инфаркта головного мозга в молодом возрасте. Диссекция зачастую взаимосвязана с другими артериопатиями, включая фибромускулярную дисплазию и коллагенные васкулярные расстройства. Установлена также роль других НАВ, в том числе синдрома обратимого церебрального спазма сосудов (вазиконстрикция), односторонней интракраниальной артериопатии детей, болезни моямоя, пострадиационных васкулопатий и церебральных васкулитов.
Механизмы инсульта при НАВ варьируют от сосудистых, воспалительных и инфекционных до травматических, зачастую при установлении основополагающей генетической предрасположенности.
Диссекция брахиоцефальных артерий (БЦА) является одной из самых частых причин ишемических инсультов и 15–20 % случаев церебральных инфарктов у пациентов молодого возраста. При этом диссекция внутренней сонной артерии (ВСА) почти всегда вовлекает мобильный участок артерии, не прикрепленный к костным структурам, часто включает в себя экстракраниальный фарингеальный и дистальный сегменты внутренней сонной артерии, нередко продлеваясь до своего каменистого супраклиноидного сегмента.
Экстракраниальный отдел позвоночной артерии (ПА) фиксирован в месте ее отхождения от подключичной артерии, в канале поперечных отростков позвонков и в месте проникновения в череп через твердую мозговую оболочку. Короткие мобильные сегменты артерий, расположенные между ее фиксированными участками, наиболее подвержены растяжению при поворотах головы и предрасположены к разрыву интимы. Самым частым местом локализации диссекции ПА является дистальный отдел ее экстракраниального участка (сегмент V3), который относительно мобилен и уязвим для разрыва при внезапном повороте головы, приводящем к натяжению и надрыву подслизистого слоя.
Затем следует образование интрамуральной гематомы (ИМГ) внутри медиального слоя. Продольное растяжение гематомы впоследствии приводит к сужению и уменьшению просвета сосуда, локальному стенозу или окклюзии пораженной артерии. По длине артерии ИМГ может распространяться на различное расстояние и вовлекать как экстракраниальные, так и интракраниальные отделы мозговых артерий. Когда интрамуральная гематома удлиняется между медиальным и адвентициальным слоями, может образоваться псевдоаневризма, или ложный просвет. При интракраниальной локализации расслаивающая аневризма может явиться причиной субарахноидального кровоизлияния.
Поражение внутренней сонной артерии наблюдается чаще, чем позвоночной, вместе с тем в последнее десятилетие отмечается примерно одинаковая частота. В современных исследованиях все чаще указывается на увеличение частоты диссекции позвоночной артерии (до 60–70 %) по сравнению с ВСА, что связано с широким использованием специальных режимов МРТ, направленных на выявление интрамуральной гематомы.
Нередко диссекция БЦА развивается в нескольких артериях, а диссекции внутренней сонной артерии и позвоночной могут сочетаться.
Этиопатогенез диссекции брахиоцефальных артерий остается пока малоизученным. Основной причиной спонтанной диссекции является слабость соединительной ткани артериальной стенки, что снижает ее эластические свойства. Пациенты с наследственным нарушением соединительной ткани и лежащей в основе артериопатии, такой как фиброзно-мышечная дисплазия, синдром Элерса — Данло 4-го типа (сосудистый вариант) и синдрома Марфана, особенно подвержены артериальным диссекциям.
Клинический случай
В нашей практике зафиксирован случай множественной диссекции (обеих ВСА и правой ПА), которая развилась одномоментно у молодого человека после падения.
Пациент Л., 28 лет, работающий IT-сфере, поступил в неврологическое отделение для больных с ОНМК с жалобами на головокружение, шаткую походку, онемение в руках и ногах, приступы кратковременного нарушения речи, памяти. Накануне во время прогулки поскользнулся, упал и ударил левым плечом шею, сознание не терял, после чего почувствовал онемение языка, кратковременное головокружение, тошноту, была рвота, нарушилась речь. Симптомы регрессировали через 10–15 минут. За медицинской помощью сразу не обращался. Через день симптомы повторились, пациент самостоятельно обратился в приемное отделение, госпитализирован по экстренным показаниям. В анамнезе: артериальная гипертензия, редкие простудные заболевания.
МРТ головного мозга:
- патологических изменений, нарушений мозгового кровообращения не выявлено. На серии МР-ангиограмм, выполненных с болюсным введением контрастного препарата, визуализируются брахиоцефальные артерии и их экстра- и интракраниальные ветви. Визуализируется сужение правой внутренней сонной артерии в экстракраниальном отделе при переходе в интракраниальный на 45 %. Также отмечается локальное выпячивание в этой зоне передней стенки правой ВСА размером до 1,7×2,5 мм с дном, направленным кпереди. Аневризма? Отсутствует контраст
- в экстракраниальном отделе левой внутренней сонной артерии при переходе в интракраниальный на протяжении 14 мм. Отсутствует контраст на протяжении 29 мм, а также имеется двойной контур и сужение просвета правой позвоночной артерии в сегменте V3. Отмечается задняя трифуркация левой ВСА — вариант развития интракраниальных артерий.
Заключение: МР-данных за патологический объемный процесс головного мозга, острое нарушение мозгового кровообращения на момент исследования не выявлено; МР-признаки аневризмы экстракраниального отдела ВСА (дифференцировать с атеросклеротическими изменениями); МР-признаки гемодинамически значимого стеноза экстракраниального отдела левой ВСА; МР-признаки диссекции правой позвоночной артерии. Пациенту назначены низкомолекулярные гепарины, антиоксидантная, нейропротекторная, гипотензивная терапия.
В стационаре состояние оставалось стабильным на протяжении 5 суток, затем повторно нарушилась речь, развился правосторонний гемипарез. В первый час проведен внутривенный системный тромболизис альтеплазой в дозе 0,9 мг/кг. Выполнено контрольное МРТ головного мозга, на которой визуализируется очаг пониженной плотности в области базальных ядер и внутренней капсулы слева.
Диагноз: ЦВБ: инфаркт головного мозга в бассейне левой средней мозговой артерии, повторные транзиторные ишемические атаки в бассейне левой средней мозговой артерии, обусловленные множественной посттравматической диссекцией БЦА — обеих ВСА в экстракраниальном отделе с переходом на интракраниальный отдел левой внутренней сонной артерии и правой позвоночной в сегменте V3. Пациент продолжил лечение в прежнем объеме: низкомолекулярные гепарины в лечебной дозе + ацетилсалициловая кислота под контролем коагулограммы, нейроцитопротекторы, гипотензивная терапия, клинико-лабораторный мониторинг, динамическое наблюдение, занятия с логопедом, инструктором ЛФК. Пациенту выполнена церебральная ангиография.
Заключение: протяженная диссекция интракраниального отдела обеих ВСА и сегментов V3, V4 правой позвоночной артерии. Имеется анастомоз между НСА и ВСА через офтальмические ветви.
УЗИ сердца, БЦА, артерий верхних и нижних конечностей: патологии не выявлено. Лабораторные исследования не выявили коагулопатий, нарушений углеводного и липидного обмена. Для дальнейшего лечения переведен в МОЦМР «Загорье».
Рассмотренный клинический пример — уникальный случай. Нет литературных данных о множественной диссекции одновременно трех артерий — обеих внутренних сонных артерий и правой позвоночной.
Что может спровоцировать расслоение?
Повысить риск диссекции могут наследственные, экзогенные и эндогенные, инфекционные факторы. Травма головы и шеи в качестве провоцирующего фактора отмечается чаще при поражении ВСА (26 %), чем ПА (3 %). Повреждение может возникнуть при различных обстоятельствах — удар, падение, удушение. Чрезмерный форсированный поворот головы с натяжением экстракраниальных артерий приводит к надрыву интимы и проникновению крови в артериальную стенку. Диссоциация между относительной легкостью травмы и серьезными последствиями свидетельствует о слабости артериальной стенки, а травма выступает в роли триггера.
Провоцирующими факторами диссекции наряду с травмой могут быть также запрокидывание головы и ее неудобное положение (синдром «салона красоты»), занятия некоторыми видами спорта (плавание), долгий разговор по мобильному телефону, когда аппарат удерживается плечом, интубационный наркоз, мануальная терапия, интенсивные усилия во время родов, неудобное положении головы во время сна.
Это также приводит к натяжению стенки артерий и ее травматизации о расположенные рядом костные структуры, вследствие чего образуется надрыв интимы. Описаны случаи диссекции при физическом напряжении во время кашля, рвоты, поднятия тяжести. Вместе с тем следует понимать, что эти факторы приводят к повреждению сосудистой стенки только при слабости или «неполноценности» коллагена (чаще всего генетической), разрыв интимы здоровых артерий встречается крайне редко.
Роль инфекционных факторов
Частота спонтанных диссекций увеличивается в осенне-зимний период, так как возрастает риск вирусных заболеваний. Ишемические инсульты при диссекции БЦА, обусловленные инфекционными факторами, возникают почти в 30 % случаев. Это значительно чаще, чем при инсультах другого генеза (13,5 %). При этом в патологический процесс вовлекается несколько артерий, что предполагает наличие у пациента более тяжелой артериопатии.
Подтверждением роли инфекции является повышение уровня цитокинов, свободных радикалов и протеиназ, которые ослабляют сосудистую стенку. Это в сочетании с характерными для вирусных инфекций кашлем и чиханием приводит к повреждению артерий. Другим подтверждением влияния воспалительных изменений в сосудистой стенке при диссекции является выявление при МРТ-исследовании периартериального отека, который коррелирует с лабораторными изменениями. Однако некоторые инфекции могут быть непосредственной причиной спонтанной диссекции брахиоцефальных артерий у молодых пациентов: перенесенная ветряная оспа, которая сопровождается персистированием вируса в нервных ганглиях, при сифилисе, ВИЧ-инфекции. Развитие диссекции в этих случаях обусловлено специфическим артериитом.
К другим состояниям, связанным с повышенным риском диссекции БЦА, относятся мигрень, артериальная гипертензия, мутации гена MTHFR, гомоцистеинурия (редкое наследственное нарушение обмена серосодержащих аминокислот), болезнь Такаясу, врожденное сужение главной артерии (аорты), атеросклероз, артериальная гипертензия, курение, прием оральных контрацептивов, менинговаскулярный сифилис.
Тонкости диагностики
Диагностика диссекции БЦА может представлять значительные трудности. Даже при осведомленности неврологов патология выявляется в небольшом количестве случаев — 6–10 %
Заболевание зачастую является асимптомной и случайной находкой на МРТ или КТ. Характерным клиническим проявлением диссекции БЦА выступают ипсилатеральные головные или шейные боли с ретроорбитальными и ретроаурикулярными болями, нарушение мозгового кровообращения (инфаркт головного мозга, транзиторные ишемические атаки), описанные у пациентов с диссекцией внутренней сонной и позвоночной артерий.
Головную боль или боль в шее отмечают большинство пациентов — 80 %. При этом она является первым клиническим признаком и предшествует очаговым симптомам. Интенсивность боли варьирует и бывает не похожа на боли, которые пациенты испытывали ранее. Нередко она настолько легкая и кратковременная, что пациенты не придают ей значения и вспоминают только после уточняющих вопросов.
Другие неврологические симптомы, возникающие из-за прямой компрессии диссекционной аневризмой или стеноза/окклюзии артерии:
- синдром Горнера;
- параличи черепных нервов;
- пульсирующий шум в ушах (тиннитус);
- извращение вкуса и зрительные нарушения (окклюзия центральной артерии сетчатки, ишемическая невропатия зрительного нерва).
Нарушения мозгового кровообращения являются наиболее частым и серьезным проявлением диссекции БЦА. Среди пациентов они наблюдались в 90 % случаев и были представлены инфарктами головного мозга.
Важные критерии
Диагностика инфаркта головного мозга, обусловленного диссекцией БЦА, должна базироваться на следующих показателях:
- молодой возраст пациента;
- отсутствие типичных факторов риска инсульта;
- отсутствие атеросклеротического поражения сосудов головного мозга;
- отсутствие клинических и лабораторных признаков гиперкоагуляции;
- наличие характерных провоцирующих моментов (травма головы и шеи, форсированные движения и мануальные воздействия на шейном отделе позвоночника);
- наличие головной, лицевой или шейной боли на стороне поражения.
Когда есть подозрения на диссекцию БЦА, рекомендуются неинвазивные исследования головы и шеи, такие как дуплексное сканирование с допплеровским картированием, МРТ и магнитно-резонансная ангиография, мультиспиральная компьютерная томографическая ангиография (МСКТА), которые облегчают раннюю диагностику и способствуют назначению адекватной терапии.
Ангиографическими признаками диссекции БЦА являются:
- симптом струны — равномерное продолженное сужение просвета сосуда, обусловленное наличием в стенке интрамуральной гематомы, или неравномерное сужение просвета артерии по типу нитки бус или четок;
- конусообразное предокклюзионное сужение артерии на 2–3 см выше ее устья — симптом «пламени свечи» (рис. 1, 2);
- наличие ложного просвета, образованного проникшей через разрыв интимы кровью;
- образование расслаивающей аневризмы.
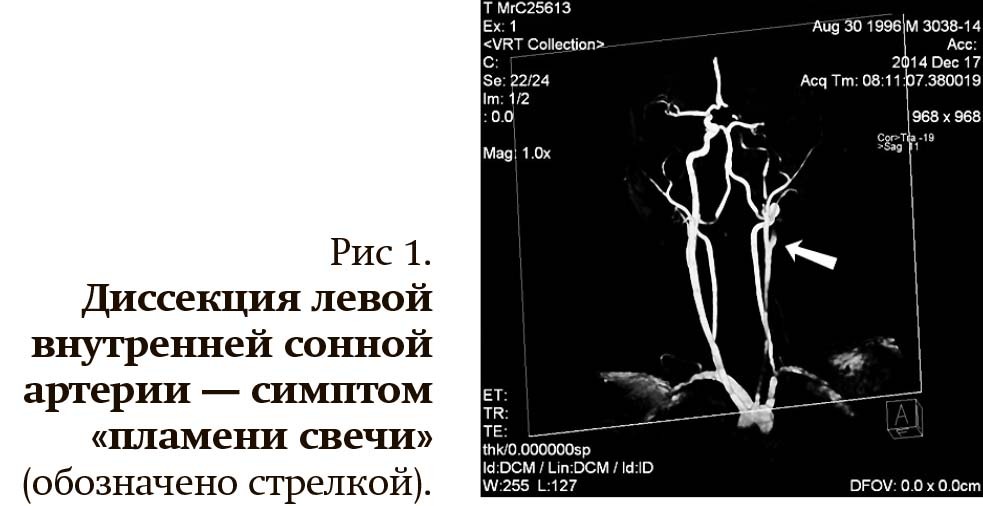 Однако церебральная ангиография не выявляет такой важный диагностический симптом диссекции, как увеличение наружного диаметра внутренней сонной артерии, обусловленный интрамуральной гематомой в ее стенке, а также является инвазивным и дорогостоящим методом, что ограничивает возможность повторного обследования в динамике. Тем не менее данное исследование сохраняет свою актуальность тогда, когда данные КТ или МРТ были не совсем убедительными.
Однако церебральная ангиография не выявляет такой важный диагностический симптом диссекции, как увеличение наружного диаметра внутренней сонной артерии, обусловленный интрамуральной гематомой в ее стенке, а также является инвазивным и дорогостоящим методом, что ограничивает возможность повторного обследования в динамике. Тем не менее данное исследование сохраняет свою актуальность тогда, когда данные КТ или МРТ были не совсем убедительными.
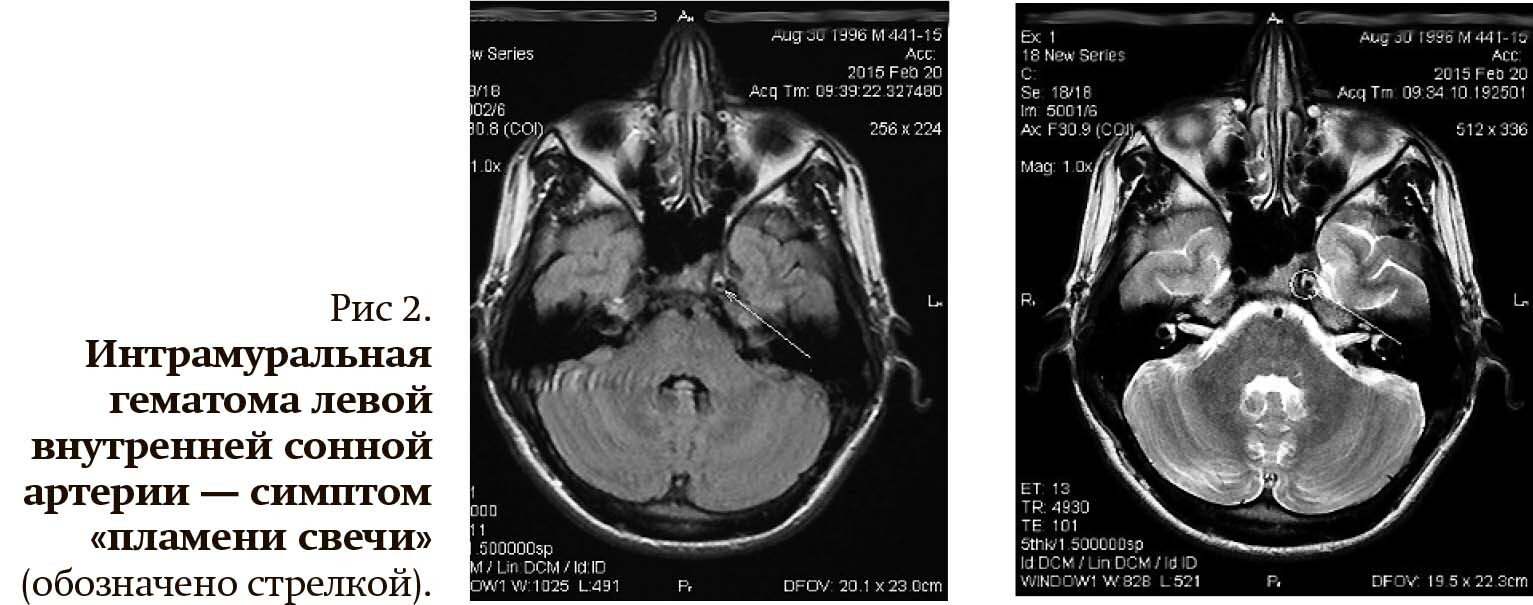 МСКТА позволяет обеспечить высококачественное и высококонтрастное изображение артериального просвета и сосудистой стенки с высокой чувствительностью (90–100 %) и специфичностью.
МСКТА позволяет обеспечить высококачественное и высококонтрастное изображение артериального просвета и сосудистой стенки с высокой чувствительностью (90–100 %) и специфичностью.
Ограничения по проведению этого исследования связаны с предварительной оценкой выделительной функции почек в связи с риском развития нефропатии на введение контраста.
Симптомы диссекции, выявляемые при МС КТА, аналогичны ангиографическим признакам: равномерное или неравномерное сужение артериальной стенки, симптом «пламени свечи», наличие расслаивающей аневризмы. Кроме того, данное исследование выявляет увеличение наружного диаметра внутренней сонной артерии, обусловленное интрамуральной гематомой в ее стенке.
Бесконтрастная КТ головного мозга в остром периоде диссекции внутренней сонной артерии может обнаружить интрамуральную гематому в прекраниальном отделе в виде участка повышенной плотности полулунной формы. Иногда КТ-ангиографии удается визуализировать отслоенную интиму, выступающую в просвет артерии, и двойной просвет, образованный кровью в стенке сосуда. Находки могут включать в себя псевдоаневризматическое образование, движение внутренней стенки сосуда с двойным светом, стеноз сосуда или полную закупорку артерии.
Магнитно-резонансная томография по сосудистой программе выявляет большинство патогномоничных для диссекции признаков: симптом «пламени свечи», неравномерное сужение артерии (симптом четок), аневризмы, однако чувствительность этой техники в диагностике диссекции ниже, чем КТА. Большое диагностическое значение имеет МРТ с подавлением жира в режиме Т1, которое позволяет выявить наличие интрамуральной гематомы внутри стенки сосуда.
Ультразвуковая диагностика занимает важную роль в диагностике диссекций и последующего мониторирования проходимости артерий, так как диссекция представляет собой динамический процесс. Ее характерными УЗ-признаками является гипоэхогенная гематома внутри стенки артерии, наличие ложного просвета, псевдоаневризмы, гиперэхогенной отслоенной интимы, пролонгированное сужение просвета артерии.
Особенности терапии
До настоящего времени имеются противоречивые клинические данные по сравнительной оценке различных вариантов лечения и профилактики инфаркта головного мозга, обусловленного диссекцией БЦА. Терапия обычно направлена на предотвращение пролонгирования интрамуральной гематомы, образования тромбов и развития артериальной эмболии.
Лечение включает в себя внутривенный или внутриартериальный тромболизис у пациентов, подходящих для назначения альтеплазы. Оптимальные стратегии для предотвращения повторной диссекции БЦА остаются противоречивыми. Эти варианты включают в себя антитромбоцитарную либо антикоагулянтную терапию.
Лечение артериальной диссекции должно быть индивидуально, в зависимости от остроты симптомов, клинических проявлений, повторных эпизодов, а также данных нейровизуализации. Антитромбоцитарные препараты часто выписываются пациентам с асимптомным стенозом, в подострых или поздних случаях. В сравнительных клинических испытаниях наличие тромба в диссектной артерии делает использование антикоагулянтов более предпочтительным. Хирургические и эндоваскулярные вмешательства с сосудистой пластикой и стентированием показаны пациентам с повторными инфарктами, медикаментозная терапия которых была неэффективной. Большинство диссекций БЦА излечивается спонтанно, прогноз и конечный исход обычно благоприятный. Повторная диссекция в компрометированном сосуде очень редка и проявляется в течение первых 2-х месяцев после первоначального случая.
Практические рекомендации
1. У пациентов молодого возраста по сравнению с группой контроля достоверно чаще выявлялись следующие факторы риска:
- васкулопатии: системные васкулиты, антифосфолипидный синдром, диссекции церебральных артерий (18,7 % и 6 % соответственно);
- врожденные и приобретенные нарушения свертываемости крови: гипергомоцистеинемии, тромбофилии (20,4 % и 1 % соответственно);
- артериальная гипотония, сочетающаяся с венозной церебральной дисциркуляцией (26,2 %);
- врожденная патология сердца и церебральных сосудов (13,6 % и 5 % соответственно).
У лиц молодого возраста развитие ишемического инсульта во всех случаях имело многофакторный характер.
2. Высокий процент выявления у лиц молодого возраста «редких подтипов» ишемического инсульта предполагает проведение в острейшем периоде инсульта тщательный сбор анамнеза и современный спектр диагностических мероприятий по выявлению кардиальной патологии, заболеваний свертывающих и реологических свойств крови, васкулопатий различной этиологии, генетической патологии.
3. При наличии генетической предрасположенности (синдром MELAS, CADASIL, лизосомальные болезни) необходимо проводить активную борьбу с модифицируемыми факторами риска ишемического инсульта. Лечение пациентов молодого возраста должно учитывать индивидуальные особенности этиопатогенеза в каждом отдельном случае.
4. Учитывая относительно благоприятный прогноз восстановления нарушенных функций и трудоспособности, всем пациентам молодого возраста должны проводиться интенсивные реабилитационные мероприятия начиная с первых дней ишемического инсульта. После выписки из стационара все больные молодого возраста, перенесшие инфаркт мозга, должны направляться в реабилитационные центры, что позволит улучшить функциональные исходы, снизить процент выхода на инвалидность.

