Частота тромбоэмболических осложнений у критически тяжелых больных с СOVID-19, госпитализированных в ОРИТ, согласно многим исследованиям, достигает 80–90 %, сообщает заведующий отделом сердечно-сосудистой патологии Всероссийского центра экстренной и радиационной медицины им А. М. Никифорова МЧС России (Санкт-Петербург), доктор мед. наук, профессор Владимир Хирманов.
В рамках Республиканского кардиологического форума с международным участием «РНПЦ «Кардиология» — 45 лет достижений» эксперт привел случаи из практики и поделился международными рекомендациями по лечению (презентация в соавторстве с директором центра Сергеем Алексаниным).
Случаи из практики
 Владимир Хирманов:
Владимир Хирманов:
Новая коронавирусная инфекция в начале пандемии воспринималась исключительно как острое респираторное тяжелое заболевание, что отражалось и в его названии. Но с течением времени стало понятно, что это системное заболевание, при котором поражаются многие органы и ткани.
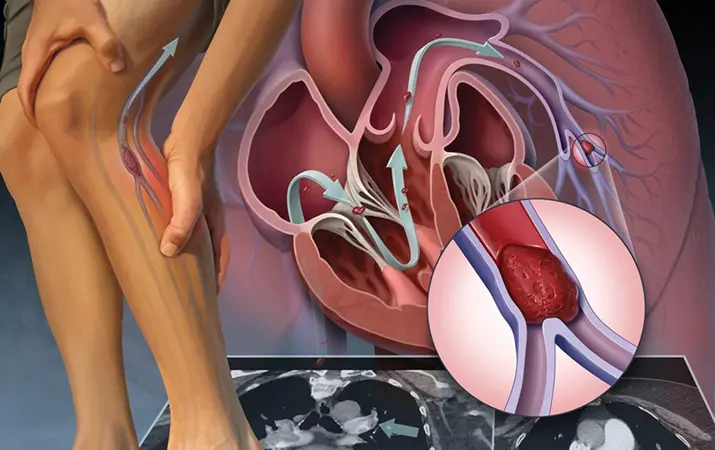
Одной из сторон этой системности является высокая склонность к развитию тромбоэмболических осложнений. В основном тромбоэмболические осложнения в сознании врачей ассоциируются с флеботромбозами в бассейне глубоких вен нижних конечностей и тромбоэмболией легочной артерии. Однако это не только так.
Поражаются крупные и мелкие артерии, микроваскулярные русла, вены самых разнообразных локализаций. И вот примеры…
Пациентка Р., 50 лет. Обратилась на амбулаторный прием в июне 2022 года в связи с астенической симптоматикой и лабильностью АД.
Исходно здорова, обладала высокой работоспособностью, занималась спортом (горные лыжи). Весной 2021 года получила прививку от СOVID-19, в конце октября заболела. В конце второй недели на фоне кажущегося выздоровления внезапно развились сильнейшие головные боли, гиперестезия в области покровов головы, тошнота, спастические нарушения, бессонница. Обследовалась невропатологами. Выполнено МРТ головного мозга спустя 2 недели от начала мозгового эксцесса (28 ноября).
Через 2–3 месяца головные боли уменьшились, но сформировалась лабильная гипергипотензия (с колебаниями давления пациентка связывает плохое самочувствие). Астения имеет стойкий и резко выраженный характер.
Результаты МРТ: признаки частичного тромбирования левых сигмовидного и поперечного синусов и луковицы яремной вены (подтверждается усилением МР-сигнала от синусов слева и ослабленным заполнением суженных левых синусов).
Относительно ситуации с тромбозом мозговых синусов, говорит Владимир Хирманов, данные статистики свидетельствуют о высокой частоте этого нарушения при инфицировании SARS-CoV-2.
Пациент П., 32 года. В прошлом здоров, занимался спортом. Без факторов риска сердечно-сосудистых заболеваний. В феврале 2020-го оба родителя, с которыми живет пациент П., почти одновременно заболели тяжелой «пневмонией». Через несколько дней лихорадка, катаральные явления и кашель появились у пациента П. К врачам не обращался, считал, что выздоровел через 2–3 недели.
В дальнейшем был переведен на дистанционную работу дома. На протяжении полугода прибавил в весе (исходно нормальном) на 13 кг. В июле вновь развились катаральные явления, кашель, субфебрильная лихорадка на протяжении 5 дней. При флюорографии (спустя 2–3 недели) дано заключение о хроническом бронхите. Длительное (более месяца) недомогание.
В середине октября появились боли за грудиной при ходьбе. 10 ноября случился 20-минутный приступ загрудинных болей, спровоцированный подъемом по лестнице. Вызвал скорую помощь. Снята ЭКГ: блокада правой ножки пучка Гиса. Высказано предположение о ДДЗП, не госпитализирован. В последующие 2 недели произошло явное снижение переносимости нагрузок из-за болей. А 1 декабря поступил в клинику.
3 декабря проведена коронарография, диагностирована окклюзия в проксимальном отделе передней нисходящей артерии. Выполнена пластика передней межжелудочковой ветви, восстановлен кровоток. Пациент получает стандартную терапию, бессимптомен.
Как поясняет Владимир Хирманов, в отдаленном анамнезе у пациента два эпизода, которые подозрительны в отношении коронавирусной инфекции, сам факт ее к моменту выявления коронарных изменений подтверждался высоким уровнем антител к вирусу SARS-CoV-2 (пациент не был привит).
Пациент С., 49 лет. Поступил в клинику 16 декабря 2020 года в связи с болями, ощущением холода и парестезией в стопах (больше справа). Симптомы развились в периоде реконвалесценции от СOVID-19 за неделю до поступления и быстро нарастали. Заболел остро 11 ноября: лихорадка с ознобом, слабость, в дальнейшем присоединились кашель и одышка. Безуспешно лечился дома.
Через 2 недели от начала заболевания госпитализирован в инфекционное отделение. ПЦР-тестирование подтвердило диагноз СOVID-19. Выявлено типичное двустороннее поражение легких (55 %). Лечение проводилось в соответствии с текущими протоколами, включало профилактические дозы НМГ.
Фоновое заболевание — хронический лимфолейкоз (выявлен в 2010-м), с 2016 года выполнено 4 курса противоопухолевой полихимиотерапии, достигнута длительная ремиссия, сохранявшаяся к моменту возникновения СOVID-19. Вплоть до этого времени пациент получал поддерживающую терапию противоопухолевым препаратом ибрутинибом.
17 декабря выполнена МСКТ-аортоангиография. 19–21 декабря проводились катетерные ангиографии и вмешательства. Выявлен двусторонний тромбоз (больше справа) нескольких артерий голени. Выполнен тромболизис. В дальнейшем потребовались дополнительная тромбоаспирация и пластика, которая в значительной мере анатомически привела к выздоровлению и устранению симптоматики.
Механизмы повреждений
Владимир Хирманов:
Тромбоэмболические осложнения в системном артериальном, венозном русле, микроваскулярные тромбозы можно считать осложнением COVID-19, потому что присоединение таких нарушений резко меняет течение заболевания и может стать непосредственной причиной смерти.
Но с моей точки зрения, в определенных случаях это является патогенетическим проявлением коронавирусной инфекции. Для того чтобы понять, в каких именно случаях и каким образом это происходит, нужно подробнее рассмотреть патогенез такого рода нарушений. Речь идет о воздушно-капельной инфекции. Инфекционный агент тропен к рецепторам АПФ-2, представленным в эпителии верхних дыхательных путей (в трахеях — значительно, в мелких бронхах — скорее нет, чем да).
Рецептор располагается также в альвеолярном аппарате, но лишь в альвеолоцитах 2-го типа, которые ответственны за выработку сурфактанта и регенерацию эпителия альвеол. Инфекционное повреждение альвеол при повторном вдыхании инфицированного воздуха, заражение альвеолярного аппарата означает, что, несомненно, в условиях микробиоза возникает повреждение базальной мембраны, которое моментально распространяется на эндотелий. Расстояние здесь — микроны. И вот это знаменует очень важный этап в течении болезни.
Развивается микроваскулярный тромбоз. То, что называется ковидной пневмонией, в действительности является сочетанием трахеобронхита с альвеолитом и микроваскулярным тромбозом в легких, который развивается при пневмонии в 100 % случаев. Это является самым частым тромботическим повреждением при COVID-19 в тех случаях, когда поражаются легкие, а они поражаются не всегда и не при всех штаммах коронавируса.
Далее речь идет главным образом о двух важных процессах. Если вирусы, реплицируемые в этом клеточном аппарате, оказываются в сосудистом русле, то возникает вирусемия, которая является подоплекой вирусного сепсиса. Но, с другой стороны, микроэмболы диссеминируют в сосудистом русле.
Где же приживаются вирусы, которые оказались в сосудистом русле? Важно то, что рецепторы АПФ-2 представлены в «родоначальных» клетках костного мозга, клетках-предшественницах тромбоцитов и эндотелиоцитов. Поврежденные клетки, а это совершенно точно показано не только в отношении тромбоцитов и эндотелия, но и других клеток крови, морфологически и функционально резко отличаются от тех, которые имеются у здорового человека.
Важно подчеркнуть, что мегакариоциты располагают дополнительными рецепторами к коронавирусу — CD147. Инфицированные мегакариоциты воспроизводят дефектные тромбоциты, и это потенцирует тромбозы. История с тромбоцитами и эндотелием приводит к патологическому состоянию, которое трактуется как LongCOVID.
Имеются данные ПЭТ/КТ, которые показывают, что у пациентов с LongCOVID locus minoris resistentiae обнаруживаются в костном мозге и в большом количестве — в сосудистом русле.
Взгляды на терапию
Владимир Хирманов:
В России разработаны методические рекомендации по профилактике, диагностике и лечению СOVID-19, которые подверглись уже 16-му пересмотру. В практическом руководстве пациенты логично разделены на амбулаторных и госпитализированных, в активной фазе заболевания и в период реконвалесценции, учитывается степень тяжести заболевания.
Алгоритмы большей частью составлены на основании мнений экспертов. 5 июля опубликованы рекомендации Международного общества специалистов по тромбозу и гемостазу (ISTH), несомненно, самого компетентного. Эти рекомендации основаны сугубо на доказательной базе.
Так, у негоспитализированных больных с симптомной формой СOVID-19 инициация терапии антиагрегантами/прямыми антикоагулянтами в плане снижения необходимости в госпитализации, риска артериальных и венозных тромбозов, а также вероятности смерти неэффективна. Но может рассматриваться использование сулодексида в пределах 3-х дней от начала болезни.
Касательно пользы аспирина при СOVID-19 Владимир Хирманов приводит следующие данные.
Владимир Хирманов:
С одной стороны, два открытых рандомизированных исследования (несколько сотен наблюдений, огромная вариабельность материала) не показали убедительных результатов в пользу эффективности аспирина при СOVID-19. С другой стороны, метаанализы, основанные на десятках тысяч наблюдательных исследований, свидетельствуют о явном преимуществе аспирина по сравнению с неиспользованием препарата в отношении снижения риска смерти, а также тромбозов.
Чему больше верить? Я бы сказал, что мудрость заключается в том, что антиагреганты в кардиодозах — это доступная терапия, вполне оправданная при наличии у пациента факторов риска, требующих назначения аспирина. Кроме того, нужно учитывать, что в 2 из 3 наблюдений представлены первичные тромбозы артериального русла. Это ситуация, когда аспирин является хорошо доказанным средством профилактики.
Также Владимир Хирманов обращается к вопросу применения низкомолекулярного гепарина (НМГ) в амбулаторных условиях.
Владимир Хирманов:
На недавнем Европейском конгрессе кардиологов были представлены 2 открытых рандомизированных многоцентровых исследования первичной профилактики тромбозов НМГ у амбулаторных пациентов — OVID и ETHIC. Оба показали неэффективность этого лечения в предотвращении смертей.
В открытом рандомизированном проспективном исследовании ROXANE сравнивались ривароксабан в дозе 10 мг (в некоторых случаях 15 мг) и эноксапарин в профилактической дозе в среднем на протяжении 8 дней (у госпитализированных с СOVID-19 легкого или среднетяжелого течения, n=230).
Ривароксабан способствовал снижению риска тромботических событий на 80 % по сравнению с эноксапарином, клинически значимые кровотечения наблюдались значительно реже при использовании ривароксабана.
Каковы рекомендации ISTH по антитромботической терапии у критически тяжелых госпитализированных пациентов с СOVID-19?
Владимир Хирманов:
Обращает внимание тенденция: чем тяжелее больной, тем больше осторожности требуется при назначении антикоагулянтов. Это связано с тем, что антикоагуляционная терапия не очень эффективна у этих пациентов, а риски кровотечений у них возрастают. Если следовать рекомендациям ISTH, то в основном нужно опираться на применение антикоагулянтов в виде НМГ в профилактических дозах, иногда в бόльших, чем профилактические.
Но исследование COVID-PACT, представленное на Европейском конгрессе кардиологов, показало, что применение НМГ у критически тяжелых пациентов в полной лечебной дозе обладает явно большей эффективностью, чем в стандартной, в плане предотвращения комбинации тромбозов вен или артерий, включая ТЭЛА, ИМ, инсульты на протяжении 28 дней или за время госпитализации.
С другой стороны, было подтверждено, что антиагреганты неэффективны. Но я хотел бы вернуться к обратной стороне антикоагуляции: риски кровотечений при использовании интенсивной антикоагуляционной терапии в сравнении со стандартной возрастают более чем в 10 раз, и это может нивелировать конечный эффект.
В рандомизированном анализе данных 1 098 пациентов из трех исследований показано, что исходы (выживаемость, длительность ИВЛ, сроки госпитализации) у критически тяжелых больных СOVID-19 не зависят от начальной стратегии антикоагуляции гепаринами — активной или осторожной.
Рекомендации ISTH по антитромботической терапии у больных СOVID-19, выписанных из стационара: у отдельных пациентов дальнейшее лечение может включать профилактические дозы ривароксабана на протяжении примерно 30 дней в расчете на снижение риска венозных тромбоэмболических осложнений.
Владимир Хирманов:
У этих пациентов риск тромботических осложнений все еще велик. Насчет терапии в данном случае немного информации. Но согласно регистру CORE-19 (данные наблюдения 4 906 пациентов с СOVID-19 в стационарах и после выписки на весну 2020-го), при использовании ривароксабана в небольшой дозировке после выписки из стационара (независимо от того, какая антикоагуляция использовалась) исходы были значительно лучше.
Открытое многоцентровое рандомизированное контролируемое исследование MICHELLE (320 больных СOVID-19 с повышенным риском тромбоэмболических осложнений, 2020–2021) показывает, что применение после выписки из стационара ривароксабана в дозе около 10 мг обеспечивает снижение риска тромбоэмболических осложнений на 67 %.
Представленные данные, обращает внимание Владимир Хирманов, относятся в основном к прежним штаммам СOVID-19.
Владимир Хирманов:
Что касается «омикрона», то складывается впечатление, что этот вариант вызывает гораздо реже повреждение легких, т. е. ситуацию, которая открывает шлюз для проникновения вирусов в организм, и значительно реже осложняется тромбозами и эмболиями.
К сожалению, коронавирус не исчезнет, но с течением времени наша терапия при этой инфекции будет более осмысленной, и в этом отношении мы одержим победу над новым заболеванием.