Токсоплазмоз является одним из наиболее распространенных протозойных заболеваний в мире: число инвазированных превышает 1,5 млрд человек.
Токсоплазмоз входит в состав группы TORCH-инфекций, представляющих опасность внутриутробного заражения плода, приводящего к его гибели, выкидышу, различной патологии у новорожденных. Ежегодно регистрируется свыше 200 тысяч случаев внутриутробного заражения.
 В настоящее время с учетом роста числа заболеваний, сопровождающихся выраженным нарушением статуса иммунной системы (онкогематологическая патология, коронавирусная инфекция, врожденные ошибки иммунитета), а также развитием высокотехнологичных вмешательств (трансплантология), проблема токсоплазмоза приобрела дополнительную актуальность.
В настоящее время с учетом роста числа заболеваний, сопровождающихся выраженным нарушением статуса иммунной системы (онкогематологическая патология, коронавирусная инфекция, врожденные ошибки иммунитета), а также развитием высокотехнологичных вмешательств (трансплантология), проблема токсоплазмоза приобрела дополнительную актуальность.
Циркуляция возбудителя
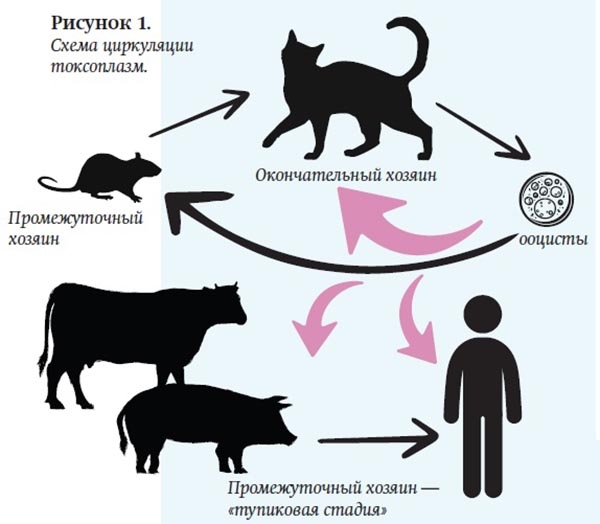
Возбудитель заболевания Toxoplasma gondii относится к простейшим внутриклеточным микроорганизмам. Согласно современной таксономической классификации, является представителем семейства Sarcocystidae рода Toxoplasma. Все виды восприимчивых к токсоплазме существ могут быть разделены на промежуточных и основных хозяев (см. рис. 1). В этой цепочке участвуют представители семейства кошачьих, грызуны, млекопитающие и человек.
Пути заражения человека (по механизму передачи патогена):
- алиментарный — при употреблении сырого либо недостаточно термически обработанного мяса и фарша, а также контаминированной токсоплазмами питьевой воды;
- контактно-бытовой — при энтеральном попадании в организм возбудителей токсоплазмоза в результате несоблюдения санитарно-гигиенических норм (например, контакт необработанными руками с ротовой полостью после тесного общения с кошками, уборки кошачьего туалета либо проведения сельскохозяйственных земляных работ);
- вертикальный — при заражении матери во время беременности и передаче возбудителя плоду;
- контактный (редко) — проникновение возбудителя через поврежденные кожные покровы у лиц, занимающихся переработкой мяса.
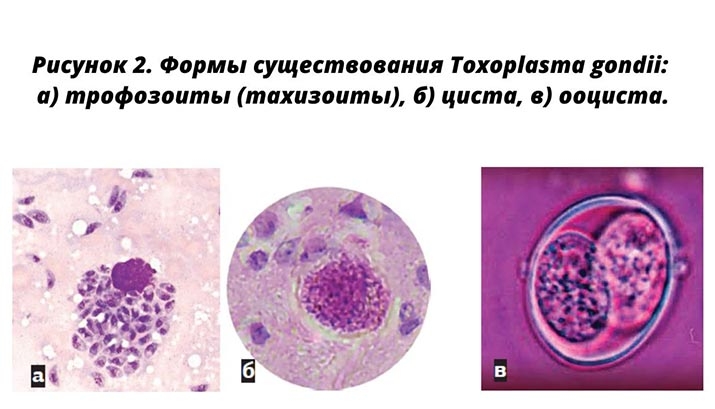
Toxoplasma gondii существуют в трех основных формах: трофозоит (тахизоит, эндозоит); циста (формирование брадизоитов); ооциста (формирование спорозоитов) (см. рис. 2).
Обнаружены два пути размножения: половой (заканчивающийся образованием ооцист со спорозоитами и протекающий в организме исключительно представителей семейства кошачьих) и бесполый (заканчивающийся формированием цист, протекающий в организме различных видов млекопитающих).
Именно ооцисты играют основную роль в передаче инфекции. Их формирование и развитие происходит в срок от 3 до 24 дней в слизистой оболочке тонкого кишечника кошки с последующим выделением в окружающую среду на протяжении 1–3 недель. За сутки с испражнениями одного животного выделяется до 10 млн ооцист, в которых в последующем при благоприятных условиях (около +25 °С) в течение 2–3 дней формируются споры, обладающие способностью длительного сохранения (до года) в окружающей среде (от –20 °С до +60 °С).
При пероральном попадании в организм млекопитающих из спор развиваются вегетативные формы токсоплазм, которые могут поражать различные клетки восприимчивого организма (за исключением эритроцитов) с образованием цист в скелетных мышцах, тканях сердца и центральной нервной системе. Внутри каждой цисты находится до нескольких тысяч паразитов. Цисты могут пожизненно присутствовать в организме иммунокомпетентных животных и человека без видимых клинических проявлений паразитарного заболевания.
При употреблении человеком в пищу инфицированного мяса происходит разрушение защитной оболочки цист с выходом брадизоитов, которые превращаются в тахизоитов и начинают активно поражать клетки нового хозяина путем проникновения через мембранную оболочку либо посредством фагоцитоза. Часть пораженных клеток разрушается при размножении токсоплазм с последующим заражением новых здоровых клеток, образованием зон некроза, формированием фиброза и кальцинатов. В случаях попадания в кровоток возбудители токсоплазмоза разносятся по всему организму с развитием диссеминированной формы поражения.
Клинические проявления
Специфические признаки заболевания, присущие именно токсоплазмозу, отсутствуют. При манифестных формах болезни по прошествии инкубационного периода (от нескольких недель до двух месяцев) появляется кратковременное лихорадочное состояние с умеренной гипертермией, общим недомоганием и слабостью, увеличением региональных лимфоузлов, печени и селезенки.
В подавляющем большинстве случаев токсоплазмоз завершается выздоровлением с формированием пожизненного устойчивого иммунитета. Однако у лиц с ослабленным иммунитетом возможна генерализации процесса с множественным поражением органов и тканей, летальным исходом на фоне развития полиорганной недостаточности.
По течению заболевания выделяют острую (до месяца), подострую (до 3 месяцев) и хроническую (более 3 месяцев) формы. По степени тяжести — легкую, среднетяжелую, тяжелую.
Действующая МКБ-10 предусматривает 6 типов заболевания:
- В58.0 Токсоплазмозная окулопатия
- В58.1 Токсоплазмозный гепатит (К77.0)
- В58.2 Токсоплазмозный менингоэнцефалит (G05.2)
- В58.3 Легочной токсоплазмоз (J17.3)
- В58.8 Токсоплазмоз с поражением других органов
- В58.9 Токсоплазмоз неуточненный
Особое значение токсоплазмоз имеет для беременных женщин: в первом триместре может привести к гибели плода на ранних сроках, в середине беременности — к тяжелым внутриутробным поражениями плода (гидроцефалия, поражения сердца, легких, печени, селезенки, органов зрения). Поражение токсоплазмозом плода в третьем триместре проявляется, как правило, спустя годы после рождения ребенка нарушением зрения и отставанием в психическом развитии.
Лабораторная диагностика
Комплекс лабораторных исследований включает:
1) неспецифические — общий и биохимический анализы крови. Выявляется снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов, повышение уровня трансаминаз и билирубина;
2) специфические:
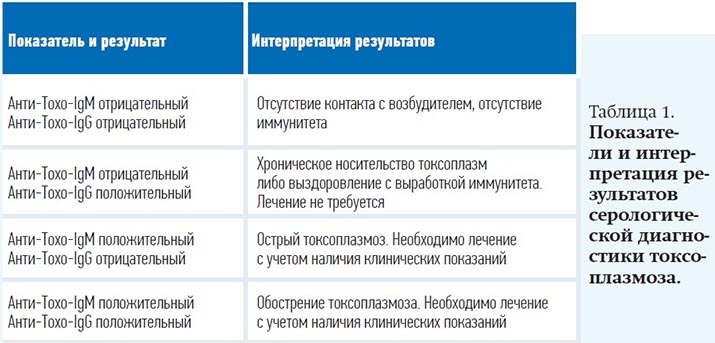
- проведение серологических исследований, направленных на выявление антител класса М (анти-Toxo-IgM) и G (анти-Toxo-IgG) к антигенам Toxoplasma gondii;
- молекулярно-биологическая детекция ДНК токсоплазм методом ПЦР в реальном времени в качественном и количественном вариантах;
- морфологическая визуализация структурных форм возбудителей токсоплазмоза в биоптатах органов и тканей методом микроскопии.
Кратковременный период нахождения Toxoplаsma gondii в крови и технические сложности в заборе биоптатов внутренних органов и тканей ограничивают применение молекулярно-биологических и морфологических исследований. Таким образом, серологическая диагностика в варианте иммуноферментного анализа является наиболее доступным и результативным методом для специфической лабораторной диагностики токсоплазмоза, выявления в анамнезе контакта с возбудителем протозооза, подтверждения выработки иммунитета в результате перенесенного заболевания (см. табл. 1).
Опыт РНПЦ ДОГИ
Для пациентов, находящихся на лечении в РНПЦ детской онкологии, гематологии и иммунологии, лабораторная диагностика токсоплазмоза имеет большую актуальность. C учетом иммунокомпрометированного состояния на фоне основной патологии, а также при подготовке и после проведения трансплантации костного мозга и гемопоэтических стволовых клеток существенно возрастает риск клинически выраженного первичного заражения токсоплазмозом (при нарушении правил профилактики болезни) либо активации имеющегося хронического носительства. Кроме того, в ряде случаев при направлении детей в РНПЦ ДОГИ по поводу различных жалоб на ухудшение состояния здоровья на фоне выхода за пределы норм показателей общего и биохимического анализов крови выявлялась субклиническая форма токсоплазмоза.
Лечение и предупреждение
К числу подлежащих этиотропному лечению относятся: лица с клинически выраженным обострением вызванного токсоплазмами хронического заболевания; беременные с доказанной формой первичного заражения Toxoplasma gondii; дети с врожденной формой токсоплазмоза; иммунокопрометированные люди в острой фазе (либо при активации хронического процесса) протозойного заболевания.
Продолжительность этиотропного лечения составляет 4 недели, при замедленной динамике до 6 недель. Согласно клиническому протоколу «Диагностика и лечение пациентов (взрослое население) с инфекционными и паразитарными заболеваниями», утвержденному постановлением Минздрава № 94 от 13.12.2018 г., назначают сульфаметоксазол/триметоприм 10 мг/кг по триметоприму в 2–3 приема внутрь или в 2–3 введения внутривенно. При остром токсоплазмозе, возникшем во время беременности, для профилактики инфицирования плода назначают: спирамицин (дорамицин) 3 млн МЕ внутрь 3 раза/сут до родов, чередуя 2 недели приема с 2 неделями перерыва.
Основополагающую роль в профилактике токсоплазмоза играет строгое соблюдение санитарно-гигиенических правил:
- запрет на употребление сырого либо недостаточно термически обработанного мяса и фарша;
- тщательное промывание водой выросших на земле овощей и зелени;
- обязательное мытье рук перед приемом пищи и после контакта с животными;
- проведение земляных работ на участке и уход за кошачьим туалетом в защитных перчатках.
Важным элементом профилактики внутриутробных и послеродовых осложнений токсоплазмоза является скрининг специфических антител к антигенам Toxoplasma gondii, позволяющий выявить наличие иммунитета, риск возникновения болезни либо активно протекающее заболевание, вовремя назначить и провести профилактику острого токсоплазмоза у беременных.