Нефробластома (опухоль Вильмса, WT) является наиболее распространенной опухолью почки у детей, которая может проявляться как в виде единичного узла, так и в виде мультифокального одностороннего поражения либо двусторонней опухоли.
В структуре злокачественных опухолей у детей нефробластома занимает четвертое место, следуя за гемобластозами, опухолями ЦНС и саркомами мягких тканей. Нефробластома составляет примерно 7–8 % всех злокачественных опухолей у детей.
Согласно данным Американского онкологического общества, ежегодно в США выявляется 500–600 новых случаев нефробластомы у детей, или 5 % от всех злокачественных опухолей. По данным детского канцер-субрегистра Республики Беларусь, ежегодно регистрируется 8–9 новых случаев нефробластомы на 1 млн детского населения, что также составляет 5 % от всех злокачественных опухолей. У 78 % детей опухоль диагностируется в возрасте 1–5 лет, пик заболеваемости приходится на 3–4-й год. У взрослых нефробластомы встречаются редко.
История вопроса
 Первым описал нефробластому немецкий патологоанатом и хирург Макс Вильмс. Едва ли он осознавал, что его диссертация «Смешанные опухоли почки» (1899) свяжет его имя с самой распространенной опухолью почки у детей. В своей работе он исследовал 9 (в основном больших по своим размерам) опухолей у детей в возрасте от 11 недель до 11 лет. Макс Вильмс описал опухоль как образование с округлыми клетками (миосаркома) с содержанием эпителиальных структур, в которых было установлено сходство с эмбриональной почкой. Он подозревал, что компонент, названный им круглоклеточной саркомой, представляет собой опухолевые эмбриональные клетки с потенциалом дифференцировки в мезенхиму и эпителий почки, и предположил его происхождение от «бластемы почки», связав онкогенез этих опухолей с почечной эмбриологией.
Первым описал нефробластому немецкий патологоанатом и хирург Макс Вильмс. Едва ли он осознавал, что его диссертация «Смешанные опухоли почки» (1899) свяжет его имя с самой распространенной опухолью почки у детей. В своей работе он исследовал 9 (в основном больших по своим размерам) опухолей у детей в возрасте от 11 недель до 11 лет. Макс Вильмс описал опухоль как образование с округлыми клетками (миосаркома) с содержанием эпителиальных структур, в которых было установлено сходство с эмбриональной почкой. Он подозревал, что компонент, названный им круглоклеточной саркомой, представляет собой опухолевые эмбриональные клетки с потенциалом дифференцировки в мезенхиму и эпителий почки, и предположил его происхождение от «бластемы почки», связав онкогенез этих опухолей с почечной эмбриологией.
В первой половине 20-го века хирургическое лечение было единственным методом терапии, частый летальный исход был отчасти обусловлен большими размерами опухоли. Ранняя попытка (1916) лечения неоперабельной нефробластомы при помощи рентгеновского облучения показала, что рентгеновские лучи могут уменьшить опухоль, и это дало первоначальный успех, но метод не получил широкого распространения. Постепенно методы хирургического лечения улучшались, что позволяло спасти часть детей, в частности с небольшими размерами опухоли. Прорыв произошел при комбинировании хирургического лечения с облучением и химиотерапией, о чем в 1956 году сообщила Сидни Фарбер с коллегами, в результате чего 2-летняя выживаемость составила 81 %. Следующим шагом стало создание двух основных исследовательских групп — NWTS и SIOP, которые оказали огромное влияние на успех лечения нефробластомы.
Национальная группа по исследованию опухоли Вильмса (NWTS, National Wilms Tumor Study Group, США), основанная в 1969 году, собрала большое количество пациентов и провела несколько клинических рандомизированных исследований, направленных на оптимизацию лечения для различных групп риска нефробластомы и определения возможных генетических факторов риска. Классификация нефробластомы культового патологоанатома Брюса Беквита, который твердо связал гистопатологию с прогнозами лечения и выявил опухоли с благоприятной или неблагоприятной морфологией, по-прежнему действительна для опухолей без предоперационного лечения.
В Европе небольшая группа преданных своему делу французских врачей в 1961 году открыла клуб детских онкологов, который в 1969 году был преобразован в SIOP — международное общество детских онкологов, членами которого сегодня являются медицинские специалисты из более чем 100 стран мира. SIOP сотрудничает с Группой изучения детского рака Соединенного Королевства (UKCCSG) и немецким Обществом детской онкологии и гематологии (GPOH).
Белорусские детские онкогематологи для лечения нефробластомы в прошлом использовали клинические протоколы как SIOP, так и NWTS. В настоящий момент для лечения детей применяется последний передовой протокол ренальной исследовательской группы SIOP — SIOP RTSG Umbrella, который объединил в себе протокольное лечение наиболее часто встречающихся злокачественных опухолей почек у детей.
Этиология и патогенез
Обычно нефробластома возникает спорадически, в 2 % случаев имеет семейный характер. В норме участки метанефрогенной бластемы, формирующие секреторный аппарат почки (клубочки, извитые канальцы), должны исчезать после 36-й недели беременности, однако у 1 % детей при рождении часть бластемы остается функционирующей. Эти фокусы бластемы описываются как нефрогенные остатки, которые определяются как участки с повышенным риском развития опухоли Вильмса. Судьба нефрогенных остатков двояка: они могут регрессировать или давать малигнизацию, постепенно трансформируясь в нефробластому.
Нефробластома нередко является одним из симптомов врожденных пороков и генетических синдромов. Врожденные аномалии выявляются в 12–15 % случаев опухоли Вильмса. Наиболее часто диагностируются следующие из них: аниридия, гемигипертрофия, синдром Беквита — Видемана, аномалия мочеполового тракта, WARG-синдром, синдром Дениса — Драша.
В начале 1970-х годов американский генетик Альфред Кнудсон, используя предыдущие разработки на гене Rb, предложил две модели туморогенеза при опухоли Вильмса. В первом случае имеет место развитие спорадической нефробластомы, при которой в нефробласте оба аллеля гена WT (Wilms tumor) повреждаются двумя независимыми соматическими мутациями; происходит полная инактивация данного гена, что приводит к развитию опухоли. Мутация носит гомозиготный характер, обнаруживается только в клетках опухоли и не наследуется. Наследственная форма нефробластомы характеризуется передачей мутированной копии гена WT из поколения в поколение. Каждый нефробласт гетерозиготного носителя мутации уже имеет инактивированный аллель WT. Таким образом, для развития нефробластомы достаточно всего одной соматической мутации, затрагивающей оставшуюся копию гена.
В настоящее время эта модель, оставаясь правильной по сути, представляется излишне упрощенной: в патогенез нефробластомы может быть вовлечено множество других генетических поломок.
Клиническая картина
Наиболее частый признак опухоли Вильмса — определяемая пальпаторно опухоль в брюшной полости. Нефробластома может длительное время протекать бессимптомно. Иногда отмечаются боли в животе. Гематурия может выявляться при микроскопическом исследовании. Гипертензия отмечается приблизительно у 25 % пациентов.
Гистологическое строение и классификация
Опухоли почки характеризуются гистологической гетерогенностью. Около 80 % случаев нефробластомы составляют классический вариант опухоли. Гистологическое стадирование предусматривает выделение 3 степеней злокачественности опухолей почки у детей, связанных с прогнозом заболевания. Стадирование применимо для опухолей, которые получали предоперационную химиотерапию, и опухолей, лечение которых началось с хирургического удаления.
Без предоперационной химиотерапии:
- низкий риск: мезобластическая нефрома, кистозная частично дифференцированная нефробластома;
- средний риск: неанапластические варианты нефробластомы, фокальная анаплазия;
- высокий риск: нефробластома — диффузная анаплазия, светлоклеточная саркома почки, рабдоидная опухоль почки.
С предоперационной химиотерапией:
- низкий риск: мезобластическая нефрома, кистозная частично дифференцированная нефробластома, полностью некротизированная нефробластома;
- средний риск: нефробластомы — эпителиальный, стромальный, смешанный, регрессивный типы, нейробластома — фокальная анаплазия;
- высокий риск: нефробластома — бластемный тип, диффузная анаплазия, светлоклеточная саркома почки, рабдоидная опухоль почки.
Клиническое стадирование
В настоящее время группы SIOP и NWTS используют единую систему стадирования нефробластомы, которая является определяющей для лечения:
- 1-я стадия — опухоль локализуется в пределах почки, возможно полное удаление;
- 2-я стадия — опухоль выходит за пределы почки, возможно полное удаление, в т. ч. прорастание капсулы почки, с распространением в околопочечную клетчатку и/или в ворота почки, поражение регионарных лимфатических узлов (стадия II N+); поражение внепочечных сосудов; поражение мочеточника;
- 3-я стадия — опухоль распространяется за пределы почки, возможно неполное удаление, в т. ч. в случае инцизионной или аспирационной биопсии, пред- или интраоперационный разрыв, метастазы по брюшине, поражение внутрибрюшных лимфоузлов (за исключением регионарных), опухолевый выпот в брюшную полость, нерадикальное удаление;
- 4-я стадия — наличие отдаленных метастазов;
- 5-я стадия — двусторонняя нефробластома; варианты двусторонних нефробластом включают: А — поражение одного из полюсов обеих почек; Б — поражение одной почки с вовлечением ворот в опухолевый процесс (тотальное или субтотальное) и одного из полюсов второй почки; С — поражение обеих почек с вовлечением в процесс ворот (тотальное или субтотальное).
Диагностика
Как и при других злокачественных опухолях, диагностика нефробластомы основана на морфологическом заключении. Однако в отношении нефробластомы допускается исключение из традиционного правила «проведение биопсии перед началом химиолучевой терапии».
Во время биопсии возникает нарушение целостности псевдокапсулы, и заключенный в псевдокапсулу опухолевый детрит, имеющий кашицеобразный характер, рассеивается по брюшной полости или по ходу иглы, что увеличивает распространенность опухоли, изменяет клиническую стадию заболевания (автоматически переводит в 3-ю стадию) и ухудшает прогноз. Поэтому у пациентов старше 6 месяцев и младше 16 лет диагноз нефробластомы устанавливают при консервативном обследовании.
Диагностика первичной опухоли основана на выявлении типичных признаков нефробластомы и исключении других заболеваний. В круг дифференциальных диагнозов входят пороки развития почки, гидронефроз, нейрогенные опухоли и другие опухоли забрюшинного пространства, опухоли печени, гамартома. Диагностика нефробластомы и определение стадии включает лабораторные и инструментальные исследования, такие как общеклинические анализы: общий анализ крови и мочи, биохимическое исследование крови, коагулограмма, онкомаркеры, исследование катехоламинов в моче.
Инструментальные методы обследования
- УЗИ органов брюшной полости и забрюшинного пространства — выявление опухоли в трех измерениях и определение объема опухоли. При УЗИ может быть визуализирован опухолевый тромб в нижней полой вене.
- Компьютерная томография органов брюшной полости и забрюшинного пространства с оральным и внутривенным контрастированием (см. рис. 1).
- Магнитно-резонансная томография брюшной полости и забрюшинного пространства без и с контрастным усилением (дает дополнительную информацию о распространенности и связи опухоли с окружающими органами).
- Ангиография выполняется при сомнениях в диагнозе. На ангиограммах обнаруживается патологическая сеть сосудов, выявляется источник кровоснабжения. Ангиографически возможно визуализировать опухолевый тромб в нижней полой вене.
- Радиоизотопное исследование почек — реносцинтиграфия, которая позволяет оценить как суммарную функцию почек, так и отдельно функцию каждой из них.
- Диагностика метастазов включает рентгенографию грудной клетки; при подозрении на метастазы в легкие — КТ органов грудной клетки. УЗИ брюшной полости и забрюшинного пространства также оценивает метастазы в регионарные лимфоузлы, печень, другие органы и ткани, выпот в брюшную полость.
Рисунок 1. КТ брюшной полости ребенка с большой нефробластомой с метастазами в печень.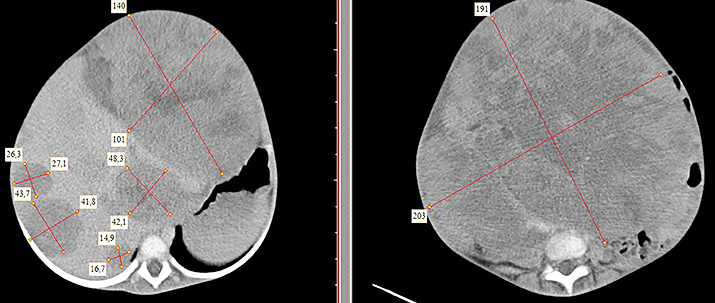
Лечение
Стандартным является комплексное лечение: химиотерапия, хирургическое лечение и лучевая терапия.
Химиотерапия: согласно протоколу SIOP, в течение 4 недель пациент получает предоперационную химиотерапию препаратами винкристин, дактиномицин для 2–3-й стадии; для 4-й стадии препаратами винкристин, дактиномицин, доксорубицин в течение 6 недель. Пациенты с 5-й стадией стадируются локально для каждой почки, и в зависимости от локальной стадии определяется режим предоперационной терапии.
Целью предоперационной химиотерапии является уменьшение размеров опухоли, что снижает риск интраоперационного разрыва псевдокапсулы, регресса метастазов. На 5-й неделе лечения при 2–3-й стадии и на 7-й неделе при 4-й стадии проводится предоперационное обследование, включающее общеклинические и инструментальные исследования, оценку ответа опухоли на химиотерапию.
Затем выполняется хирургическое лечение — радикальное удаление опухоли в объеме туморнефроуретерэктомии либо же резекции почки, биопсия регионарных лимфоузлов, метастазэктомия.
После операции и получения морфологического заключения проводится послеоперационное рестадирование, и в зависимости от гистологического варианта опухоли, поражения лимфоузлов, наличия метастазов либо же их тотального регресса/некроза определяется тактика послеоперационного лечения, которое может включать различные комбинации химиотерапевтических препаратов и добавление лучевой терапии в течение 26–34 недель.
Прогноз нефробластомы при выполнении программной терапии является хорошим. Выживаемость зависит от стадии заболевания и гистологического варианта. Независимо от прогностических факторов 90 % больных выздоравливают.
Общая выживаемость пациентов с нефробластомой в Республике Беларусь — 92 %, бессобытийная выживаемость — 90 %, что соответствует результатам лечения групп NWTS и SIOP.
Случай из практики
Девочка, 4 года. Мама обратила внимание на наличие дополнительного образования в животе. В связи с этим ребенок был госпитализирован в одну из областных клиник, проведено обследование, обнаружена опухоль брюшной полости. Ребенок переведен в РНПЦ ДОГИ для дообследования.
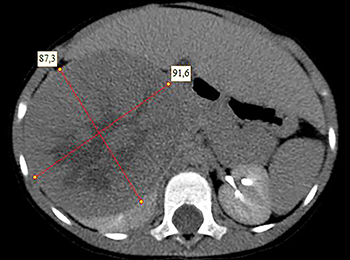 Клинически: при пальпации опухоль в проекции правой почки до 12 см в диаметре. Общеклинические исследования в пределах возрастной нормы. При КТ органов брюшной и грудной полости: КТ-картина объемного образования правой почки без признаков интрапульмональных метастазов (см. рис. 2). УЗИ брюшной полости: в проекции правой почки солидно-кистозное образование 101ґ114ґ99 мм, объемом 500 мл, васкуляризация активная, интактная часть почки 57ґ12ґ40 мм. Объемное образование правой почки — опухоль Вильмса. Предварительный диагноз: опухоль Вильмса правой почки, 2-я стадия.
Клинически: при пальпации опухоль в проекции правой почки до 12 см в диаметре. Общеклинические исследования в пределах возрастной нормы. При КТ органов брюшной и грудной полости: КТ-картина объемного образования правой почки без признаков интрапульмональных метастазов (см. рис. 2). УЗИ брюшной полости: в проекции правой почки солидно-кистозное образование 101ґ114ґ99 мм, объемом 500 мл, васкуляризация активная, интактная часть почки 57ґ12ґ40 мм. Объемное образование правой почки — опухоль Вильмса. Предварительный диагноз: опухоль Вильмса правой почки, 2-я стадия.
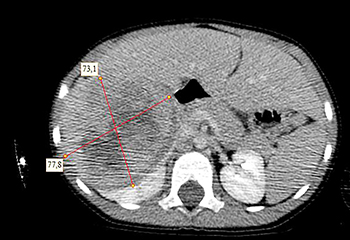 Ребенку проведена предоперационная химиотерапия. На 5-й неделе лечения КТ-контроль показал уменьшение опухоли в размерах до 90ґ80ґ100 мм (см. рис. 3).
Ребенку проведена предоперационная химиотерапия. На 5-й неделе лечения КТ-контроль показал уменьшение опухоли в размерах до 90ґ80ґ100 мм (см. рис. 3).
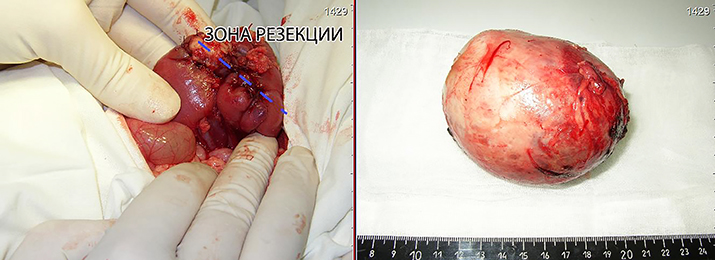
Выполнена операция: лапаротомия, удаление опухоли правой почки с ее резекцией. Гистологическое заключение: классическая нефробластома, промежуточная группа риска (см. рис. 4).
Послеоперационная программа включала еженедельное введение трех препаратов: винкристин, дактиномицин, доксорубицин на протяжении 27 недель. Девочка перенесла лечение удовлетворительно, без осложнений, находится в ремиссии более 5 лет.
Рисунок 4. Интраоперационная фотография: резецированная почка (справа), опухолевый узел (слева).