На 9-м Белорусском международном стоматологическом конгрессе проректор по учебной работе, заведующий кафедрой хирургической стоматологии и челюстно-лицевой хирургии Первого Санкт-Петербургского госмедуниверситета им. акад. И. П. Павлова, доктор мед. наук, профессор, президент стоматологической ассоциации России Андрей Яременко поделился опытом ведения крайне сложной категории пациентов — больных с постковидными остеонекрозами лицевого отдела черепа.
Жизнеугрожающая инфекция
 С 2020 года в клинических направлениях челюстно-лицевой хирургии и оториноларингологии выросло число пациентов с осложнениями после перенесенной коронавирусной инфекции. В том числе к таким осложнениям относятся вторичные инфекции, вызванные микроскопическими грибами, — инвазивные микозы с поражением костей лицевого отдела черепа, полости носа и околоносовых пазух.
С 2020 года в клинических направлениях челюстно-лицевой хирургии и оториноларингологии выросло число пациентов с осложнениями после перенесенной коронавирусной инфекции. В том числе к таким осложнениям относятся вторичные инфекции, вызванные микроскопическими грибами, — инвазивные микозы с поражением костей лицевого отдела черепа, полости носа и околоносовых пазух.
Андрей Яременко:
Грибная микрофлора сопровождает нас в течение всей жизни. Грибы прекрасно переживают неблагоприятные изменения внешней среды — кипячение, антисептики и т. д. Единственное, что они не могут пережить, — это система защиты организма, но до той поры, пока барьерные функции не дают сбой.
Так, в практике каждого стоматолога-хирурга встречались пациенты с длительно текущими периимплантитами, которые заканчивались удалением имплантата именно из-за присутствия там грибковой флоры.
Грибы неимоверно инвазивны, высокопатогенны и вирулентны. Среди разнообразия грибного мира есть два гриба, соседство с которыми фатально, — плесневые грибы рода Аspergillus и порядка мукоровых (в простонародье «черная плесень»).
Андрей Яременко:
Обширные зоны микотического поражения костей лицевого отдела черепа и околоносовых пазух — это жизнеугрожающие состояния. Но при грамотном ведении данной категории больных мы можем спасти огромное количество жизней.
Инвазивный аспергиллез путают с опухолевыми образованиями, поэтому челюстно-лицевые хирурги часто выполняют резекционные операции пациентам, имеющим эту инфекцию. А после биопсийный материал показывает присутствие друзов гриба. Еще хуже складывается ситуация с мукоромикозом. Противомикотического иммунитета у человека нет, организм защищен собственной неспецифической резистентностью. Но если мукор присоединяется к тем или иным патологическим процессам, это чревато катастрофическими последствиями для пациента.
COVID-ассоциированный мукоромикоз
Мукоромикоз — вторая (в некоторых странах находится на третьем месте) по частоте грибковая инфекция после аспергиллеза. Распространено заболевание в странах Юго-Восточной Азии и Азиатско-Тихоокеанского региона. В Северном полушарии он встречается в значительно меньшей степени. Тем не менее здесь его нельзя назвать редкой инфекцией.
Андрей Яременко:
Наш университет познакомился с этой патологией впервые именно у детей, получающих высокодозную химиотерапию и готовящихся к трансплантации костного мозга. Эти дети практически не имеют ни иммунитета, ни неспецифической резистентности. И именно они, к сожалению, сильно подвержены инвазивным микозам.
Первый маленький пациент клиники ПСПбГМУ с мукоромикозом приехал из Сирии. У него была молниеносно текущая синоорбитальная форма. Быстро стало понятно, что если мы не выполним ребенку резекцию верхней челюсти, он погибнет. В этот момент на хирурга ложится тяжелейшая моральная нагрузка — принять решение о резекции верхней челюсти ребенку на фоне протекающего у него острого лимфобластного лейкоза, не имея ни опыта такого хирургического вмешательства, ни опыта лечения такой патологии. Но было совершенно очевидно, что ребенок не выживет, если не попробовать хирургическую тактику. Маленький пациент был прооперирован, после ему были установлены протезы-обтураторы, которые периодически (по мере роста ребенка) меняются.
Клиницисты отмечают тревожный рост числа случаев мукоромикоза у пациентов с перенесенной коронавирусной инфекцией или активным ее течением. Связанный с COVID-19 мукоромикоз (COVID-19-associated mucormycosis, CAM, COVID-M) признан эпидемией в Индии. В этой стране зафиксировано почти 30 тысяч случаев COVID-M.
По данным международного многоцентрового исследования мукоромикозов, общая летальность составляет 24 % при синоорбитальной локализации заболевания без поражения ЦНС, с поражением ЦНС — 59 %. Почти половина выживших в этих двух группах теряет зрение.
Андрей Яременко:
Развитию CAM способствует не сама коронавирусная инфекция, а иммунодепрессивная терапия, назначенная пациенту для борьбы с вирусом. Она приводит к тому, что защитные силы организма резко слабнут, особенно это касается пациентов, получавших антицитокиновую терапию. Иначе победить инфекционно-токсический шок при COVID-19 нельзя, но расплата, к сожалению, может быть и в виде развития инвазивного мукоромикоза.
Факторы риска
Для COVID-ассоциированного мукоромикоза существует 2 группы факторов риска — экологические и факторы хозяина. Заболевание развивается, если окружающая среда способствует персистенции мукора, а хозяин при этом иммунологически скомпрометирован.
В анамнезе у таких пациентов:
- обязательный факт перенесенной либо переносимой коронавирусной инфекции;
- лечение в условиях ОРИТ, ПИТ;
- терапия ГКС и/или моноклональными антителами;
- высокопоточная оксигенотерапия (назальные, лицевые маски);
- повышенное содержание несвязанного железа;
- сахарный диабет, болезни почек, артериальная гипертензия.
Диагностика заболевания
Важная особенность — мукоромикоз никогда не начинается с поражения первичных слизистых оболочек, костной ткани челюстей. Он проявляется поражением придаточных пазух носа, причем главным образом начинается с верхнечелюстных пазух. Поэтому врачи-стоматологи и челюстно-лицевые хирурги, работающие в стационарах, где проходят лечение пациенты с COVID-19, должны внимательно осматривать их на наличие изолированных поражений верхнечелюстных пазух, которые резко ухудшают состояние здоровья больного без какого-либо предшествующего фона.
Андрей Яременко:
К сожалению, у части этих пациентов болезнь развивается уже после выписки из стационара. Дебют болевого синдрома в районе верхней челюсти обязательно должен насторожить врача, консультирующего человека по месту жительства. Подробный сбор анамнеза очень помогает в такой ситуации.
Клиническая картина дебюта инвазивного микоза:
- затруднение носового дыхания на фоне перенесенной или переносимой COVID-инфекции тяжелого течения;
- появление выделений из носа;
- выраженная сухость и заложенность носа;
- выраженные лицевые боли и боли в челюстях;
- онемение зубов и челюстей, мягких тканей лица;
- эпизоды декомпенсации сахарного диабета и артериальной гипертензии, ухудшение течения COVID-19.
Клинические проявления инвазивного мукоромикоза обусловлены главным образом некрозом тканей в результате ангиоинвазии и последующего тромбоза.
Чем моложе пациент, тем более драматичными будут последствия, т. к. эндотелий капилляров и микрососудистого русла этих пациентов не готов к сопротивлению такой агрессии.
Андрей Яременко:
Очень быстро развивается синдром краевого стояния форменных элементов крови, тромбозы и, как следствие, некрозы. Особенно в случае синоорбитальной формы заболевания клиника нарастает в часах, и не вовремя начатое лечение часто драматично.
Для установки верного диагноза важно содружество между инфекционистом, челюстно-лицевым хирургом, лором и стоматологом. Необходимо провести осмотр полости рта на предмет одонтогенных очагов инфекции, в которых может располагаться мукор, эндовидеоскопический осмотр полости носа и носоглотки, электроодонтометрию.
Андрей Яременко:
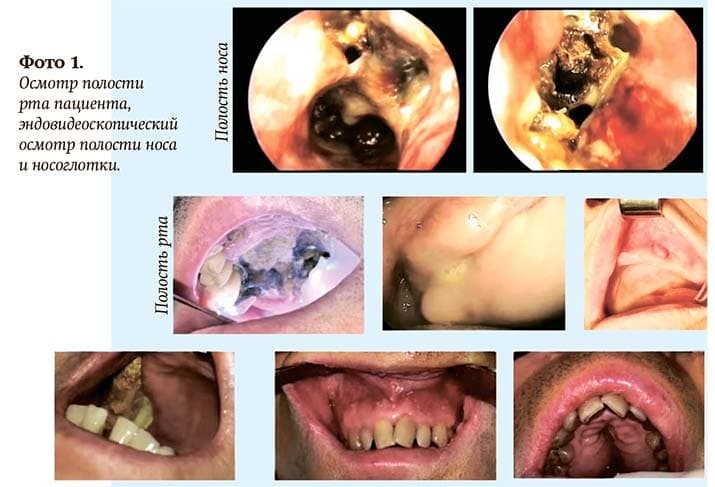
В полости носа мы можем увидеть черного цвета корки, оголение нижней носовой раковины, носовой перегородки. В полости рта наблюдаем оголение костной ткани челюстей, появление участков гиперемии и самое главное — признаки некроза (см. фото 1).
Лабораторно мукоромикоз подтверждается микроскопией биоптата и/или аспирата из пораженных зон с калькофлюором белым, посевом и гистологическим (окраска по Грокотту и PAS) исследованием материала из очага поражения.
Для лучевой диагностики необходимо проведение КЛКТ и МСКТ челюстно-лицевой области, дополненные внутривенным болюсным контрастным усилением для детальной оценки кровотока в пораженной зоне. Дополнительно проводится КТ органов грудной полости, живота и малого таза при выявлении распространения. Следует отметить, что конусно-лучевая компьютерная томография (КЛКТ) зубочелюстной системы значительно более информативна при диагностике этих поражений, нежели мультиспиральная компьютерная томография (МСКТ).
Андрей Яременко:
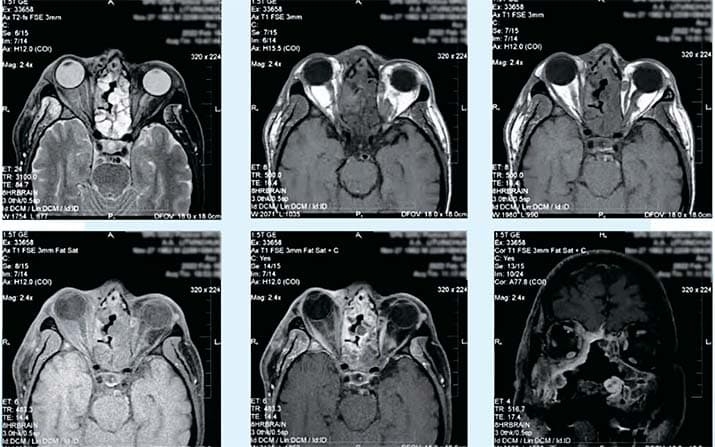
В лучевой диагностике мы увидим на фоне заболевания остеонекроз в бассейне верхнечелюстной артерии (см. фото 2–3). Это ранние признаки проявления некроза, которые четко указывают на то, что ждать больше нельзя — требуется хирургическое устранение очага. В ином случае омертвление тканей будет распространяться дальше.
Фото 2. МСКТ костей лицевого отдела черепа и сагиттальная проекция. Остеонекроз в бассейне левой верхнечелюстной артерии.
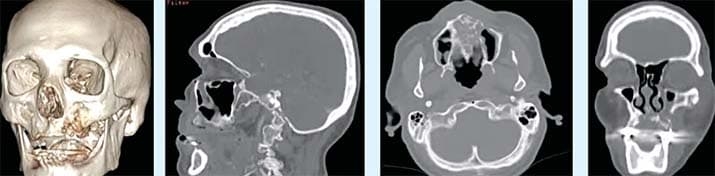
Фото 3. КЛКТ в просмотровом режиме MPR. Остеонекроз альвеолярного отростка справа, стенок правой верхнечелюстной пазухи, решетчатой кости справа, нижней и медиальной стенок правой орбиты.
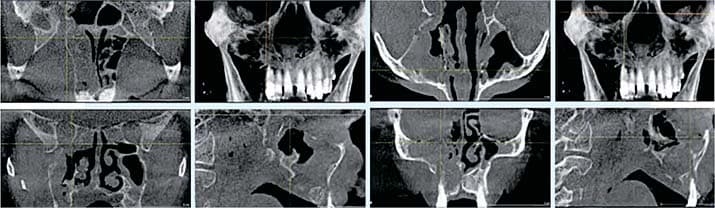
Магнитно-резонансная визуализация покажет степень и специфику распространения остеонекроза (см. фото 4).
Фото 4. МРТ орбит с контрастированием. Правосторонний экзофтальм. Ретробульбарная клетчатка с признаками отека. На фоне МР-отека мягких тканей интраорбитально в нижних и медиальных отделах правой орбиты определяются тканевые массы. Отсутствие контрастирования медиальной прямой мышцы справа. Незначительное скопление жидкости. Тканевые массы интимно прилежат к зрительным нервам сразу после выхода из зрительных каналов и ВСА на уровне отхождения глазничной артерии.
Лечение в условиях стационара
Обязательное условие успешного лечения мукоромикоза — ранняя антимикотическая терапия, хирургическое удаление пораженных тканей, контроль фонового заболевания и уменьшение выраженности иммуносупрессии.
В антимикотической терапии на первое место выходит антибиотик липосомальный амфотерицин В (в/в 5–10 мг/кг/с) или липидный комплекс АмВ (в/в 5 мг/кг/с). Препарат принимается не менее 14 дней. Важно использовать именно эти формы антибиотика, содержащие более устойчивые молекулы вещества. К обычному амфотерицину мукор практически нечувствителен.
После достижения стабилизации или при признаках почечной недостаточности лечение продолжается изавуконазолом (1-й и 2-й день — 600 мг в сутки, далее 200 мг в сутки) или позаконазолом (сироп 400 мг 2 раза в сутки или таблетки 300 мг 2 раза в первые сутки, затем 300 мг в сутки однократно независимо от приема пищи) не менее 6 недель с учетом лекарственных взаимодействий.
Вместе с этим идет комбинированная антибактериальная терапия, чтобы не присоединялась вторичная инфекция.
Андрей Яременко:
На фоне продолжающейся антимикотической терапии, контроля основных соматических заболеваний проводим хирургическую санацию с удалением всех пораженных тканей. В ходе вмешательства необходимо применять радикально исчерпывающую хирургическую тактику в пределах видимых здоровых тканей.
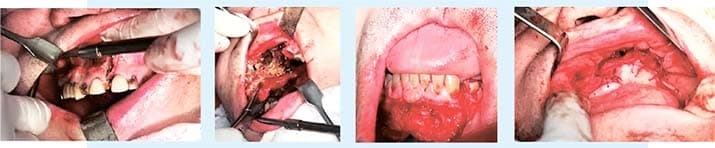
Типичная операция для распространенной формы мукоромикоза: внутриротовой доступ, резекция одной или двух верхних челюстей, содержимого носа (см. фото 5). Конечно, не хочется удалять такие огромные объемы тканей, обрекая пациента быть на многие годы клиентом реконструктивных клиник. Но, к сожалению, если мы этого не сделаем, процесс будет распространяться дальше.
Фото 5. Этапы хирургического вмешательства.
Несвоевременно начатая хирургическая тактика влечет за собой тотальное поражение обеих верхних челюстей, потерю глаза, орбиты, полную потерю лобной кости и т. д.
Практические рекомендации
- всем пациентам с сахарным диабетом, получающим гормонотерапию и оксигенотерапию, необходима рентгенография придаточных пазух носа или КЛКТ перед выпиской из ковидного стационара;
- неукоснительное соблюдение противоэпидемического режима кислородотерапии (для мукора там складываются идеальные условия — мокро, тепло и большое количество кислорода);
- при начальных признаках риносинусита — микологическое обследование;
- при развитии риноцеребральной формы мукоромикоза — немедленная радикальная хирургическая практика;
- обязательное включение в штат COVID-центров, а также в систему реабилитации лор-специалиста;
- обязательный доступ к микологическим исследованиям;
- включение лор-специалиста в схему диспансерного обследования больных с постковидным синдромом;
- ранняя консультация челюстно-лицевого хирурга при подозрении на деструктивный процесс.
В завершение Андрей Яременко подчеркнул, что для успешной реабилитации пациентов с сочетанной патологией лицевого черепа важны мультидисциплинарный подход, преемственность в комплексном обследовании и лечении с применением современного высокотехнологичного оборудования.