Проблемные вопросы интенсивной терапии новорожденных обсудили специалисты в ходе научно-практической конференции с международным участием, организованной БелМАПО. Предлагаем вашему вниманию самые актуальные аспекты прозвучавших выступлений.
Особенности гемостаза у новорожденных
Практически все тяжелые состояния сопровождаются нарушениями системы гемостаза, что повышает риск летальности и инвалидизации. Эта патологическая закономерность характерна для всех возрастов, но ведение таких пациентов в период новорожденности имеет свои особенности. С докладом на эту тему выступил профессор кафедры неонатологии БелМАПО, доктор мед. наук Георгий Шишко.
 Георгий Шишко:
Георгий Шишко:
Система гемостаза у новорожденных весьма неустойчива. Для них характерна быстрая трансформация капиллярного типа кровоточивости в гематомный, что сопровождается высоким риском кровоизлияний в головной мозг.
По результатам недавнего исследования с использованием стандартизированного и валидированного инструмента оценки неонатальных кровотечений (NeoBAT), 25 % всех новорожденных, поступавших в восемь различных отделений интенсивной терапии, перенесли эпизод кровотечения.
Наша задача не допустить такого развития событий, поэтому исследования системы гемостаза должны стать рутинным методом мониторинга в отделениях реанимации и интенсивной терапии новорожденных.
Как известно, система гемостаза человека представлена в двух звеньях: сосудисто-тромбоцитарное звено (первичный гемостаз) и плазменное звено (факторы свертывания крови в плазме).
Георгий Шишко:
Особенности сосудисто-тромбоцитарного звена гемостаза у новорожденных связаны с неонатальной транзиторной тромбоцитопатией или тромбастенией, а плазменного звена — с дефицитом витамина К. Причем дефицит этого витамина может предопределять дефицит К-зависимых факторов свертывания крови — II, VII, IX, X, а также факторов контакта XI и XII. Разумеется, это приводит к повышенному риску кровотечения.
Однако совсем недавно было установлено, что есть витамин К-зависимые антикоагулянты протеинов C и S и антитромбина III, дефицит которых может привести к развитию тромбоза. Этим объясняется неустойчивость системы гемостаза у новорожденных, то есть риски и кровотечений, и тромбозов, за тромбозом вдруг может последовать кровотечение и наоборот.
Специалист напомнил, что витамин К не переносится трансплацентарно из крови матери к плоду, а грудное вскармливание не обеспечивает потребности в витамине К новорожденного. Так, согласно рекомендациям американской ассоциации педиатров, потребность в витамине К составляет 4,8 мкг/кг/сутки, а его содержание в грудном молоке — 2–4 мкг/л.
Глобальная профилактика витамин К-дефицитного состояния для детей на естественном вскармливании проводится внутримышечным введением витамина К в родзале, и потом трижды еженедельно по 2 мг, что упреждает развитие поздней формы геморрагической болезни новорожденных.
В сравнении со взрослыми даже у здоровых новорожденных присутствует дефицит по всем факторам свертывания крови, но особенно он выражен у недоношенных, причем коррелирует со сроком гестации (см. табл. 1).
Таблица 1. Факторы гемокоагуляции у новорожденных по сравнению со взрослыми.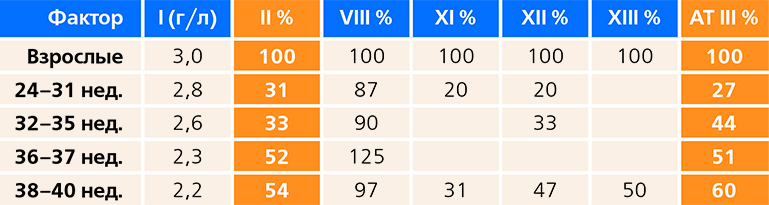 Исследование системы гемостаза у новорожденных представляет большие сложности.
Исследование системы гемостаза у новорожденных представляет большие сложности.
Георгий Шишко:
Показатели рутинной гемостазиограммы — АПТВ, ПТВ, МНО, фибриноген, ТВ — характеризуют только плазменное звено свертывающей системы, но не отражают состояние сосудисто-тромбоцитарного звена, состояние сгустка и фибринолиза. Трудности с оценкой показателей коагуляционных тестов возникают еще и потому, что в период новорожденности разброс референтных значений очень большой.
Например, у здоровых недоношенных (30–36 недель гестации) разброс АПТВ составляет 27,5–79,4 сек (у взрослых 26,6–40,3 сек). Поэтому дать рекомендации практическому врачу как ориентир для корригирующей терапии достаточно сложно, а может быть, даже бессмысленно.
По данным опубликованных исследований, риском геморрагического синдрома сопровождается пролонгирование ПТВ до 16 сек (чувствительность 0,7, специфичность 0,57 при положительной прогностической значимости 0,82), удлинение АПТВ до 55 сек (чувствительность 0,8, специфичность 0,95, при положительной прогностической значимости 0,8). Однако на практике нередко встречаются пациенты с абсолютным несоответствием показателей коагулограммы клинической картине. Георгий Шишко привел несколько примеров таких клинических случаев.
Поиск более достоверных и чувствительных методов исследования системы гемостаза у новорожденных ведется давно, одна из методик — тромбоэластография (ТЭГ), в ее основе — исследование кинетики кровяного сгустка. Образец крови помещается в специальную кювету, которая вращается с определенной скоростью. Выпадение фибрина на датчиках и изменение реологических свойств сгустка отражается в показателях тромбоэластограммы. У здоровых новорожденных после естественных родов в срок получены следующие параметры ТЭГ: R — 5,41 ± 1,34 мин, К — 1,62 ± 0,75, угол a — 65,39 ± 8,77°, МА (максимальная амплитуда) — 65,86 ± 5,81 мм.
Георгий Шишко:
Данные ТЭГ-профиля у недоношенных детей позволяют достаточно четко прогнозировать внутричерепные кровоизлияния. Есть определенная корреляция между показателями рутинной коагулограммы и ТЭГ, но степень чувствительности и диагностическая ценность показателей ТЭГ выше.
Кроме того, на основании результатов ТЭГ можно сделать выбор среди препаратов коррекции нарушений гемостаза. В частности, при пролонгировании R препаратом выбора является СЗП, при пролонгировании К и/или уменьшении угла a — криопреципитат, при снижении МА — тромбомасса или препарат DDAVP.
При доказанном тромбозе проводится тромболитическая терапия, с этой целью применяются: t-PA (Alteplasa, рекомбинантный тканевой активатор плазминогена) 0,1–0,5 мг/кг/час 6 часов; Streptokinase 2 000– 4 000 ЕД/кг за 10 мин, далее 1 000–2 000 ЕД/кг/час 6 часов; Urokinase 4 000 ЕД/кг за 10 мин, далее 4 000 ЕД/кг 6 часов.
Георгий Шишко:
Тромболитическая терапия у новорожденных сопровождается риском кровоточивости. При малейших признаках кровоточивости или гипокоагуляции необходимо переливание СЗП или криопреципитата. Уровень фибриногена при тромболитической терапии должен быть не менее 1,0 г/л, уровень тромбоцитов не менее 50ґ109/л. Учитывая высокий риск кровотечения при тромболизисе, мы рекомендуем поддерживать уровень фибриногена не менее 1,5–2,0 г/л дотациями криопреципитата.
Потенциально управляемые причины тяжелой патологии неонатального периода
Помимо нарушений гемостаза неонатологам приходится встречаться и с другими серьезными проблемами у новорожденных. Это гипоксия, инфекции (как внутриутробные, так и постнатальные, включая внутригоспитальные), недоношенность, гипербилирубинемия, ВПР, неврологические, легочные и другие последствия патологии перинатального периода. Заведующий кафедрой неонатологии БелМАПО, доцент, доктор мед. наук Юрий Устинович в своем выступлении обозначил моменты, на которые можно повлиять.
Гипоксия может возникать антенатально, интранатально и постнатально, оказывая многогранное негативное воздействие на организм, в т. ч. легочно-сердечную деятельность.
 Юрий Устинович:
Юрий Устинович:
Опыт работы отделений реанимации и интенсивной терапии новорожденных РНПЦ «Мать и дитя» показывает, что более 80 % доношенных и более 95 % недоношенных нуждаются в респираторной поддержке в том или ином виде.
Более 70 % доношенных и более 85 % недоношенных, которые находятся на респираторной поддержке, нуждаются в поддержке гемодинамики кардиотоническими, вазопрессорными препаратами, волемической экспансии.
Специалист подчеркнул важность адекватной диагностики гипоксии (КТГ, КОС, непрерывный мониторинг оксигенации) и подбора оптимального уровня респираторной поддержки (с позиций ее достаточности при наименьшей инвазивности).
Юрий Устинович:
Применение устройств с автоматической подачей кислорода на основе пульсоксиметрии пациента позволяет избежать или сократить частоту и длительность эпизодов гипоксии, но вместе с этим увеличивает эпизоды гипероксии. Следует об этом помнить при длительном лечении и не допускать любых эпизодов гипероксии, гипер- и гипокапнии, которые могут привнести негативный вклад в последствия, иногда даже более серьезный, чем основное заболевание. Возникают риски денатурации, повреждения растущего мозга ребенка, повреждения ДНК, что впоследствии может привести к онкопатологии.
При лечении и профилактике инфекций выбор антибактериальной терапии и ее контроль должен проводиться не только с позиции эффективности, но и безопасности. Классический пример — аминогликозиды с их нефро- и ототоксичностью.
Юрий Устинович:
Концентрационная способность почек у новорожденных очень ограничена. Поэтому важен контроль диуреза. Я предлагаю ориентироваться на возраст ребенка и физпотребности в жидкости, 60 % которой должен составлять диурез.
Например, у ребенка в возрасте 3 суток диурез должен быть 60 мл/кг/сутки, это 2,5 мл/кг/час. На 5-е сутки физпотребность 120 мл, следовательно, диурез 72 мл/кг/сутки или 3 мл/кг/час по этой формуле расчета. Если ребенок демонстрирует меньший темп диуреза, то в моче не может сконцентрироваться и выйти из организма все то, что мы в него ввели. Речь не только об аминогликозидах, но и о цефалоспоринах и других препаратах.
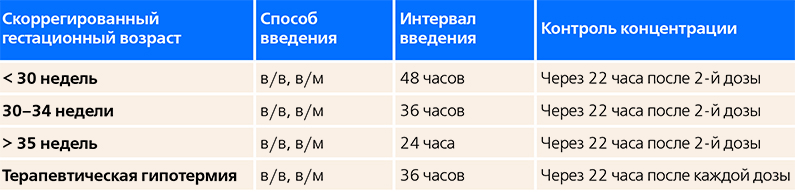
Юрий Устинович поделился наработанным опытом контроля концентрации гентамицина и коррекции дозировок с целью предотвращения его избыточного накопления в организме ребенка. Суть алгоритма в том, что после 2-й инъекции через 22 часа выполняется забор крови с определением концентрации препарата, и в зависимости от ее значений определяется время следующего введения препарата (см. табл. 2).
Таблица 2. Схема введения гентамицина (доза 5 мг/кг).
Гипербилирубинемия может быть неиммунной, изоиммунной по группе крови, резус-фактору или другим редким факторам.
Юрий Устинович:
Чтобы сформировать понятие о токсичности билирубина, задайте себе вопрос: почему у взрослого уровень билирубина 50–70 мкмоль/л расценивается как катастрофа, а новорожденного с 200 мкмоль/л выписываем домой? Какими последствиями это обходится, достоверно неизвестно. Лично я сторонник ранней активной терапии гипербилирубинемии, тем более все технические средства для этого у нас есть.
Нозокомиальные инфекции в ОРИТ новорожденных
Нозокомиальные (внутрибольничные или связанные с оказанием медицинской помощи) инфекции (НИ) обусловлены образованием и циркуляцией устойчивых штаммов микроорганизмов в лечебных учреждениях. Частота госпитального инфицирования новорожденных, по разным данным, составляет от 4 % до 7 %. Наиболее проблемные отделения — реанимации, интенсивной терапии, хирургии, выхаживания недоношенных.
Создаваемые с целью профилактики НИ системы инфекционного контроля обязательно должны быть адаптированы к условиям и особенностям конкретного учреждения и конкретного отделения. Об этом рассказала главный внештатный неонатолог Минздрава, доцент кафедры неонатологии БелМАПО, кандидат мед. наук Ирина Крастелева.
 Ирина Крастелева:
Ирина Крастелева:
Преждевременные роды являются наиболее важным фактором риска НИ. По данным американских исследователей, частота инфекций обратно пропорциональна массе тела при рождении и гестационному возрасту. При этом 50 % случаев инфицирования наблюдались у младенцев, родившихся в возрасте менее 25 недель или с массой тела менее 750 г. Показатели позднего неонатального сепсиса в разных центрах варьируют от 10,6 % до 31,7 % независимо от массы тела при рождении.
Многоцентровые исследования показывают, что за последние 20 лет произошли изменения в локализации и структуре возбудителей НИ. На первое место по частоте встречаемости вышли внутрибольничные пневмонии. Наиболее распространенный этиологический фактор: коагулазонегативный стафилококк, энтерококки, кишечная и синегнойная палочка, клебсиеллы, энтеробактерии и грибы рода Candida.
В последние годы чаще стали выявляться вирусные инфекции — респираторно-синцитиальный вирус, вирусы гриппа, парагриппа, риновирус. Ротавирусы и аденовирусы ассоциированы со вспышками заболеваний ЖКТ в ОРИТ и могут привести к некротизирующему энтероколиту.
К факторам риска НИ у новорожденных относятся длительная продолжительность парентерального питания с отсроченным энтеральным питанием, внутрисосудистая катетеризация, ИВЛ, вмешательства на ЖКТ, применение антибиотиков (АБ) широкого спектра действия.
Ирина Крастелева:
Наличие центрального венозного катетера (ЦВК) у младенца массой тела менее 1 500 г увеличивает риск развития сепсиса в 1,7 раза. Поэтому всегда следует взвешивать пользу и риск установки ЦВК, ежедневно оценивать необходимость в дальнейшем нахождении ЦВК в вене, немедленно удалять при отсутствии необходимости в нем. Постановку ЦВК и уход за ними следует поручать только обученному персоналу, периодически проверять владение навыками и соблюдение рекомендаций.
«Особенно высок риск возникновения катетер-ассоциированных инфекций (КАИ) при постановке пупочных катетеров. Нахождение катетера в пупочной артерии более 5 суток увеличивает риск развития сепсиса в 16 раз, а в пупочной вене — в 21 раз! Оптимальный срок для пупочного катетера — не более 5 суток, он может быть продлен при отсутствии признаков инфекции и асептическом уходе. Но при малейших признаках КАИ, сосудистой недостаточности или тромбоза пупочный катетер следует немедленно удалить и не заменять».
Результаты микробиологического исследования смывов из просвета удаленных сосудистых катетеров оказываются положительными в 1/3 случаев, как правило, доминирует коагулазонегативный стафилококк.
Смена повязки в области центрального венозного или пупочного катетера должна проводиться в стерильных условиях, замена — при любом загрязнении, намокании, ненадежной фиксации. Не рекомендуется рутинная противомикробная профилактика, использование мазей, кремов с АБ-препаратами, поскольку они могут поспособствовать развитию грибковой инфекции и резистентности к АБ-препаратам.
Ирина Крастелева:
Грибы рода Candida колонизируют кожу и слизистые 60 % новорожденных, находящихся в критическом состоянии, и могут быстро вызвать инвазивную грибковую инфекцию. Особенно высок риск инвазивного кандидоза у недоношенных с массой тела при рождении менее 1 000 г при лечении цефалоспоринами, применении двух АБ-препаратов, нахождении на парентеральном питании более 5 суток, наличии ЦВК. В таких случаях при развитии инвазивного кандидоза летальность достигает 70 %, а у выживших отмечается нарушение развития ЦНС.
Для предотвращения развития инвазивного кандидоза у недоношенных с массой тела при рождении менее 1 000 г или гестационным возрастом менее 27 недель рекомендуется введение флуконазола 3 мг/кг 2 раза в сутки, начиная с первых дней жизни ребенка до момента, пока не отпадет необходимость в центральном или периферическом венозном катетере.
Ирина Крастелева:
Для детей с массой 1 000– 1 500 г при рождении профилактика кандидоза рассматривается отдельно, с учетом частоты возникновения инвазивного кандидоза в отделении. Данных к развитию устойчивости к флуконазолу при таком режиме применения нет, хотя отмечается возрастающая устойчивость к нему во взрослых ОРИТ.
Главный внештатный неонатолог Минздрава напомнила, что наиболее простой и эффективный путь снижения НИ в родовспомогательных учреждениях — гигиена рук медперсонала, соблюдение правил дезинфекции и мытья рук.
Важный момент, о котором иногда забывают: вымытые руки нужно правильно вытереть одноразовым полотенцем. Многоразовые можно применять только при условии индивидуального использования с кратностью замены не реже 1 раза в рабочую смену.
Ирина Крастелева:
Мероприятия системы инфекционного контроля должны выполняться синергично и непрерывно, по принципу «все или ничего». Частичное или нерегулярное выполнение будет неэффективным и сведет все затраты и усилия к нулю. Например, строжайшее соблюдение всех правил асептики при постановке ЦВК может быть полностью перечеркнуто несоблюдением правил и алгоритмов ухода за катетером и его эксплуатации.
Терапевтическая гипотермия
Большой интерес участников конференции вызвал белорусский опыт применения терапевтической гипотермии для улучшения выхаживания и исходов младенцев, рожденных в асфиксии. Метод впервые был применен в 5-й ГКБ Минска в 2018 году. Полученные результаты представила врач-анестезиолог-реаниматолог отделения реанимации новорожденных 5-й ГКБ Минска Екатерина Дегтярева.
Екатерина Дегтярева сообщила, что внедренная методика аппаратной гипотермии с контролируемым индуцируемым снижением температуры применяется при средней и тяжелой форме гипоксической ишемической энцефалопатии. Самое главное — попасть в терапевтическое окно — до 6–15 часов после рождения, чем раньше, тем лучше. После этого времени у новорожденного прогрессирует вторичное повреждение головного мозга, и терапевтическая гипотермия (ТГ) уже не даст результата.
Аппаратная гипотермия на сегодняшний день применяется также в РНПЦ «Мать и дитя». Возможно, этого достаточно, поскольку детей, рожденных в тяжелой асфиксии, в нашей стране, к счастью, немного. По словам Ирины Ляховской, заведующей отделением анестезиологии и реанимации с палатами интенсивной терапии новорожденных детей Городского клинического родильного дома № 2 Минска, за год у них бывает 1–2 таких ребенка.
Ирина Ляховская:
Мы связываемся с коллегами из 5-го роддома и просим помочь, при этом необходимо согласование на уровне руководителей учреждений, что вызывает сложности, когда ребенок рождается ночью.
Ирина Ляховская внесла предложение о разработке четких алгоритмов действий при необходимости проведения ТГ новорожденному.
Это мнение поддержала Ирина Крастелева, добавив, что в перспективе нужно развивать ТГ в других крупных родовспомогательных учреждениях.
По данным ВОЗ, в мире рождается 4 млн детей в асфиксии, каждый четвертый ребенок после этого имеет стойкие нервно-психические отклонения. При гипоксической ишемической энцефалопатии летальность превышает 50 %.