Заведующая кафедрой акушерства и гинекологии с курсом ФПКиП ГомГМУ, кандидат мед. наук, доцент Татьяна Захаренкова свое выступление на республиканской научно-практической конференции с международным участием «Современные перинатальные медицинские технологии в решении проблем демографической безопасности» посвятила инфекционным факторам при преждевременных родах. «Медицинский вестник» знакомит читателей с этой работой.
Актуальность проблемы
 Татьяна ЗахаренковаЧастота преждевременных родов в разных странах варьирует от 4 % до 12 % всех родов, в Беларуси этот показатель составляет 4,3–4,5 %. Ежегодно в мире рождается 15 млн недоношенных детей и около 1 млн детей до 5 лет умирает по причине, связанной с преждевременным рождением.
Татьяна ЗахаренковаЧастота преждевременных родов в разных странах варьирует от 4 % до 12 % всех родов, в Беларуси этот показатель составляет 4,3–4,5 %. Ежегодно в мире рождается 15 млн недоношенных детей и около 1 млн детей до 5 лет умирает по причине, связанной с преждевременным рождением.
Выживаемость недоношенных новорожденных и состояние их здоровья в последующем связаны с гестационным возрастом при рождении, а также наличием осложнений и заболеваний, из которых внутриутробная инфекция (ВУИ) играет первостепенную роль. Поэтому приоритетное направление современного здравоохранения — прогнозирование, диагностика, лечение и профилактика преждевременных родов (ПР), что ведет к снижению предотвратимых случаев смерти новорожденных и детей до 5 лет.
Приблизительно 30–40 % преждевременных родов обусловлено наличием инфекции — как системной, так и локализованной в репродуктивных органах. Причиной ПР могут быть хориоамнионит и бессимптомно протекающие дисбиотические состояния половых путей, нередко недооцениваемые.
Урогенитальная инфекция в генезе ПР
Мы с коллегами провели ретроспективное исследование (Проблемы здоровья и экологии. 2021. Т. 18. № 3. С. 72–79), в ходе которого была обследована 431 беременная. У 353 женщин диагностирована урогенитальная инфекция (УГИ), при которой беременность в 49 % случаев протекала с угрозой прерывания, рецидивирующей в 17,6 % случаев (p=0,046), значимо чаще заканчивалась преждевременными родами — в 24,7 % случаев (р=0,009). Добавлю, что в этом исследовании мы установили важный фактор для управления рисками на этапе прегравидарной подготовки. Перенесенные до беременности УГИ и наличие заболеваний шейки матки значимо повышали риск УГИ при беременности (OR=2,1; 95% CI 1,28–3,45, р=0,005) и риск ВУИ (OR=2,85; 95% CI 1,46–5,55, р=0,003).
Наши данные согласуются с данными малазийского исследования, проведенного в 2023 году, когда были обследованы 237 женщин с ПР. Авторы (Ng B. K. et al.) показали, что у женщин с бактериальным вагинозом была значительно более высокая частота ПР до 34 недель, чем у беременных с нормальным биоценозом влагалища (22,7 % против 6,2 %, р=0,019). А исследование Haque M. M. 2017 года доказало, что нарушения вагинального микробиома в первом триместре беременности — прогностический критерий преждевременных родов.
Механизмы действия инфекционного агента при ПР были показаны в работе профессора Николая Рухляды «Бактериальный вагиноз как фактор риска преждевременных родов», опубликованной в 2019 году. Процесс можно представить в виде схемы (см. рис. 1).
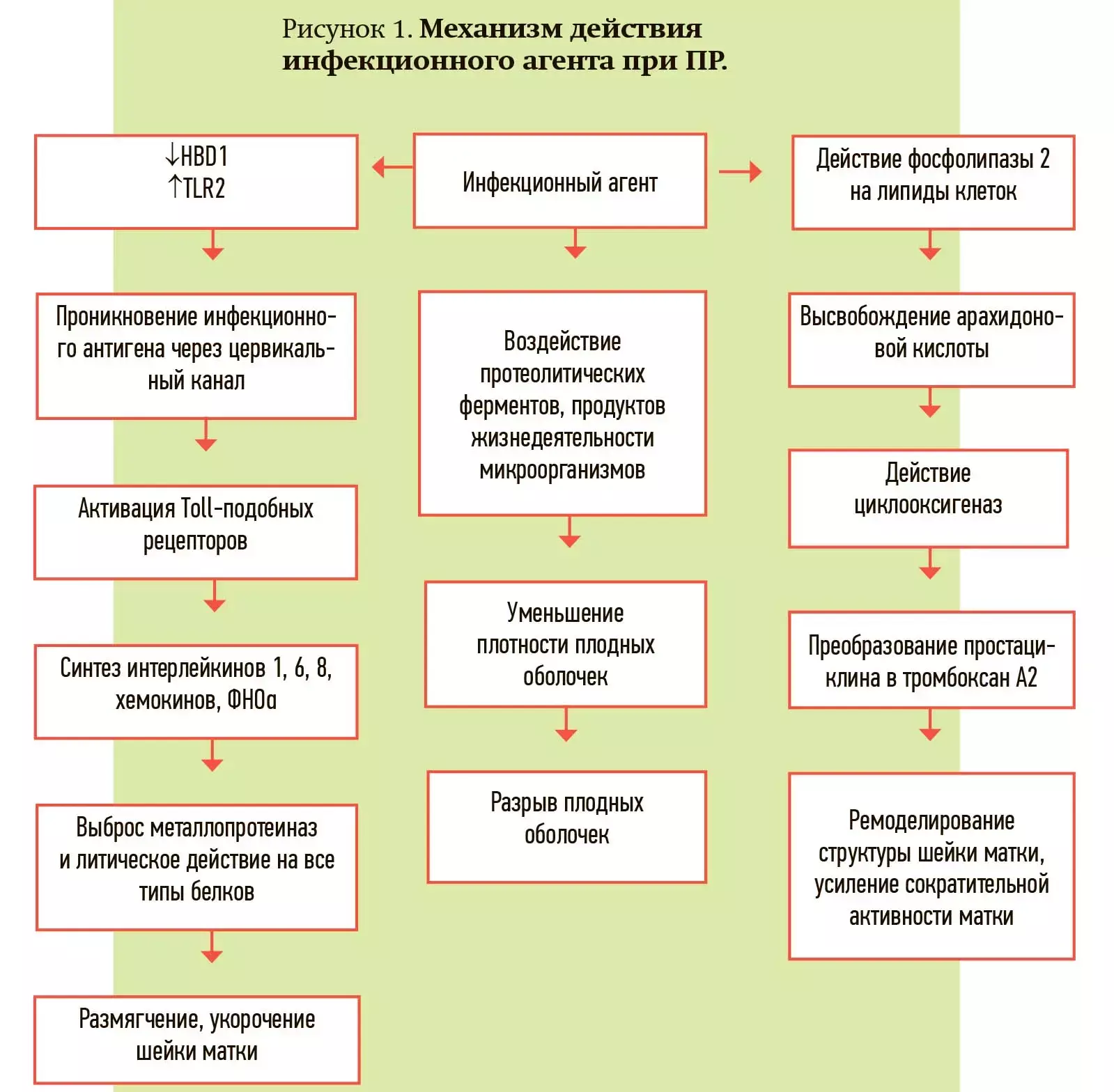
Не только наличие УГИ — фактор риска ПР, но и другие изменения микробиоценоза влагалища. Исследование, проведенное в Лондоне в 2017 году (Kindinger et al.), включающее 161 беременную, показало, что доминирование L.iners на 16-й неделе ассоциировалось с короткой шейкой матки менее 25 мм (р <0,05) и ПР до 34 недель (n=18; p <0,01; 69 % PPV). При этом применение вагинального прогестерона в дозе 400 мг/сут не снижало число ПР до 34 недель, связанных с L.iners, и не изменяло структуру вагинальных бактериальных сообществ.
Напомню также о единственном в настоящий момент зарегистрированном мультицентровом исследовании по интраамниальным инфекциям, проводимом с 2018 года (Испания, Чешская Республика, Швеция, Норвегия) «Неинвазивное получение внутриматочных образцов у женщин с ПР и целыми плодными оболочками». Изучается вопрос амниоцентеза и бактериологического исследования околоплодных вод при риске ПР для выбора дальнейшей тактики, если роды обусловлены инфекционным фактором.
При положительном результате посева околоплодных вод токолиз сомнительный, проводят профилактику респираторного дистресс-синдрома плода, переводят пациентку на более высокий технологический уровень, назначают нейропротекцию сульфатом магния и антибиотик. Результаты исследования, опубликованные в мае 2022 года, говорят о рентабельности стратегии в отношении улучшения неонатальных исходов (у недоношенных, рожденных до 30 недель) и конкретно в плане развития нервной системы в возрасте 1,2 года и 5 лет, а также снижения материнской инфекционной заболеваемости.
Но многие женщины и врачи сомневаются в амниоцентезе для диагностики интраамниальной инфекции при угрожающих ПР, так как инфицированные воды (когда выделяют микроорганизмы) наблюдаются только у 10–14 % женщин с ПР, а в 26 % при ПР наблюдается «стерильная» интраамниальная инфекция, когда только повышен интерлейкин-6. А в целом, как показало одно из наших исследований с применением метагеномного секвенирования, в околоплодных водах выделяется более 100 видов микроорганизмов даже при отсутствии воспаления. В то же время сама процедура амниоцентеза сопряжена с риском ПР.
Частота и структура УГИ у беременных в Беларуси
Актуальность УГИ у беременных обусловлена высокой частотой их распространенности.
По данным Министерства здравоохранения за 2023 год, в структуре заболеваемости беременных в нашей стране заболевания мочеполовой системы находятся на первом месте, составляя 25 %, на втором месте — анемия (20 %), на третьем — угроза прерывания беременности (15 %).
Для уточнения частоты встречаемости различных УГИ мы провели обследование беременных в первом триместре, причем протокольный скрининг (микроскопия и бактериологическое исследование отделяемого урогенитального тракта, ПЦР на C.trachomatis, M.genitalium) дополнили методами рН-метрии вагинальной жидкости и методом оценки биоценоза влагалища «Фемофлор-16».
Установлено, что 45 % в структуре УГИ у беременных составлял аэробный вагинит, по 16,5 % приходилось на бактериальный вагиноз (БВ) и вульвовагинальный кандидоз, 4,6 % — ИППП и 17,4 % — смешанные УГИ. В свою очередь при ПР только у 9,1 % беременных не было диагностировано УГИ, а частота встречаемости бактериального вагиноза составила 36,4 %. При этом частота случаев ВУИ новорожденных составила 63,6 %, а воспалительные изменения в плаценте обнаружены в 86,4 % случаев. У всех беременных с ПР уровень рН вагинальной жидкости был выше 4,5, составляя 5,8, что значимо превышало уровень рН в группе срочных родов (Z=4,028; р=0,0001).
Роль биоценоза
Исследования последних лет, посвященные роли биоценоза влагалища для исхода беременности, показали положительное значение лактобациллярного состава биоценоза с доминированием Lactobacillus crispatus, что ассоциируется с низким числом осложнений беременности и срочными родами. Благодаря методу метагеномного секвенирования нам удалось оценить роль состава микробиоты при ПР.
Примеры из практики
1. Первобеременная пациентка в первом триместре перенесла аэробный вагинит. На сроке 28 недель беременность осложнилась преждевременным разрывом плодных оболочек, а во время проведения профилактики респираторного дистресс-синдрома плода произошла преждевременная отслойка нормально расположенной плаценты. Женщина была родоразрешена путем экстренной операции кесарева сечения. Ребенок родился с ВУИ, а в плаценте наблюдались выраженные воспалительные изменения. При метагеномном секвенировании выявлено, что бактерии рода Lactobacillus во влагалище составляли только 66,1 %, что говорит о проявлении дисбиоза, а относительная представленность рода Mycoplasma составила 20,1 %. Видовое типирование показало, что доминирующими видами лактобацилл были Lactobacillus taiwanensis — 36,5 % и Lactobacillus gasseri — 22,4 %.
2. У первобеременной женщины с аэробным вагинитом при беременности, трихомониазом в анамнезе беременность протекала с 22 недель с нарушениями маточно-плацентарного кровотока. Спонтанные ПР произошли через естественные родовые пути на сроке 34–35 недель. Ребенок родился весом 2 120 г с врожденной пневмонией. В плаценте наблюдались париетальный децидуит, инволютивно-дистрофические изменения. Методом метагеномного секвенирования во влагалищном отделяемом в первом триместре установлено разнообразие лактобациллярной флоры с доминированием видов: Lactobacillus gasseri — 19,3 %, Lactobacillus taiwanensis — 19,1 %, Lactobacillus gigeriorum — 12,1 %.
3. Данный клинический случай демонстрирует вклад еще одного важного фактора, определяющего риск ПР при УГИ, так называемого цервикального замка. У повторнородящей пациентки выявлен в первой половине беременности уреаплазмоз, без лечения. На 21-й неделе при УЗИ выявлены признаки истмико-цервикальной недостаточности (ИЦН) с пролабированием плодного пузыря, формированием сладжа околоплодных вод. Понадобилась коррекция шейки матки швом после курса антибиотиков. На сроке беременности 32 недели произошли ПР. Ребенок родился весом 2 350 г без признаков ВУИ. При метагеномном секвенировании доминирующими видами явились Lactobacillus taiwanensis — 28,4 % и Lactobacillus iners — 18 %. Относительная представленность Ureaplasma parvum составила 7,9 %.
ИЦН как причина ПР и фактор риска ВУИ
Шейка матки — это иммунный орган, а в цервикальной слизи представлены иммуноглобулины A, G, M, лизоцим, лактоферрин, кальпротектин, элафин — секреторный лейкоцитарный ингибитор протеазы, дефензины, цитокины и хемокины (интерлейкины 1, 2, 4, 5, 6, 8, 10, 12, 13).
Проведенные нами исследования говорят, что значимым фактором риска ПР при ИЦН являются перенесенный аэробный вагинит (р=0,04) и расширение спектра условно-патогенных микроорганизмов во влагалищном биотопе.
После коррекции ИЦН пессарием в 8,9 % случаев формируется сладж околоплодных вод, что в 75 % заканчивается ПР. Таким образом, важен УЗ-контроль и после введения пессария для своевременной диагностики сладжа и назначения необходимого лечения. У пациенток с ИЦН и последующими ПР в 7,3 раза чаще, чем при срочных родах, наблюдается гистологический хориоамнионит (OR=7,3; 95% CI 1,8–29,2; р=0,0005), что ассоциируется с преждевременным разрывом плодных оболочек (r=0,34; р=0,023), а реализация ВУИ при ПР бывает в 3 раза чаще (OR=3,0; 95% CI 1,2–7,6; р=0,017).
Исходы беременности при наличии сладжа околоплодных вод были оценены на 2 432 женщинах в 17 исследованиях, результаты опубликованы в 2020 году (V. Pergialiotis, I. Bellos, A. Antsaklis, D. Loutradis, G. Daskalakis). Авторами установлено, что при беременности, осложненной сладжем околоплодных вод, роды происходят в меньшем гестационном сроке, увеличиваются частота ПР и госпитализаций новорожденных в ОАРИТ, уровень неонатальной смертности.
Местное лечение
Предпочтительно местное лечение УГИ при беременности, основным принципом является восстановление нормальной микрофлоры. На первом этапе назначают лекарственные препараты, обладающие антибактериальной активностью. Для этой цели с успехом применяют антисептики, которые разрешены с первого триместра (хлоргексидина биглюконат, повидон-йод, деквалиния хлорид); антианаэробные лекарственные препараты, содержащие нитроимидазолы (метронидазол, тернидазол) или клиндамицин; комбинированные лекарственные средства, обладающие активностью в отношении аэробов, анаэробов и дрожжеподобных грибов Сandida (тернидазол + неомицина сульфат + нистатин + преднизолон); комбинация двух бактерицидных антибиотиков и нистатина, продемонстрировавшая эффективность в отношении бактериального вагиноза (неомицина сульфат + полимиксина В сульфат + нистатин). На втором этапе назначаются лекарственные средства, содержащие влагалищные лактобациллы, что позволяет восстановить нарушенное равновесие микрофлоры влагалища.
Тактика ведения пациенток со сладжем околоплодных вод и риском ПР предполагает системную антибактериальную терапию. В случаях, когда при ИЦН нет признаков интраамниальной инфекции, возможна коррекция ИЦН как с применением прогестерона, так и с введением пессария или методом хирургического серкляжа.
Наличие сладжа при ИЦН всегда нужно расценивать как признак интраамниальной инфекции, что обосновывает назначение антибактериальных лекарственных средств. При этом введение пессария или хирургический серкляж должны быть отсрочены, и остается возможным использование микронизированного прогестерона.
Назначение беременным с ИЦН и сладжем антибактериальных лекарственных средств широкого спектра действия приводит к исчезновению сладжа, наблюдается эрадикация бактерий, по данным контрольного исследования околоплодных вод. Согласно результатам исследований, эффективность антибактериального лечения зависит от длительности воспалительного процесса в полости матки, а также от инфекционно-обусловленных осложнений беременности, таких как выраженность ИЦН и наличие пролабирования оболочек, тонус миометрия.
В каких случаях антибиотики снижают риск ПР?
Исследование Thinkhamrop J. в 2015 году с участием 4 300 женщин показало, что антибиотикопрофилактика не снижала риск преждевременного разрыва плодных оболочек и ПР в целом, за исключением подгруппы женщин с ПР в анамнезе, у которых был БВ. В российском исследовании 2021 года доказана эффективность применения системной антибактериальной терапии у беременных с субклинической внутриматочной инфекцией, на фоне которой наблюдается снижение риска ПР в 2 раза, а риска экстремально ранних ПР — в 10 раз (Асташкина М.В. Профилактика экстремально ранних преждевременных родов у женщин с внутриматочной инфекцией).
В свою очередь нужно помнить о том, что системная антибактериальная терапия может нарушать микробиоценоз влагалища. Нами было установлено, что лечение осложненной УГИ макролидами у 46 беременных женщин сопровождалось через 30 дней увеличением во влагалищном биоценозе G.vaginalis/P.bivia/ Porph.spp., концентрация которых до лечения была 4,1 (3,6; 6,3) ГЭ/мл, а на 30-й день составила 6,1 (4,3; 7,8) ГЭ/мл. Показатели Atopobium vaginae составили 4,4 (3,4; 5,7) ГЭ/мл и 5,2 (2,8; 7,1) ГЭ/мл соответственно до и после лечения.
Кроме того, лактобациллы обладают чувствительностью к большинству антибиотиков широкого спектра, о чем свидетельствуют исследования, проведенные А. А. Мелкумян на базе лаборатории микробиологии отдела микробиологии, клинической фармакологии и эпидемиологии НМИЦ АГП им. В. И. Кулакова Минздрава России (см. рис. 2).
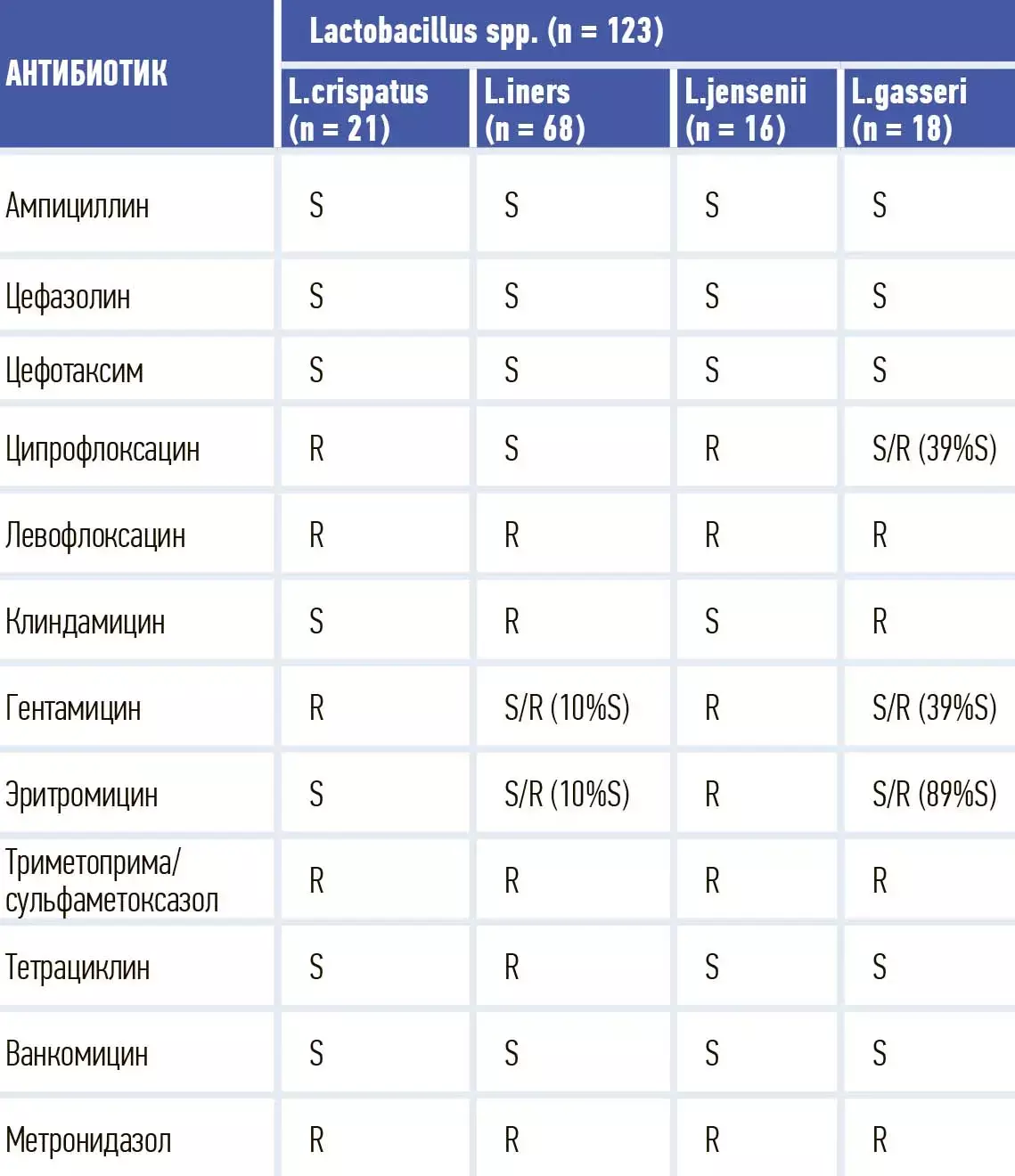
Таким образом, оценка биоценоза влагалища после курса антибиотикотерапии желательна, а обоснованное восстановление лактобациллярного доминирования во влагалищном биотопе — фактор повышения колонизационной резистентности влагалища и профилактики преждевременных родов инфекционного генеза.
Исследование, проведенное Chen еt al в 2022 году, доказывает, что пробиотики могут играть активную роль в лечении БВ, при этом лечебный эффект пробиотиков сопоставим с антибиотиками, а сочетание антибиотиков и пробиотиков продемонстрировало лучшие результаты, чем монотерапия антибиотиками. При этом пероральное введение L.rhamnose для лечения БВ было даже более эффективным, чем вагинальное применение.
Выводы
1. Значимые факторы риска ПР — это нарушения биоценоза влагалища у беременной, механическая и иммунная несостоятельность шейки матки.
2. Своевременная диагностика дисбиотических и воспалительных заболеваний влагалища, их адекватное лечение с этапом восстановления микробиоты способствуют благоприятному пролонгированию беременности.
3. Развитие интраамниальной инфекции, основными признаками которой могут являться ИЦН и формирование сладжа околоплодных вод, служит показанием для проведения системной антибактериальной терапии с этапом коррекции биоценоза урогенитального тракта, и только на втором этапе — коррекция ИЦН пессарием или хирургическим серкляжем.
